Clear Sky Science · it
APOE4 aggrava la patologia della proteina tau indotta dall'ormone dello stress glucocorticoide tramite disfunzione mitocondriale
Perché lo stress e i geni della memoria ci riguardano tutti
Molte persone temono che periodi prolungati di stress possano aumentare le probabilità di sviluppare problemi di memoria più avanti nella vita. Allo stesso tempo, una variante genetica comune chiamata APOE4 è nota per aumentare significativamente il rischio di morbo di Alzheimer. Questo studio mette insieme questi due filoni, chiedendosi come gli ormoni dello stress e APOE4 interagiscano all'interno delle cellule cerebrali e se tale interazione possa indicare nuovi modi per proteggere il cervello che invecchia.
Come un gene di rischio comune incontra lo stress quotidiano
I ricercatori si sono concentrati su APOE4, una versione di una proteina che gestisce il colesterolo e che è presente in milioni di persone nel mondo. Hanno abbinato questo background genetico all'esposizione a glucocorticoidi, i principali ormoni dello stress rilasciati durante la pressione psicologica cronica. Utilizzando topi ingegnerizzati per portare l'APOE umano APOE3 (la versione più neutra) o APOE4, e neuroni coltivati dai loro cervelli, hanno osservato l'ippocampo, un centro della memoria particolarmente sensibile sia allo stress sia al morbo di Alzheimer. L'obiettivo era verificare se APOE4 renda questi neuroni più vulnerabili agli effetti nocivi degli ormoni dello stress.
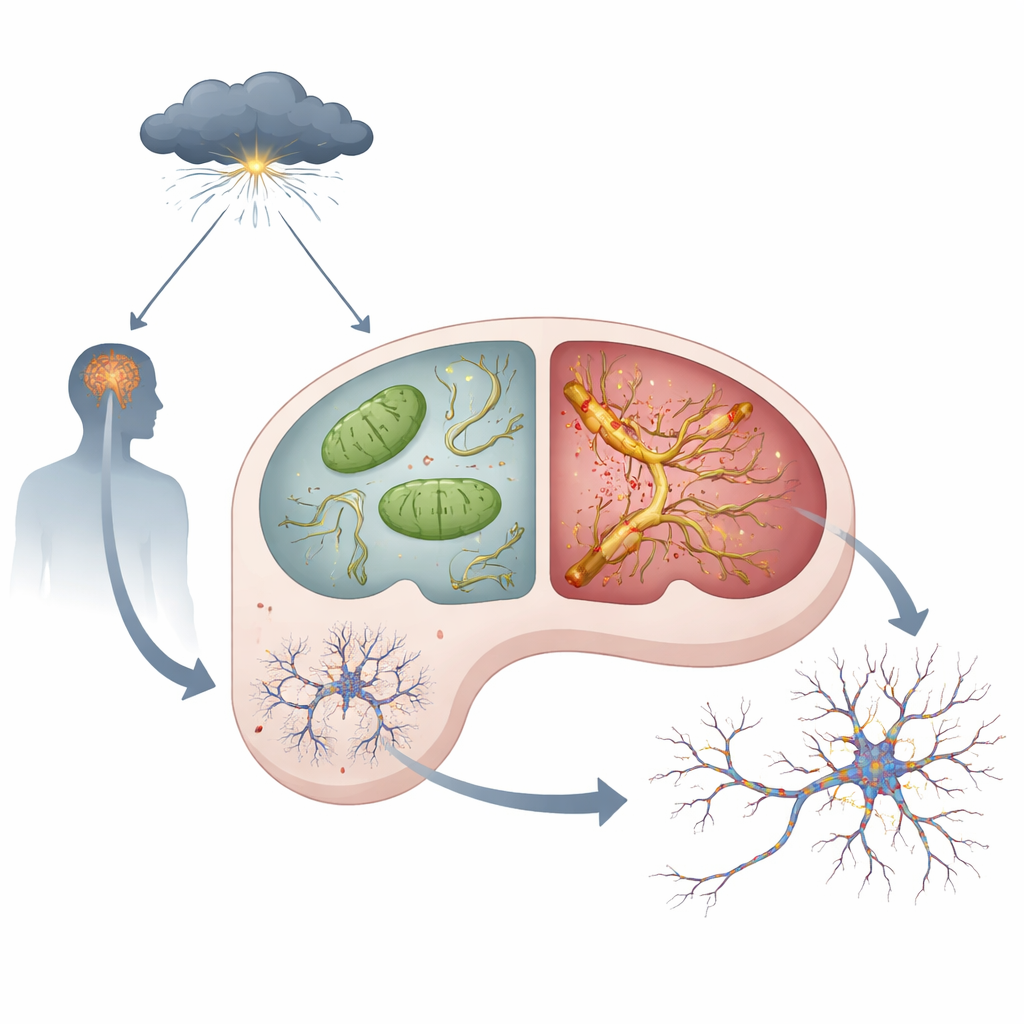
Ormoni dello stress, centrali energetiche difettose e tau tossica
All'interno di ogni neurone ci sono i mitocondri, minuscole centrali che generano l'energia necessaria per pensare e ricordare. Il gruppo ha riscontrato che, anche in condizioni di calma, i topi APOE4 mostravano segni di problemi mitocondriali nell'ippocampo: più sottoprodotti reattivi dell'ossigeno, attività più debole di un complesso chiave della produzione energetica e livelli inferiori di ATP, la valuta energetica della cellula. Quando gli animali sono stati trattati con dosi elevate di un ormone sintetico dello stress che imita lo stress cronico, questi problemi sono peggiorati nei topi APOE4 rispetto ai topi APOE3. Contemporaneamente, una proteina chiamata tau — che normalmente aiuta a stabilizzare le “rotaie” interne della cellula — ha cominciato ad accumularsi, a essere modificata in eccesso, ad aggregarsi e a diffondersi da neurone a neurone. Questi cambiamenti della tau, spesso indicati come patologia della tau, erano molto più pronunciati e si propagavano maggiormente nei cervelli APOE4 esposti agli ormoni dello stress.
Segnalazione dello stress iperattiva nei cervelli vulnerabili
Lo studio ha anche esaminato quanto intensamente le cellule cerebrali rispondessero ai segnali di stress. I glucocorticoidi agiscono attraverso recettori che normalmente risiedono nel citoplasma cellulare e si spostano nel nucleo e nei mitocondri quando attivati. Nei topi APOE4 questi recettori erano già più attivi a riposo e si spostavano più facilmente nel nucleo e nei mitocondri, nonostante i livelli globali di ormone nel sangue fossero simili a quelli degli animali APOE3. A sostegno di ciò, animali e neuroni APOE4 mostravano livelli più alti di proteine di supporto che favoriscono l'attivazione dei recettori e profili di espressione genica coerenti con una segnalazione degli ormoni dello stress più intensa. In colture cellulari, dosi molto basse di ormone dello stress che avevano scarso effetto sui neuroni APOE3 erano sufficienti a danneggiare i mitocondri e a indurre accumulo e rilascio di tau nei neuroni APOE4, dimostrando che questo background genetico abbassa la soglia per il danno legato allo stress.
Un poro critico nei mitocondri e una possibile via d'intervento
Approfondendo, i ricercatori si sono focalizzati sul poro di transizione della permeabilità mitocondriale (mPTP), un canale che può aprirsi nella membrana interna del mitocondrio. Quando questo poro si apre, i mitocondri perdono la loro carica elettrica, rilasciano molecole reattive dannose e possono spingere le cellule verso la disfunzione. Nei neuroni APOE4, anche un'esposizione modesta agli ormoni dello stress era sufficiente ad aumentare i livelli di ciclophilina D, un regolatore chiave del poro, e a innescarne l'apertura. Bloccare questo poro con due farmaci diversi — uno che interferisce direttamente con la ciclophilina D e un altro che attenua la produzione di ossidanti mitocondriali (mito-apocynin) — ha protetto i neuroni APOE4 dalla perdita energetica, dall'eccesso di molecole reattive e dai cambiamenti della tau.
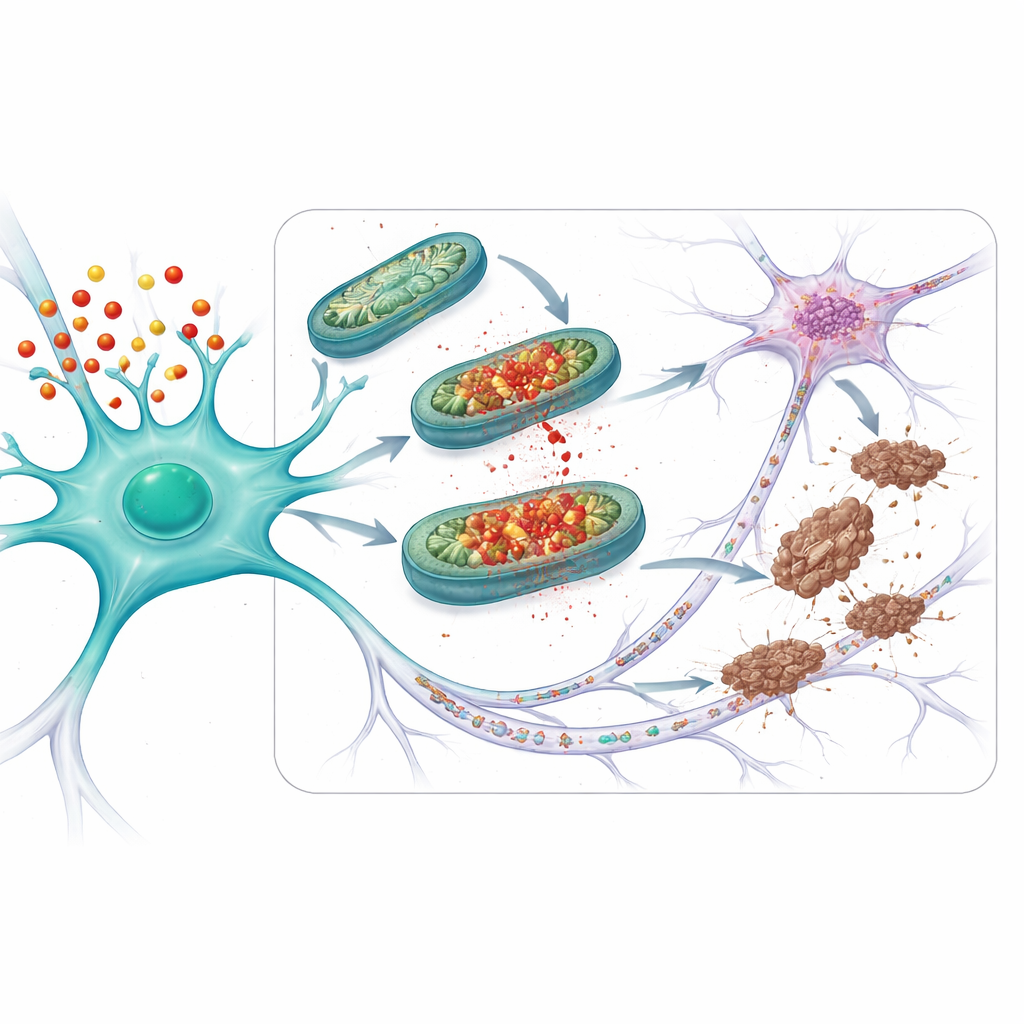
Proteggere le connessioni e il cervello che invecchia
Il gruppo ha poi valutato se questa strategia protettiva funzionasse in contesti più simili alla malattia. Hanno studiato topi che non solo portavano APOE4 ma producevano anche una forma mutante di tau che forma facilmente grovigli. In questi animali, i problemi mitocondriali, la tau anomala e la perdita di sinapsi — i punti di connessione tra neuroni — erano tutti peggiori rispetto ai topi con la versione più sicura APOE3. Il trattamento dei topi APOE4 con mito-apocynin, iniziato prima della comparsa di sintomi evidenti, ha ridotto il danno mitocondriale, i cambiamenti della tau e la perdita di sinapsi. In topi APOE4 più anziani con problemi di tau che emergevano naturalmente (anche senza tau mutante aggiunta), un trattamento a breve termine con mito-apocynin ha analogamente ripristinato la funzione mitocondriale, ridotto la tau anomala e limitato la diffusione della tau tra i neuroni.
Cosa significa per le persone a rischio
In termini semplici, questo lavoro suggerisce che APOE4 rende le centrali energetiche delle cellule cerebrali più fragili e i loro interruttori di risposta allo stress più facilmente attivabili. Quando si aggiungono ormoni dello stress cronico, questa combinazione accelera la cascata che va dal danno mitocondriale all'accumulo tossico di tau, alla sua diffusione e alla perdita di connessioni cerebrali. Crucialmente, lo studio mostra che bloccare un poro mitocondriale specifico può interrompere questa cascata nei modelli APOE4. Pur servendo molta altra ricerca prima che qualsiasi trattamento possa raggiungere i pazienti, prendere di mira questo poro — e gestire lo stress cronico, specialmente nei portatori di APOE4 — potrebbe entrare a far parte delle strategie future per rallentare o prevenire i danni legati all'Alzheimer.
Citazione: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Parole chiave: APOE4, stress cronico, mitocondri, patologia della tau, morbo di Alzheimer