Clear Sky Science · pt
APOE4 agrava a patologia de tau induzida pelos hormônios do estresse glucocorticoides via disfunção mitocondrial
Por que genes do estresse e da memória importam para todos nós
Muitas pessoas se preocupam que longos períodos de estresse possam aumentar as chances de desenvolver problemas de memória mais tarde na vida. Ao mesmo tempo, uma variante genética comum chamada APOE4 é conhecida por aumentar fortemente o risco de doença de Alzheimer. Este estudo reúne essas duas linhas, investigando como os hormônios do estresse e o APOE4 interagem dentro das células cerebrais e se essa interação pode apontar para novas maneiras de proteger o cérebro envelhecido.
Como um gene de risco comum se encontra com o estresse do dia a dia
Os pesquisadores focaram no APOE4, uma versão de uma proteína que regula o transporte de colesterol e que é carregada por milhões de pessoas no mundo. Eles combinaram esse contexto genético com exposição a glucocorticoides, os principais hormônios do estresse liberados durante pressão psicológica crônica. Usando camundongos modificados para carregar o APOE3 humano (a versão mais neutra) ou o APOE4, e neurônios cultivados a partir de seus cérebros, eles se concentraram no hipocampo, um centro da memória especialmente sensível tanto ao estresse quanto à doença de Alzheimer. O objetivo era ver se o APOE4 torna esses neurônios mais vulneráveis aos efeitos nocivos dos hormônios do estresse.
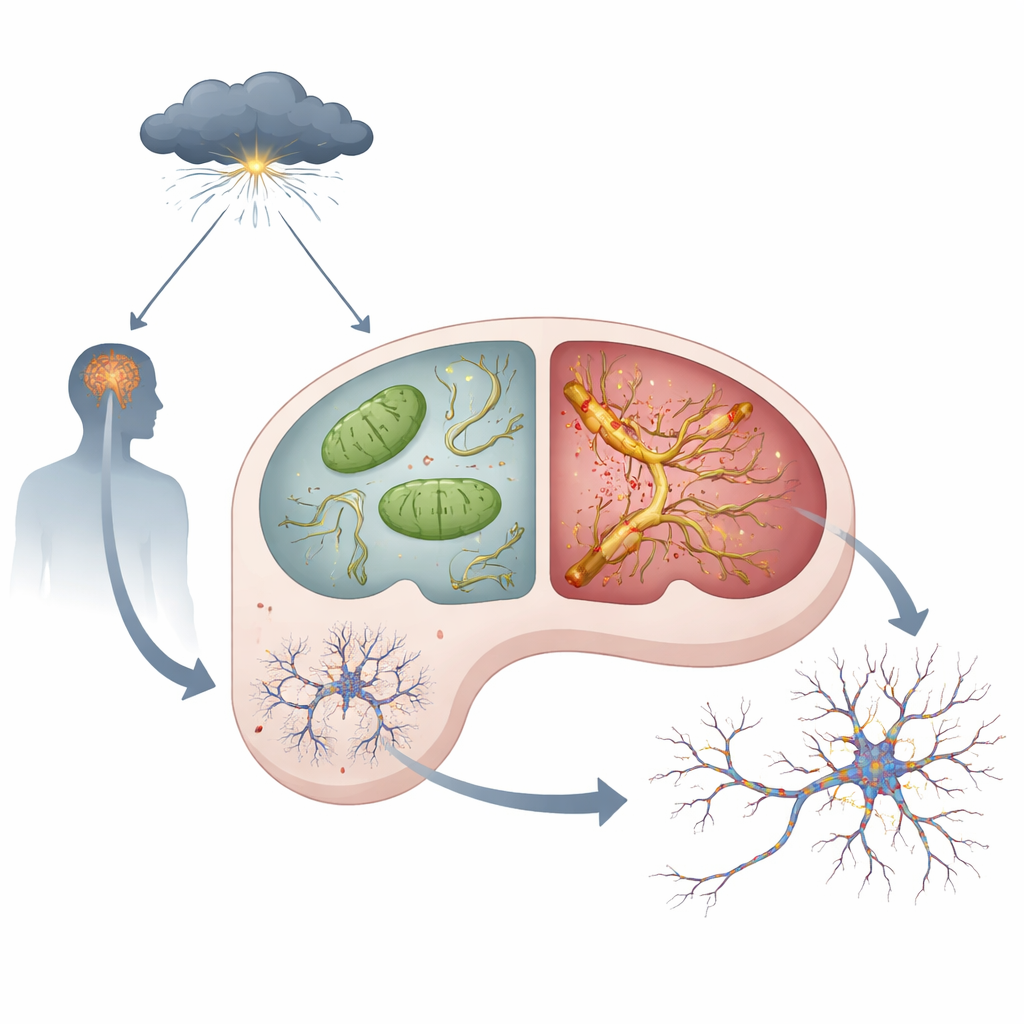
Hormônios do estresse, centrais de energia defeituosas e tau tóxico
Dentro de cada neurônio estão as mitocôndrias, pequenas centrais que geram a energia necessária para pensar e lembrar. A equipe descobriu que mesmo em condições calmas, camundongos APOE4 exibiam sinais de problemas mitocondriais no hipocampo: mais subprodutos reativos do oxigênio, atividade reduzida de um complexo chave gerador de energia e níveis mais baixos de ATP, a moeda energética da célula. Quando os animais foram tratados com altas doses de um hormônio sintético que imita estresse crônico, esses problemas se agravaram mais nos camundongos APOE4 do que nos APOE3. Ao mesmo tempo, uma proteína chamada tau — que normalmente ajuda a estabilizar os "trilhos" internos da célula — começou a se acumular, sofrer modificações excessivas, formar agregados e espalhar-se de neurônio para neurônio. Essas alterações em tau, frequentemente chamadas de patologia de tau, foram muito mais intensas e se espalharam mais em cérebros APOE4 expostos aos hormônios do estresse.
Sinalização de estresse hiperativa em cérebros vulneráveis
O estudo também examinou com que intensidade as células cerebrais respondiam aos sinais de estresse. Os glucocorticoides atuam por meio de receptores que normalmente ficam no citosol e se deslocam para o núcleo e as mitocôndrias quando ativados. Em camundongos APOE4, esses receptores já estavam mais ativos na linha de base e se translocavam mais prontamente para o núcleo e as mitocôndrias, embora os níveis gerais de hormônio no sangue fossem semelhantes aos dos animais APOE3. Em apoio a isso, animais e neurônios APOE4 mostraram níveis mais altos de proteínas auxiliares que promovem a ativação dos receptores, assim como padrões de expressão gênica consistentes com sinalização mais forte dos hormônios do estresse. Em cultura celular, doses muito baixas de hormônio do estresse que pouco afetavam neurônios APOE3 foram suficientes para danificar mitocôndrias e desencadear acúmulo e liberação de tau em neurônios APOE4, mostrando que esse contexto genético reduz o limiar para danos relacionados ao estresse.
Um poro crítico nas mitocôndrias e uma possível forma de intervenção
Aprofundando, os pesquisadores focaram no poro de transição de permeabilidade mitocondrial (mPTP), um canal que pode abrir na membrana interna mitocondrial. Quando esse poro se abre, as mitocôndrias perdem seu potencial elétrico, liberam moléculas reativas danosas e podem levar as células à disfunção. Em neurônios APOE4, mesmo uma exposição modesta ao hormônio do estresse foi suficiente para aumentar os níveis de ciclofilina D, um regulador chave do poro, e para desencadear a abertura do poro. Bloquear esse poro com dois fármacos diferentes — um que interfere diretamente com a ciclofilina D e outro que reduz a produção mitocondrial de oxidantes (mito-apocynin) — protegeu neurônios APOE4 da perda de energia, do excesso de espécies reativas e das alterações de tau.
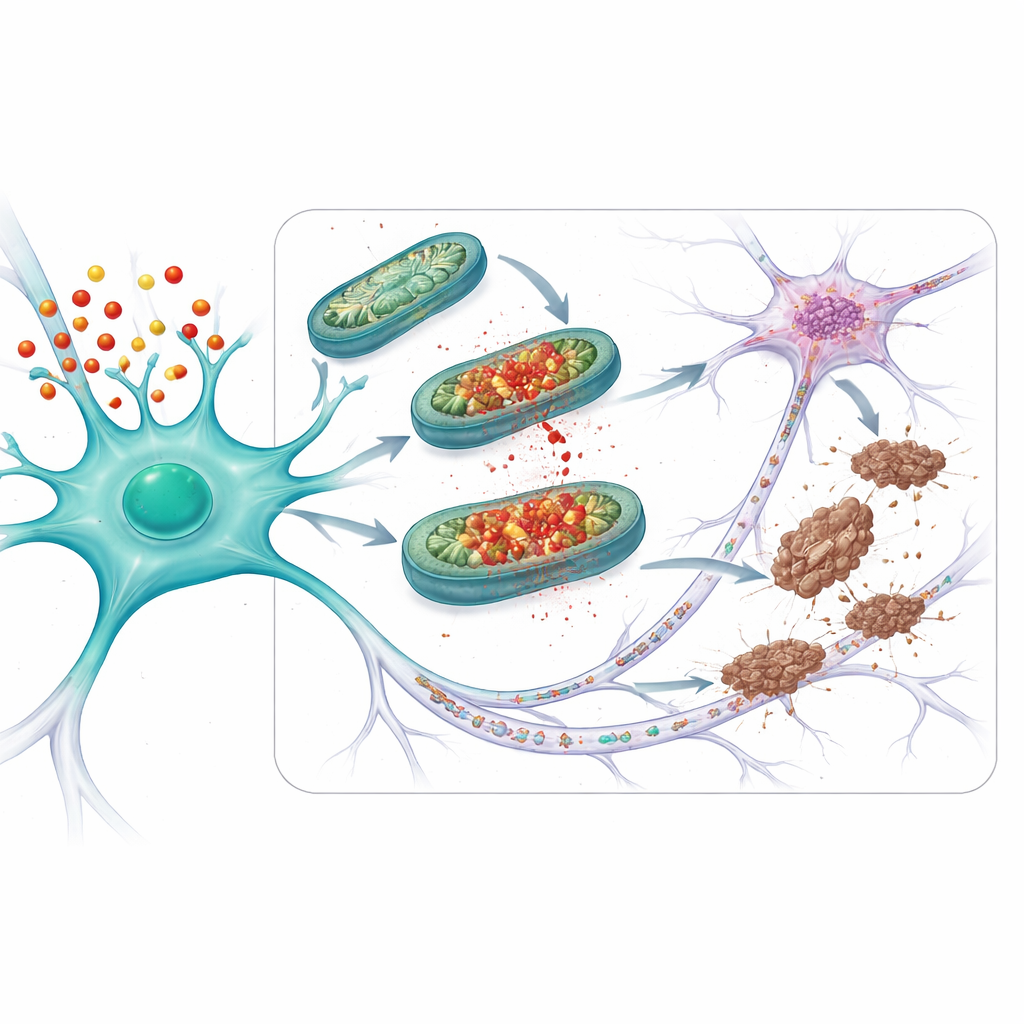
Protegendo conexões e cérebros em envelhecimento
Em seguida, a equipe perguntou se essa estratégia protetora ajudaria em contextos mais semelhantes à doença. Eles estudaram camundongos que não apenas carregavam o APOE4, mas também produziam uma forma mutante de tau que forma emaranhados com facilidade. Nesses animais, os problemas mitocondriais, o tau anômalo e a perda de sinapses — os pontos de conexão entre neurônios — foram todos piores do que em camundongos com a versão mais segura APOE3. Tratar camundongos APOE4 com mito-apocynin, começando antes do aparecimento de sintomas óbvios, reduziu o dano mitocondrial, as alterações de tau e a perda de sinapses. Em camundongos APOE4 mais velhos com surgimento natural de problemas de tau (mesmo sem tau mutante adicional), o tratamento curto com mito-apocynin também restaurou a função mitocondrial, reduziu tau anômalo e limitou a extensão da propagação do tau entre neurônios.
O que isso significa para pessoas em risco
Em termos simples, este trabalho sugere que o APOE4 torna as centrais de energia das células cerebrais mais frágeis e seus mecanismos de resposta ao estresse mais fáceis de ativar. Quando hormônios do estresse crônico se somam a isso, a combinação acelera a cascata que vai do dano mitocondrial ao acúmulo tóxico de tau, à sua propagação e à perda de conexões cerebrais. De forma crucial, o estudo mostra que bloquear um poro mitocondrial específico pode interromper essa cascata em modelos APOE4. Embora seja necessário muito mais trabalho antes que qualquer tratamento chegue aos pacientes, direcionar esse poro — e gerenciar o estresse crônico, especialmente em portadores de APOE4 — pode vir a fazer parte de estratégias futuras para retardar ou prevenir danos relacionados ao Alzheimer.
Citação: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Palavras-chave: APOE4, estresse crônico, mitocôndrias, patologia de tau, doença de Alzheimer