Clear Sky Science · de
APOE4 verschärft die durch Glukokortikoid-Stresshormone ausgelöste Tau-Pathologie über mitochondriale Dysfunktion
Warum Stress- und Gedächtnisgene uns alle betreffen
Viele Menschen sorgen sich, dass langanhaltende Stressphasen ihr Risiko erhöhen könnten, später im Leben Gedächtnisprobleme zu entwickeln. Gleichzeitig ist eine weit verbreitete Genvariante, APOE4, dafür bekannt, das Risiko für Alzheimer deutlich zu steigern. Diese Studie verknüpft diese beiden Themen: Sie fragt, wie Stresshormone und APOE4 innerhalb von Gehirnzellen zusammenwirken und ob diese Wechselwirkung mögliche Ansätze zum Schutz des alternden Gehirns aufzeigt.
Wie ein häufiges Risikogen auf alltäglichen Stress trifft
Die Forschenden konzentrierten sich auf APOE4, eine Variante eines Cholesterin-transportierenden Proteins, die von Millionen Menschen getragen wird. Sie kombinierten diesen genetischen Hintergrund mit der Exposition gegenüber Glukokortikoiden, den wichtigsten Stresshormonen, die bei chronischem psychischem Druck freigesetzt werden. An Mäusen, die so verändert wurden, dass sie menschliches APOE3 (die neutralere Variante) oder APOE4 tragen, sowie an Nervenzellen aus ihren Gehirnen, untersuchten sie den Hippocampus – eine Gedächtnisregion, die besonders empfindlich gegenüber Stress und Alzheimer ist. Ziel war es zu prüfen, ob APOE4 diese Neuronen anfälliger für die schädlichen Effekte von Stresshormonen macht.
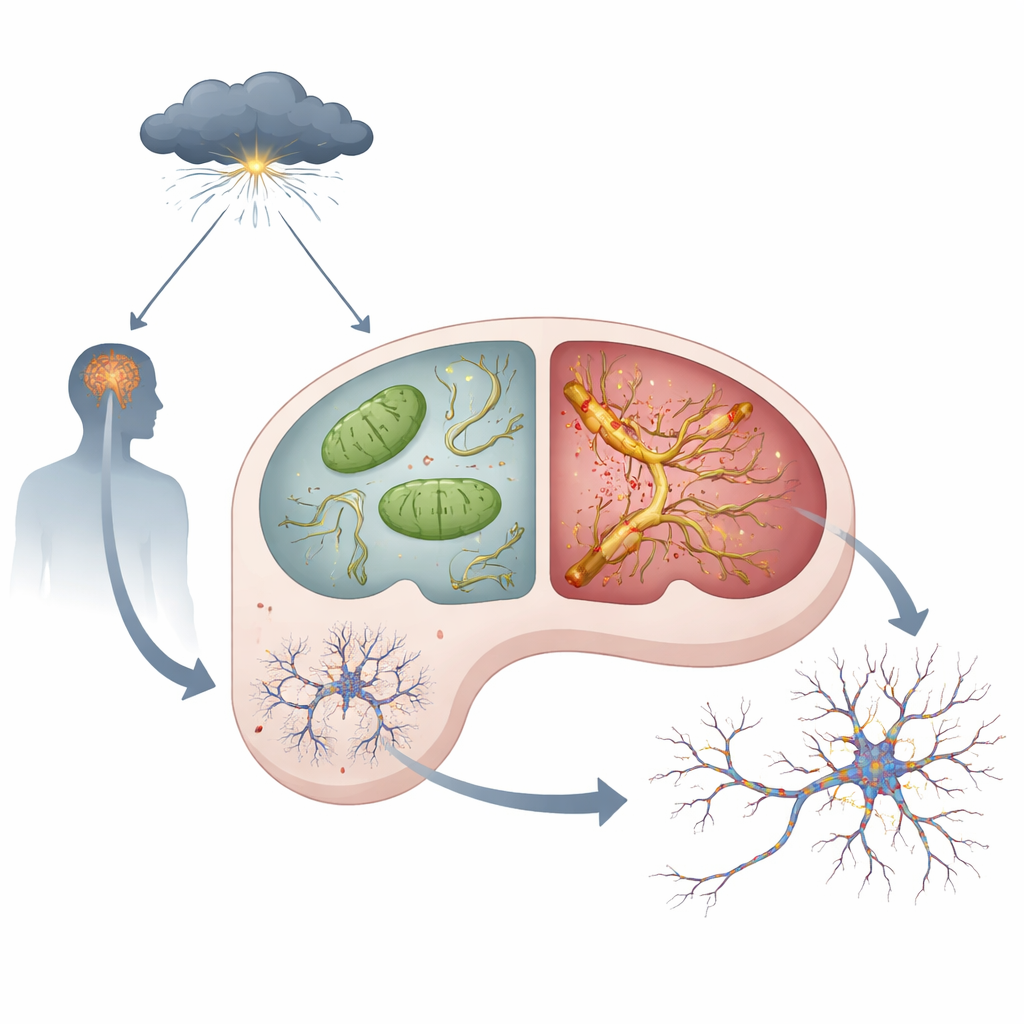
Stresshormone, fehlerhafte Kraftwerke und toxisches Tau
In jeder Nervenzelle sitzen Mitochondrien, winzige Kraftwerke, die die Energie für Denken und Erinnern erzeugen. Das Team fand heraus, dass APOE4-Mäuse bereits unter ruhigen Bedingungen Anzeichen mitochondrialer Probleme im Hippocampus zeigten: mehr reaktive Sauerstoffnebenprodukte, schwächere Aktivität eines wichtigen Energiebildungs-Komplexes und niedrigere ATP-Spiegel, die Energiewährung der Zelle. Wurden die Tiere mit hohen Dosen eines synthetischen Stresshormons behandelt, das chronischen Stress nachahmt, verschlechterten sich diese Probleme bei APOE4-Mäusen stärker als bei APOE3-Mäusen. Gleichzeitig begann ein Protein namens Tau – das normalerweise interne Zellschienen stabilisiert – sich anzureichern, übermäßig verändert zu werden, zu verklumpen und von Neuron zu Neuron zu verbreiten. Diese Tau-Veränderungen, oft Tau-Pathologie genannt, waren bei APOE4-Gehirnen, die Stresshormonen ausgesetzt waren, deutlich ausgeprägter und weiter verbreitet.
Überaktive Stresssignale in verwundbaren Gehirnen
Die Studie untersuchte außerdem, wie stark Gehirnzellen auf Stresssignale reagierten. Glukokortikoide wirken über Rezeptoren, die normalerweise in der Zellflüssigkeit sitzen und bei Aktivierung in den Zellkern und die Mitochondrien wandern. Bei APOE4-Mäusen waren diese Rezeptoren bereits im Ruhezustand stärker aktiv und verlagerten sich leichter in Kern und Mitochondrien, obwohl die Hormonniveaus im Blut insgesamt denen der APOE3-Tiere ähnelten. Unterstützend zeigte sich, dass APOE4-Tiere und -Neuronen höhere Pegel von Helferproteinen hatten, die Rezeptoraktivierung fördern, sowie Genexpressionsmuster, die auf stärkere Stresshormon-Signalisierung hinweisen. In Zellkulturen reichten sehr niedrige Dosen des Stresshormons, die bei APOE3-Neuronen kaum Wirkung zeigten, aus, um in APOE4-Neuronen Mitochondrien zu schädigen und Tau-Anreicherung sowie Freisetzung auszulösen – ein Hinweis darauf, dass dieser genetische Hintergrund die Schwelle für stressbedingten Schaden senkt.
Eine kritische Porenstruktur in Mitochondrien und ein möglicher Eingriff
Bei genauerer Untersuchung richteten die Forschenden den Fokus auf den mitochondrialen Permeabilitätsübergangspore (mPTP), einen Kanal, der in der inneren Mitochondrienmembran öffnen kann. Öffnet sich diese Pore, verlieren Mitochondrien ihre elektrische Ladung, pumpen schädliche reaktive Moleküle aus und können Zellen in Richtung Funktionsverlust treiben. In APOE4-Neuronen reichte selbst mäßige Stresshormonaussetzung, um die Spiegel von Cyclophilin D – einem Schlüsselregulator der Pore – zu erhöhen und die Pore zu öffnen. Das Blockieren dieser Pore mit zwei verschiedenen Medikamenten – einem, das direkt Cyclophilin D hemmt, und einem anderen, das die mitochondriale Oxidantienproduktion dämpft (mito-apocynin) – schützte APOE4-Neuronen vor Energieverlust, überschüssigen reaktiven Molekülen und Tau-Veränderungen.
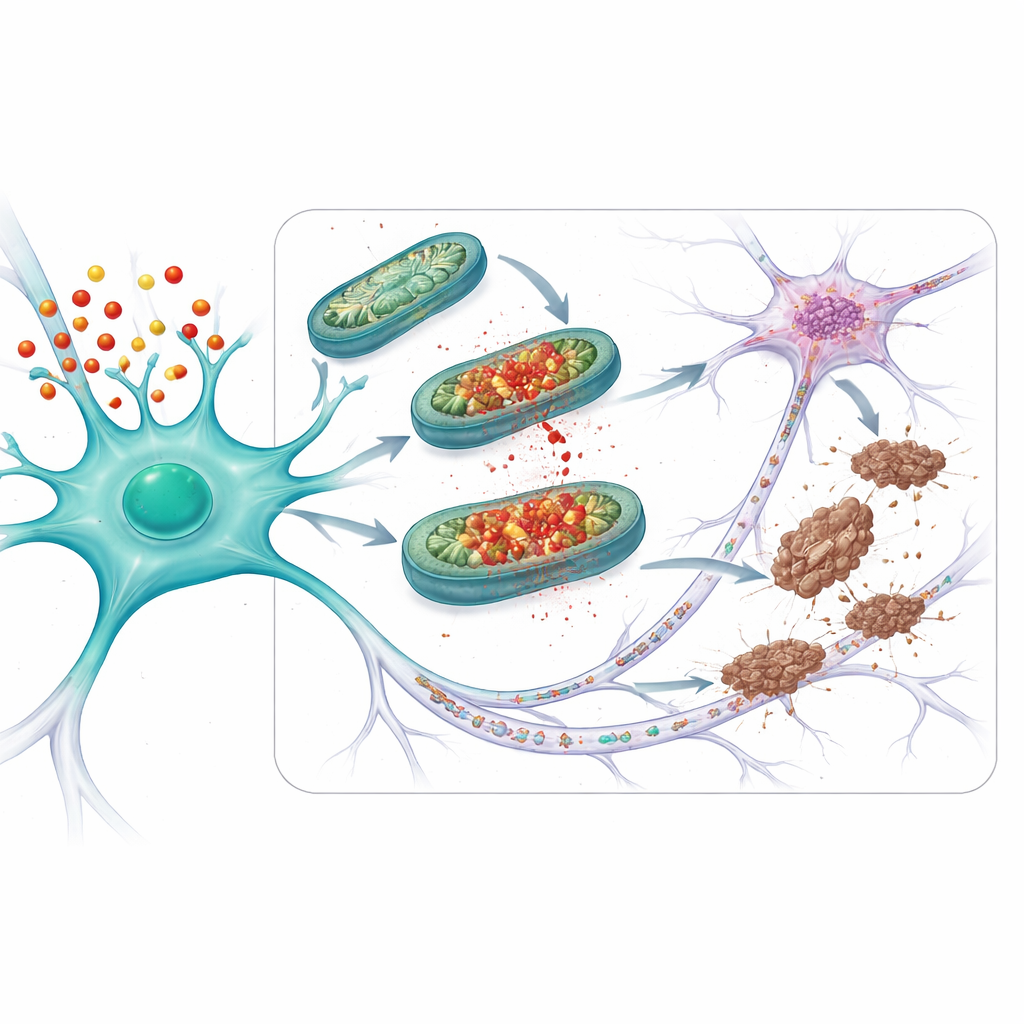
Schutz von Verbindungen und alternden Gehirnen
Das Team fragte dann, ob diese Schutzstrategie auch in stärker krankheitsähnlichen Situationen wirkt. Sie untersuchten Mäuse, die nicht nur APOE4 trugen, sondern auch eine mutierte Form von Tau produzierten, die leicht Tangles bildet. Bei diesen Tieren waren mitochondriale Probleme, abnormes Tau und Synapsenverlust – die Verbindungsstellen zwischen Neuronen – stärker ausgeprägt als bei Mäusen mit der harmloseren APOE3-Variante. Die Behandlung von APOE4-Mäusen mit mito-apocynin, beginnend bevor offensichtliche Symptome auftraten, verringerte mitochondriale Schäden, Tau-Veränderungen und Synapsenverlust. Bei älteren APOE4-Mäusen mit natürlicherweise auftretenden Tau-Problemen (auch ohne zusätzliches mutiertes Tau) stellte eine kurzzeitige Behandlung mit mito-apocynin ähnlich die mitochondriale Funktion wieder her, reduzierte abnormes Tau und begrenzte die Ausbreitung von Tau zwischen Neuronen.
Was das für Menschen mit Risiko bedeutet
Vereinfacht gesagt legt diese Arbeit nahe, dass APOE4 die Kraftwerke der Gehirnzellen fragiler und ihre Stress-Antwortschalter leichter umlegbar macht. Kommt chronischer Stress hinzu, beschleunigt diese Kombination die Kaskade vom mitochondrialen Schaden zur toxischen Tau-Anreicherung, -Ausbreitung und zum Verlust neuronaler Verbindungen. Entscheidenderweise zeigt die Studie, dass das Blockieren einer spezifischen mitochondrialen Pore diese Kaskade in APOE4-Modellen unterbrechen kann. Obwohl noch viel Arbeit nötig ist, bevor eine Behandlung Patienten erreicht, könnten das Anvisieren dieser Pore – und das Management chronischen Stresses, insbesondere bei APOE4-Trägern – Teil künftiger Strategien werden, um Alzheimer-ähnliche Schäden zu verlangsamen oder zu verhindern.
Zitation: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Schlüsselwörter: APOE4, chronischer Stress, Mitochondrien, Tau-Pathologie, Alzheimer-Krankheit