Clear Sky Science · sv
APOE4 förvärrar glukokortikoid-stresshormoninducerad tau-patologi via mitokondriell dysfunktion
Varför stress och minnesgener berör oss alla
Många oroar sig för att långvarig stress kan öka risken för minnesproblem senare i livet. Samtidigt är en vanlig genetisk variant kallad APOE4 känd för att kraftigt öka risken för Alzheimers sjukdom. Denna studie förenar dessa två trådar genom att undersöka hur stresshormoner och APOE4 samverkar i hjärnceller, och om den interaktionen kan peka på nya sätt att skydda den åldrande hjärnan.
Hur ett vanligt riskgen möter vardagsstress
Forskarlaget fokuserade på APOE4, en variant av ett kolesterolhanterande protein som bärs av miljontals människor världen över. De kombinerade denna genetiska bakgrund med exponering för glukokortikoider, de viktigaste stresshormonerna som frisätts vid kronisk psykisk påfrestning. Med hjälp av möss som konstruerats för att bära mänsklig APOE3 (den mer neutrala varianten) eller APOE4, och nervceller odlade från deras hjärnor, zoomade de in på hippocampus — en minnescentral som är särskilt känslig för både stress och Alzheimers. Målet var att se om APOE4 gör dessa neuroner mer mottagliga för stresshormonernas skadliga effekter.
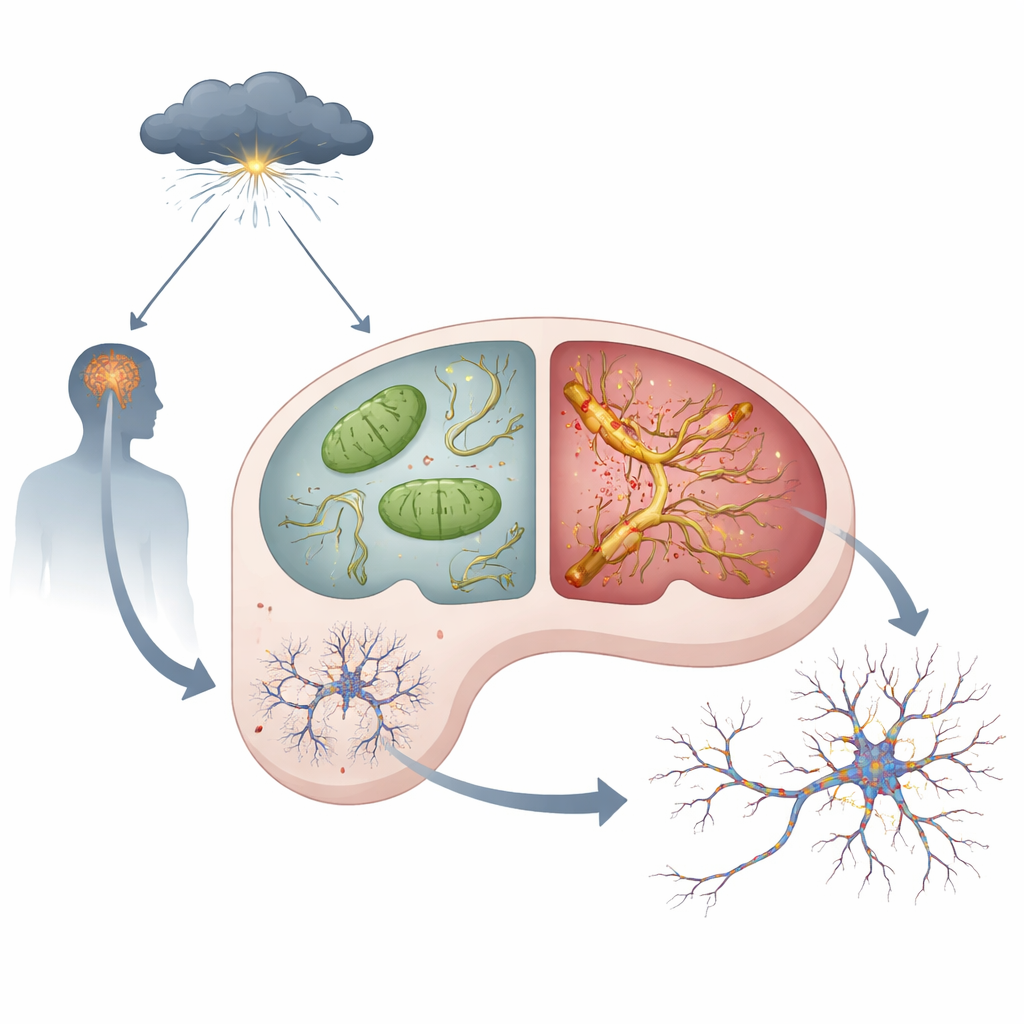
Stresshormoner, defekta kraftverk och toxisk tau
I varje neuron finns mitokondrier, små kraftverk som genererar energin som behövs för tänkande och minne. Teamet fann att även under lugna förhållanden visade APOE4-möss tecken på mitokondriella problem i hippocampus: fler reaktiva syreprodukter, svagare aktivitet i ett viktigt energi‑skapande komplex och lägre nivåer av ATP, cellens energivaluta. När djuren behandlades med höga doser av ett syntetiskt stresshormon som efterliknar kronisk stress förvärrades dessa problem mer hos APOE4-möss än hos APOE3-möss. Samtidigt började ett protein kallat tau — som normalt hjälper till att stabilisera cellens inre ”spår” — att ansamlas, modifieras överdrivet, klumpa sig och spridas från neuron till neuron. Dessa tau‑förändringar, ofta kallade tau‑patologi, var mycket starkare och spred sig längre i APOE4-hjärnor som exponerats för stresshormoner.
Överaktiv stressignalering i sårbara hjärnor
Studien undersökte också hur kraftigt hjärnceller svarade på stressignaler. Glukokortikoider verkar genom receptorer som normalt ligger i cellens cytoplasma och som vid aktivering förflyttar sig in i kärnan och mitokondrierna. I APOE4-möss var dessa receptorer redan mer aktiva i vila och förflyttade sig lättare in i kärnan och mitokondrierna, trots att de övergripande hormonnivåerna i blodet var liknande de hos APOE3-djur. Som stöd visade APOE4-djur och neuroner högre nivåer av hjälpproteiner som främjar receptoraktivering, och genuttrycksmönster som överensstämmer med starkare stresshormonssignalering. I cellkultur räckte mycket låga doser stresshormon som hade liten effekt på APOE3-neuroner för att skada mitokondrier och utlösa tau‑ansamling och utsöndring i APOE4-neuroner, vilket visar att denna genetiska bakgrund sänker tröskeln för stressrelaterad skada.
En kritisk por i mitokondrierna och en möjlig intervention
Genom att gå djupare identifierade forskarna den mitokondriella permeabilitetsövergångs‑poren (mPTP), en kanal som kan öppnas i det inre mitokondriemembranet. När denna pore öppnas förlorar mitokondrier sin elektriska laddning, pumpar ut skadliga reaktiva molekyler och kan driva celler mot dysfunktion. I APOE4-neuroner var även måttlig stresshormonexponering tillräcklig för att öka nivåerna av cyclophilin D, en nyckelregulator för poren, och för att utlösa pore‑öppning. Att blockera denna pore med två olika läkemedel — ett som direkt stör cyclophilin D och ett annat som dämpar mitokondriell oxidantproduktion (mito-apocynin) — skyddade APOE4-neuroner från energiförlust, överskott av reaktiva molekyler och tau‑förändringar.
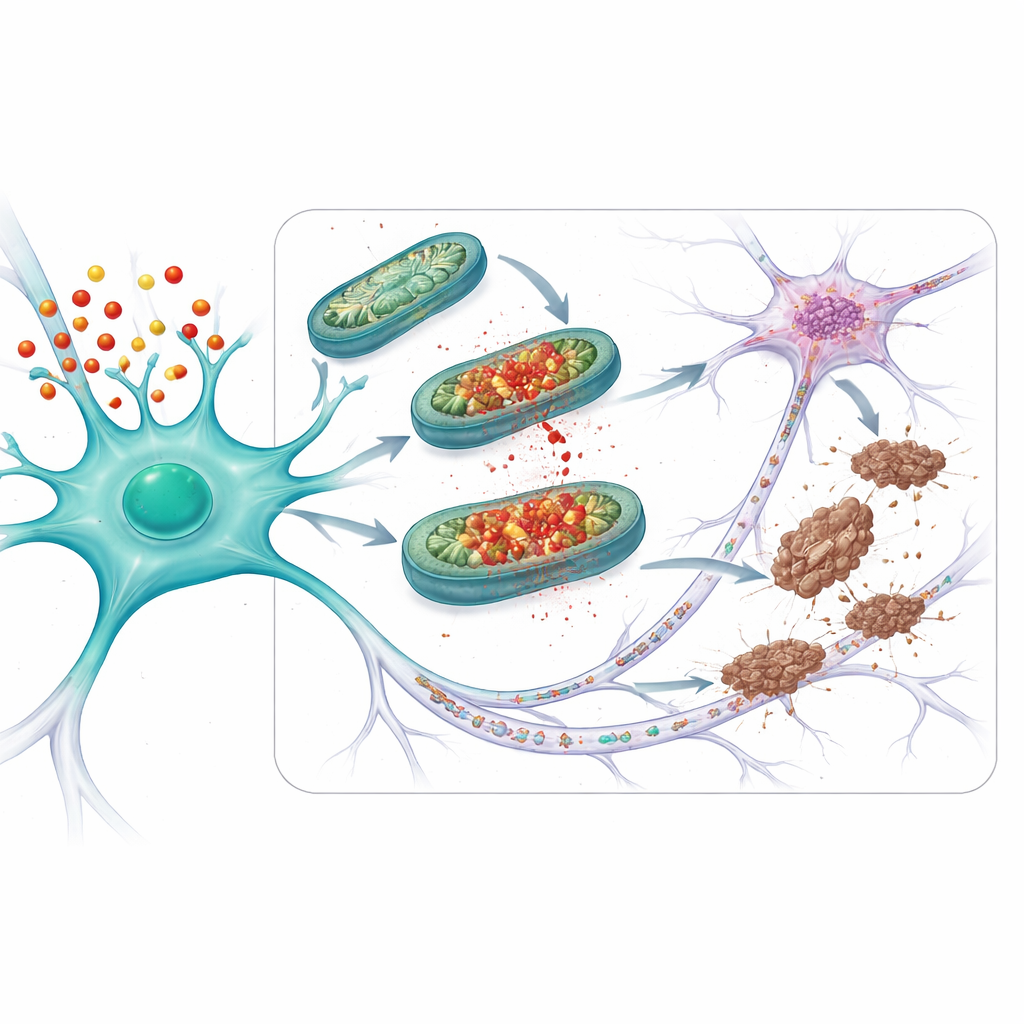
Skydda synapser och åldrande hjärnor
Teamet frågade sedan om denna skyddsstrategi skulle hjälpa i mer sjukdomsliknande miljöer. De studerade möss som inte bara bar APOE4 utan också producerade en mutant form av tau som lätt bildar trassel. I dessa djur var mitokondriella problem, abnorm tau och förlust av synapser — kontaktpunkterna mellan neuroner — alla värre än hos möss med den säkrare APOE3‑varianten. Behandling av APOE4‑möss med mito‑apocynin, med start innan uppenbara symptom uppstod, minskade mitokondriella skador, tau‑förändringar och synapsförlust. Hos äldre APOE4‑möss med naturligt uppkommande tau‑problem (även utan tillsatt mutant tau) återställde kortvarig mito‑apocyninbehandling på liknande sätt mitokondriell funktion, minskade abnorm tau och begränsade hur långt tau spreds mellan neuroner.
Vad detta betyder för personer i riskzonen
Enkelt uttryckt tyder arbetet på att APOE4 gör hjärncells kraftverk mer sköra och deras stressresponsswitchar lättare att slå på. När kroniska stresshormoner läggs till ovanpå detta accelererar kombinationen kaskaden från mitokondriell skada till toxisk tau‑ansamling, spridning och förlust av hjärnkopplingar. Viktigt är att studien visar att blockering av en specifik mitokondriell pore kan avbryta denna kaskad i APOE4‑modeller. Mycket mer forskning krävs innan någon behandling når patienter, men att rikta in sig på denna pore — och att hantera kronisk stress, särskilt hos APOE4‑bärare — kan bli en del av framtida strategier för att sakta eller förebygga Alzheimersrelaterad skada.
Citering: Yu, Q., Du, F., Puerta-Alvarado, V. et al. APOE4 exacerbates glucocorticoid stress hormone-induced tau pathology via mitochondrial dysfunction. Cell Death Dis 17, 419 (2026). https://doi.org/10.1038/s41419-026-08543-1
Nyckelord: APOE4, kronisk stress, mitokondrier, tau-patologi, Alzheimers sjukdom