Clear Sky Science · zh
ADAR2通过对IGFBP7的编辑活性诱导骨肉瘤细胞分化:对治疗的新启示
将一种危险的骨癌引向愈合
骨肉瘤是一种罕见但侵袭性强的骨癌,主要发生在儿童和青少年身上。尽管有外科手术和强效化疗,仍有太多年轻患者复发或出现肺转移。本研究探讨了一个新兴的想法:是否可以不仅仅通过杀死癌细胞,而是诱导它们“长大”并更像正常成骨细胞行事?研究者聚焦于一种天然的RNA编辑酶ADAR2,并揭示提升其活性如何推动骨肉瘤细胞走向更成熟、风险更低的状态。
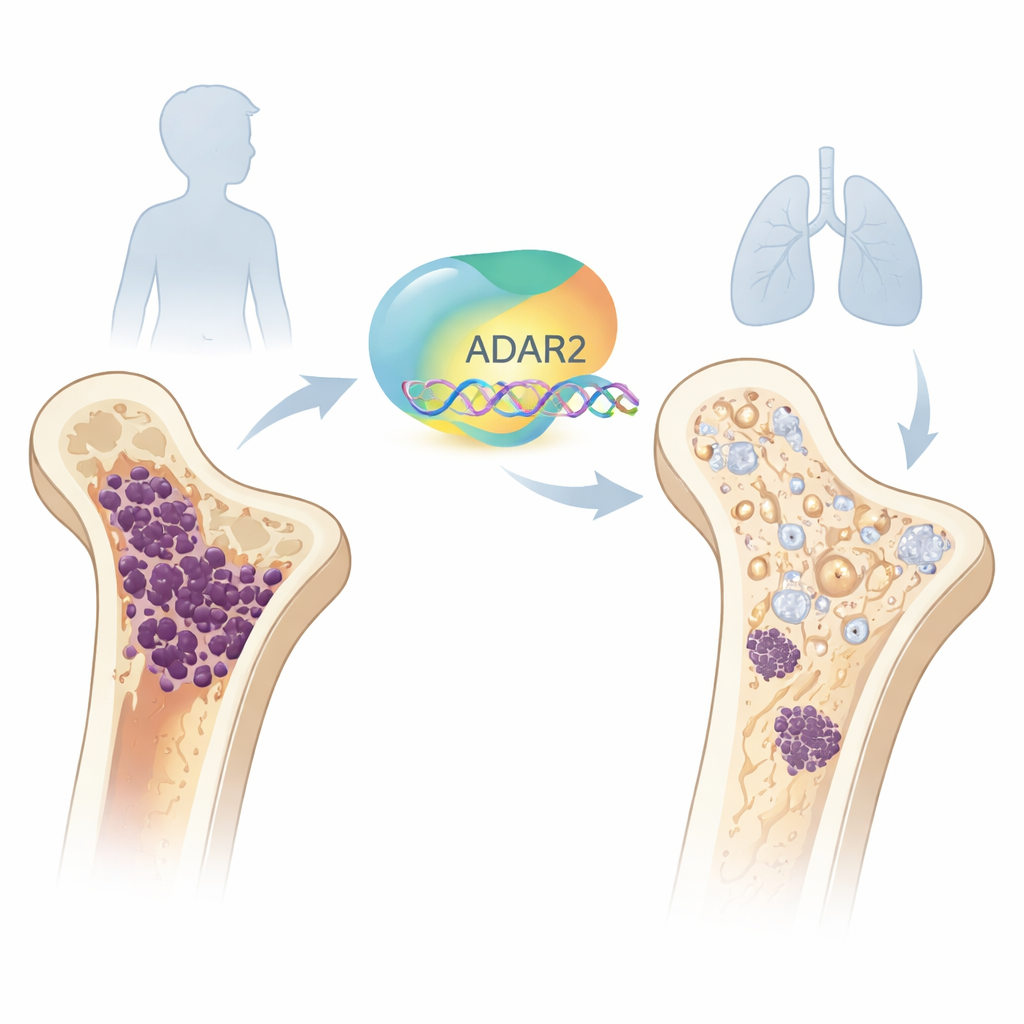
具有保护作用的分子编辑器
在每个细胞内,承载遗传信息的信使以RNA形式书写。ADAR2是体内的“编辑者”之一,能在这些信息写出后进行细微修改。团队首先观察正常的骨发育,发现ADAR2在骨髓来源的早期干细胞中水平很低,但随着这些细胞向成骨细胞分化时会上升。当他们在健康干细胞中人为提高ADAR2时,这些细胞启动了与成骨相关的基因并增强了形成矿化骨基质的能力。相反,在健康成骨细胞中降低ADAR2会削弱关键的骨标志物并减少其成骨活性,显示出ADAR2对正常成骨过程的重要性。
低ADAR2标志更具侵袭性的肿瘤
研究者随后转向骨肉瘤样本和细胞系。在患者数据集中,肿瘤组织的ADAR2远低于健康骨髓干细胞,且那些肿瘤中ADAR2特别低的患者预后更差、转移更多。在一个小鼠模型中,骨肉瘤细胞从骨部位扩散到肺时,迁移的细胞其ADAR2水平也明显低于留在骨中的细胞。总体而言,这些发现表明丧失这一分子编辑器与更具侵袭性的疾病和更差的临床结局相关。
强迫癌细胞“长大”
为测试恢复ADAR2是否能驯服骨肉瘤,团队对两种人源骨肉瘤细胞系进行了工程改造,使其过量表达活性ADAR2、失活突变体或对照。表达活性ADAR2的细胞分裂更慢,在细胞周期的静止期停留更久,侵袭周围组织的能力也较弱。在具备部分类骨行为的一个细胞系中,活性ADAR2显著增强了矿化小结节的生成并激活了与完全成熟成骨细胞相关的基因,同时降低了与干性和恶性相关的标志物。重要的是,当这些工程化细胞被植入免疫缺陷小鼠的腿骨时,过表达ADAR2的细胞所形成的肿瘤更小、侵袭性更低,小鼠出现的肝肺转移更少。失活突变体未能提供这种保护,表明ADAR2的编辑活性至关重要。
编辑癌细胞中的生长开关
为揭示ADAR2如何发挥作用,团队使用RNA测序同时绘制了基因表达变化和编辑事件。他们发现数百个基因的变化符合恶性程度降低和骨分化改善。最引人注目的是,ADAR2大量编辑了名为IGFBP7的基因,该基因编码的一种蛋白可通过IGF1受体增强生长信号——这一通路已知能促进肿瘤细胞生存和增殖。ADAR2在IGFBP7中将单个氨基酸转换,产生稍有差异的蛋白变体。在骨肉瘤细胞中,这种被编辑的形式与IGF1信号通路激活减弱以及下游生长驱动因子活性降低相关。当细胞处理未编辑的IGFBP7蛋白时,生长通路被激活,细胞增殖加快,而一关键的成骨转录因子下降。相反,被编辑的形式未能刺激生长,反而增强了该成骨相关因子,倾向于推动分化而非分裂。
将治疗重新定位为重编程
从本质上讲,这项工作揭示了ADAR2在骨肉瘤中作为天然肿瘤抑制因子的角色,其机制是通过重写特定的RNA信息,尤其是IGFBP7的讯息。提升ADAR2引导恶性成骨细胞远离失控生长,走向终末的类骨分化,同时也使其对现有化疗药物更为敏感。对患者而言,长期的希望是开发一类新的“分化疗法”,通过重编程而非单纯摧毁癌细胞——有望在这一急需更好治疗方案的儿童癌症中改善预后。
引用: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
关键词: 骨肉瘤, RNA编辑, ADAR2, 骨分化, IGFBP7