Clear Sky Science · pt
ADAR2 induz a diferenciação de células de osteossarcoma por atividade de edição em IGFBP7: novas implicações para a terapia
Transformando um Câncer Ósseo Perigoso em Cura
O osteossarcoma é um câncer raro, porém agressivo, dos ossos que atinge principalmente crianças e adolescentes. Apesar de cirurgia e quimioterapia intensiva, muitos pacientes jovens ainda recidivam ou desenvolvem metástases pulmonares. Este estudo explora uma ideia emergente: em vez de apenas tentar matar as células cancerosas, seria possível induzi-las a amadurecer e comportar-se mais como células normais formadoras de osso? Os pesquisadores concentram-se numa enzima natural de edição de RNA chamada ADAR2 e revelam como aumentar sua atividade pode empurrar células de osteossarcoma para um estado mais maduro e menos perigoso.
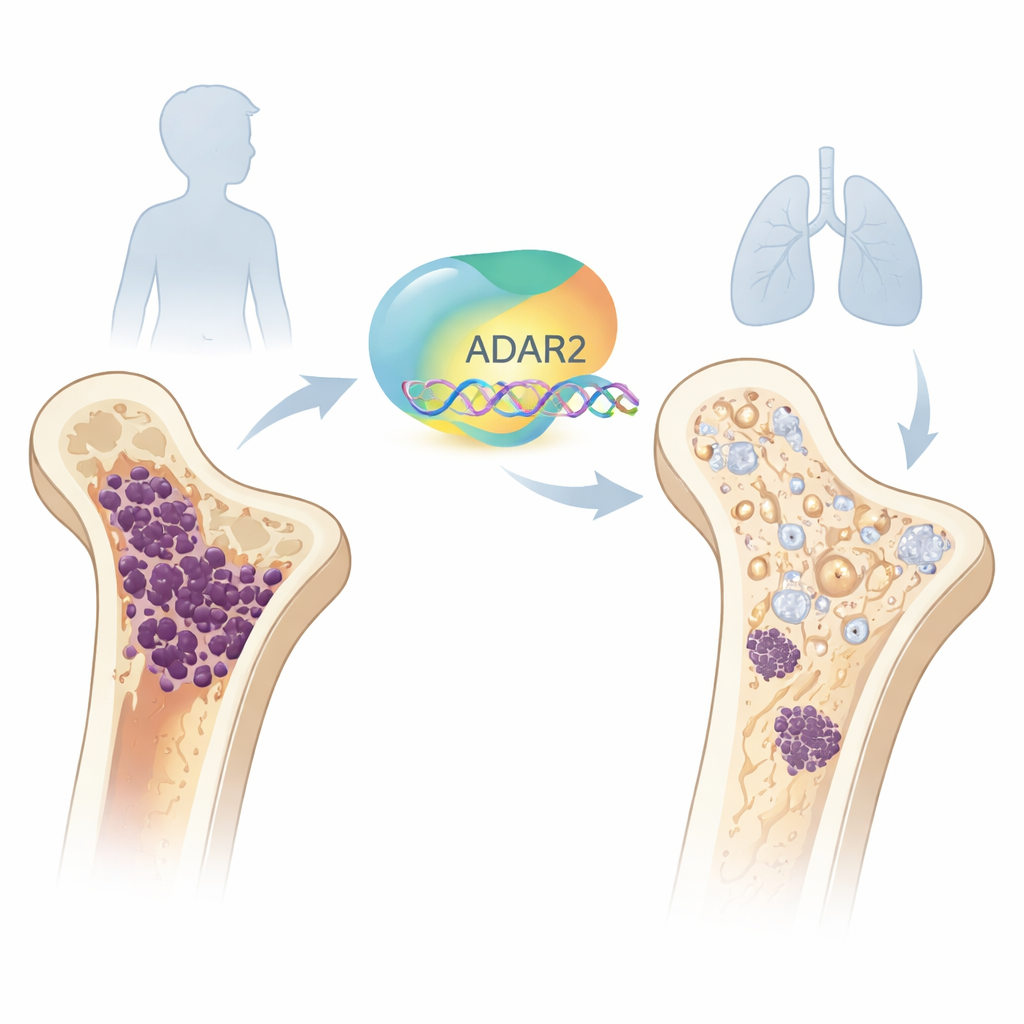
Um Editor Molecular com um Lado Protetor
Dentro de cada célula, as mensagens que carregam informação genética são escritas em RNA. ADAR2 é um dos “editores” do organismo que pode alterar sutilmente essas mensagens depois de escritas. A equipe primeiro examinou o desenvolvimento ósseo normal e constatou que os níveis de ADAR2 são baixos em células-tronco da medula óssea em estágios iniciais, mas aumentam à medida que essas células amadurecem em osteoblastos, as células que constroem o osso. Quando aumentaram artificialmente o ADAR2 em células-tronco saudáveis, essas células ativaram genes relacionados ao osso e ampliaram sua capacidade de formar matriz óssea mineralizada. Por outro lado, reduzir o ADAR2 em osteoblastos saudáveis enfraqueceu marcadores ósseos essenciais e diminuiu sua atividade formadora de osso, mostrando que ADAR2 é importante para a construção óssea normal.
Baixo ADAR2 Marca Tumores Mais Agressivos
Os pesquisadores então voltaram-se para amostras de osteossarcoma e linhas celulares. Em conjuntos de dados de pacientes, os tumores apresentaram muito menos ADAR2 do que as células-tronco da medula óssea saudável, e pacientes cujos tumores exibiam níveis particularmente baixos de ADAR2 tiveram pior sobrevida e mais metástases. Num modelo murino em que células de osteossarcoma migraram do osso para o pulmão, as células migrantes também mostraram níveis marcadamente mais baixos de ADAR2 do que as que permaneciam no osso. Em conjunto, esses achados sugerem que a perda desse editor molecular está ligada a um comportamento tumoral mais agressivo e a piores desfechos clínicos.
Forçando as Células Cancerígenas a Maturarem
Para testar se restaurar o ADAR2 poderia controlar o osteossarcoma, a equipe alterou geneticamente duas linhas celulares humanas de osteossarcoma para superproduzir ADAR2 ativo, uma versão mutante inativa ou um controle. As células com ADAR2 ativo dividiram-se mais lentamente, permaneceram por mais tempo em uma fase de repouso do ciclo celular e invadiram menos o tecido ao redor. Em uma linha celular com capacidade parcial de comportamento ósseo, o ADAR2 ativo aumentou fortemente a produção de nódulos mineralizados e ativou genes associados a osteócitos plenamente maduros, ao mesmo tempo em que reduziu marcadores ligados à imaturidade e malignidade. Importante: quando essas células modificadas foram implantadas nos ossos das patas de camundongos imunodeficientes, os tumores formados por células com superexpressão de ADAR2 foram menores e menos invasivos, e os animais desenvolveram menos metástases no fígado e nos pulmões. A versão mutante inativa não ofereceu essa proteção, indicando que a atividade de edição do ADAR2 é crucial.
Editando um Interruptor de Crescimento nas Células Cancerosas
Para descobrir como o ADAR2 produz esses efeitos, a equipe usou sequenciamento de RNA para mapear tanto mudanças na expressão gênica quanto eventos de edição. Eles encontraram centenas de genes alterados de maneiras compatíveis com menor malignidade e melhor especialização óssea. O achado mais notável foi que o ADAR2 editou intensamente um gene chamado IGFBP7, que codifica uma proteína capaz de amplificar sinais de crescimento através do receptor IGF1, uma via conhecida por promover a sobrevivência e proliferação de células tumorais. O ADAR2 converteu um único aminoácido dentro do IGFBP7, produzindo uma variante proteica levemente diferente. Em células de osteossarcoma, essa forma editada esteve associada a uma ativação mais fraca da cadeia de sinalização do IGF1 e a menor atividade de motores de crescimento a jusante. Quando as células foram tratadas com a proteína IGFBP7 não editada, as vias de crescimento foram ativadas, as células proliferaram mais rápido e um fator de transcrição ósseo importante diminuiu. Em contraste, a forma editada não estimulou o crescimento; em vez disso, aumentou o fator relacionado ao osso e favoreceu a diferenciação em vez da divisão.
Reenquadrando a Terapia como Reprogramação
Em essência, este trabalho revela o ADAR2 como um supressor tumoral natural no osteossarcoma que atua reescrevendo mensagens específicas de RNA, especialmente as de IGFBP7. Aumentar o ADAR2 direciona células ósseas malignas para longe do crescimento descontrolado e em direção à diferenciação terminal semelhante ao osso, além de torná-las mais sensíveis a quimioterápicos existentes. Para os pacientes, a esperança de longo prazo é uma nova classe de “terapias de diferenciação” que reprogramem, em vez de simplesmente destruir, as células cancerosas—potencialmente melhorando os desfechos em um câncer pediátrico onde opções melhores são urgentemente necessárias.
Citação: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
Palavras-chave: osteossarcoma, edição de RNA, ADAR2, diferenciação óssea, IGFBP7