Clear Sky Science · it
ADAR2 induce la differenziazione delle cellule di osteosarcoma tramite attività di editing su IGFBP7: nuove implicazioni terapeutiche
Convertire un tumore osseo pericoloso verso la guarigione
L'osteosarcoma è un tumore osseo raro ma aggressivo che colpisce soprattutto bambini e adolescenti. Nonostante interventi chirurgici e chemioterapie potenti, troppi giovani pazienti vanno incontro a recidive o sviluppano metastasi polmonari. Questo studio esplora un'idea emergente: invece di limitarsi a eliminare le cellule tumorali, è possibile indurle a maturare e comportarsi più come le normali cellule che formano l'osso? I ricercatori si concentrano su un enzima naturale di editing dell'RNA chiamato ADAR2 e descrivono come aumentare la sua attività possa spingere le cellule di osteosarcoma verso uno stato più maturo e meno pericoloso.
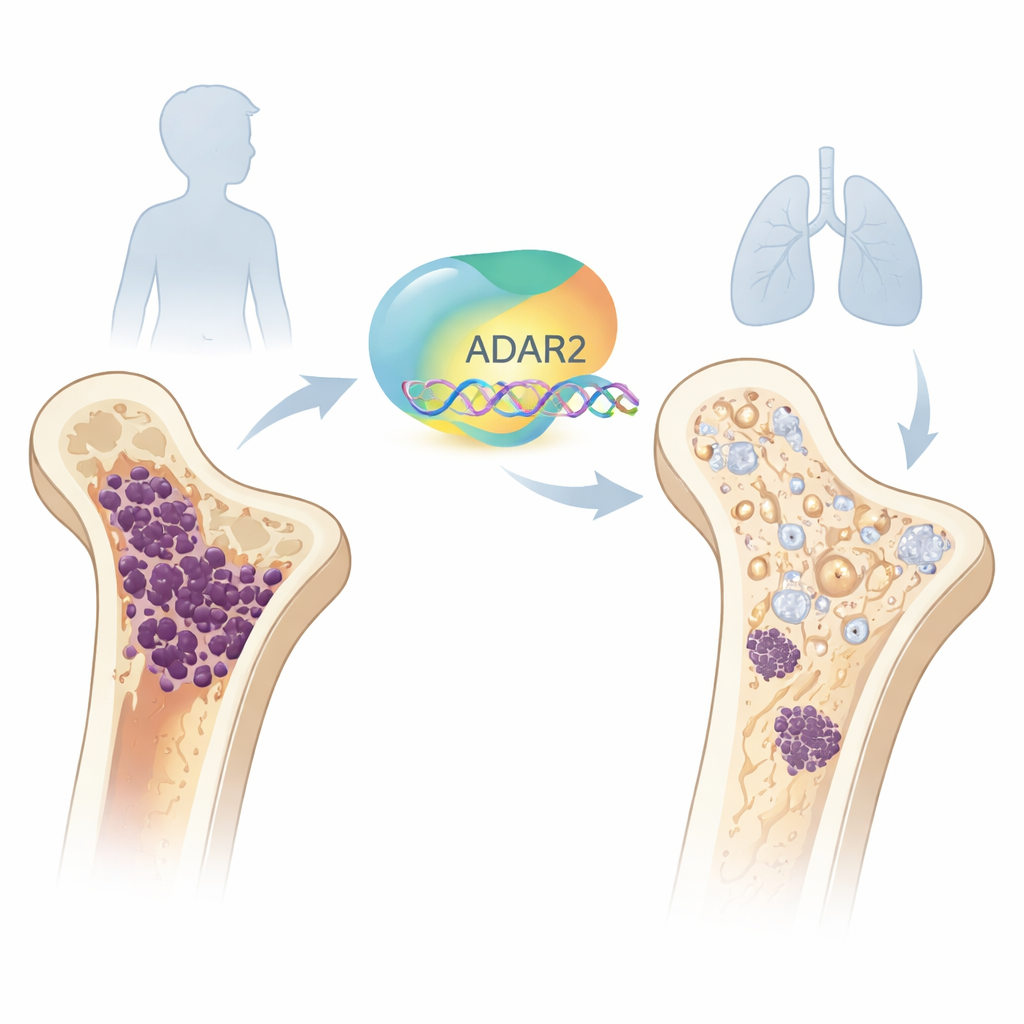
Un editore molecolare con una funzione protettiva
All'interno di ogni cellula, i messaggi che trasportano l'informazione genetica sono scritti in RNA. ADAR2 è uno degli “editor” dell'organismo che può modificare sottilmente questi messaggi dopo la loro scrittura. Il gruppo ha prima esaminato lo sviluppo osseo normale e ha rilevato che i livelli di ADAR2 sono bassi nelle cellule staminali del midollo osseo in fase iniziale, ma aumentano man mano che queste cellule maturano in osteoblasti, le cellule che costruiscono l'osso. Quando hanno aumentato artificialmente ADAR2 in cellule staminali sane, queste hanno attivato geni correlati all'osso e migliorato la loro capacità di formare matrice ossea mineralizzata. Al contrario, ridurre ADAR2 in osteoblasti sani ha indebolito marcatori ossei chiave e diminuito l'attività di formazione ossea, mostrando che ADAR2 è importante per la normale costruzione dell'osso.
Bassi livelli di ADAR2 caratterizzano tumori più aggressivi
I ricercatori si sono poi focalizzati su campioni e linee cellulari di osteosarcoma. Nei dataset dei pazienti, i tumori presentavano molto meno ADAR2 rispetto alle cellule staminali del midollo osseo sano, e i pazienti i cui tumori mostravano livelli particolarmente bassi di ADAR2 avevano una sopravvivenza peggiore e più metastasi. In un modello murino in cui le cellule di osteosarcoma migrano dall'osso al polmone, le cellule migranti mostravano livelli di ADAR2 marcatamente più bassi rispetto a quelle rimaste nell'osso. Nel loro insieme, questi risultati suggeriscono che la perdita di questo editor molecolare è associata a una malattia più aggressiva e a esiti clinici peggiori.
Costringere le cellule tumorali a crescere
Per verificare se il ripristino di ADAR2 potesse contenere l'osteosarcoma, il team ha ingegnerizzato due linee cellulari umane di osteosarcoma in modo che sovraesprimessero ADAR2 attivo, una versione mutante inattiva o un controllo. Le cellule con ADAR2 attivo si dividevano più lentamente, restavano più a lungo in una fase quiescente del ciclo cellulare e invadevano meno i tessuti circostanti. In una linea cellulare capace di un comportamento parzialmente simile all'osso, ADAR2 attivo ha aumentato fortemente la produzione di noduli mineralizzati e ha attivato geni associati a cellule ossee completamente mature, riducendo allo stesso tempo marcatori legati alla staminalità e alla malignità. Importante, quando queste cellule ingegnerizzate sono state impiantate nelle ossa delle zampe di topi immunodeficienti, i tumori formati dalle cellule che sovraesprimevano ADAR2 erano più piccoli e meno invasivi, e i topi sviluppavano meno metastasi epatiche e polmonari. La mutante inattiva non ha fornito questa protezione, indicando che l'attività di editing di ADAR2 è cruciale.
Editing di un interruttore di crescita nelle cellule tumorali
Per scoprire come ADAR2 eserciti questi effetti, il team ha utilizzato il sequenziamento dell'RNA per mappare sia i cambiamenti nell'espressione genica sia gli eventi di editing. Hanno trovato centinaia di geni alterati in modi coerenti con una ridotta malignità e una migliore specializzazione ossea. Più sorprendente, ADAR2 editava intensamente un gene chiamato IGFBP7, che codifica una proteina in grado di potenziare i segnali di crescita attraverso il recettore IGF1, una via nota per promuovere la sopravvivenza e la proliferazione delle cellule tumorali. ADAR2 ha convertito un singolo amminoacido in IGFBP7, producendo una variante proteica leggermente diversa. Nelle cellule di osteosarcoma, questa forma editata era associata a una minore attivazione della via di segnalazione IGF1 e a una ridotta attività dei fattori di crescita a valle. Quando le cellule venivano trattate con la proteina IGFBP7 non editata, le vie di crescita si accendevano, le cellule proliferavano più rapidamente e un fattore di trascrizione chiave per l'osso diminuiva. Al contrario, la forma editata non stimolava la crescita, favoriva invece il fattore legato all'osso e promuoveva la differenziazione rispetto alla divisione.
Riconsiderare la terapia come riprogrammazione
In sostanza, questo lavoro identifica ADAR2 come un soppressore tumorale naturale nell'osteosarcoma che agisce riscrivendo specifici messaggi di RNA, in particolare quelli per IGFBP7. Potenziare ADAR2 indirizza le cellule ossee maligne lontano dalla crescita incontrollata e verso una differenziazione terminale simile all'osso, rendendole al contempo più sensibili ai farmaci chemioterapici esistenti. Per i pazienti, la speranza a lungo termine è una nuova classe di “terapie della differenziazione” che riprogrammino, anziché semplicemente distruggere, le cellule tumorali — migliorando potenzialmente gli esiti in un tumore infantile per il quale sono urgentemente necessarie opzioni migliori.
Citazione: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
Parole chiave: osteosarcoma, editing dell'RNA, ADAR2, differenziazione ossea, IGFBP7