Clear Sky Science · es
ADAR2 induce la diferenciación de células de osteosarcoma mediante su actividad de edición sobre IGFBP7: nuevas implicaciones para la terapia
Orientar un cáncer óseo peligroso hacia la curación
El osteosarcoma es un cáncer óseo raro pero agresivo que afecta principalmente a niños y adolescentes. A pesar de la cirugía y quimioterapias intensas, demasiados pacientes jóvenes recidivan o desarrollan metástasis pulmonares. Este estudio explora una idea emergente: en lugar de limitarse a intentar matar las células tumorales, ¿se puede inducir que maduren y se comporten más como las células normales formadoras de hueso? Los investigadores se centran en una enzima natural de edición de ARN llamada ADAR2 y descubren cómo potenciar su actividad puede empujar a las células de osteosarcoma hacia un estado más maduro y menos peligroso.
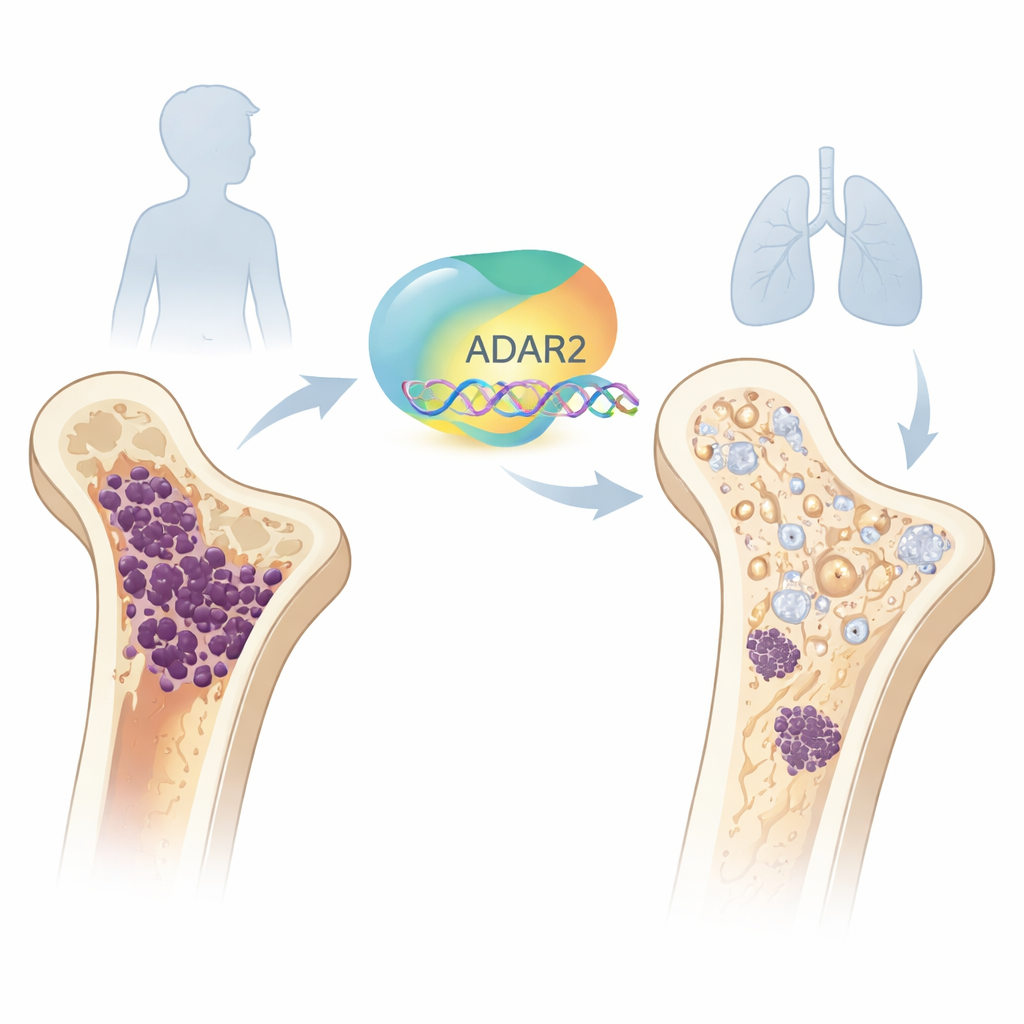
Un editor molecular con un papel protector
Dentro de cada célula, los mensajes que portan la información genética están escritos en ARN. ADAR2 es uno de los “editores” del organismo que puede cambiar sutilmente esos mensajes después de ser escritos. El equipo estudió primero el desarrollo óseo normal y observó que los niveles de ADAR2 son bajos en las células madre de la médula ósea en estado temprano, pero aumentan conforme esas células maduran en osteoblastos, las células que construyen el hueso. Cuando aumentaron artificialmente ADAR2 en células madre sanas, estas activaron genes relacionados con el hueso y mejoraron su capacidad para formar matriz mineralizada. A la inversa, reducir ADAR2 en osteoblastos sanos debilitó marcadores óseos clave y disminuyó su actividad formadora de hueso, lo que demuestra que ADAR2 es importante para la formación ósea normal.
Bajos niveles de ADAR2 señalan tumores más agresivos
Los investigadores a continuación analizaron muestras y líneas celulares de osteosarcoma. En diversos conjuntos de datos de pacientes, los tumores presentaban mucho menos ADAR2 que las células madre de médula ósea sanas, y los pacientes cuyos tumores mostraban niveles particularmente bajos de ADAR2 tuvieron peor supervivencia y más metástasis. En un modelo murino en el que células de osteosarcoma se diseminan del hueso al pulmón, las células migrantes también mostraron niveles de ADAR2 notablemente más bajos que las que permanecían en el hueso. En conjunto, estos hallazgos sugieren que la pérdida de este editor molecular se asocia con una enfermedad más agresiva y peores resultados clínicos.
Forzar a las células cancerosas a madurar
Para comprobar si restaurar ADAR2 podía domar el osteosarcoma, el equipo modificó genéticamente dos líneas celulares humanas de osteosarcoma para sobreproducir ADAR2 activo, una versión mutante inactiva o un control. Las células con ADAR2 activo se dividieron más lentamente, pasaron más tiempo en una fase de reposo del ciclo celular e invadieron menos los tejidos circundantes. En una línea celular capaz de un comportamiento parcialmente similar al óseo, ADAR2 activo aumentó de forma marcada la producción de nódulos mineralizados y activó genes asociados con osteocitos completamente maduros, mientras reducía marcadores vinculados a la pluripotencia y la malignidad. De forma importante, cuando estas células modificadas fueron implantadas en los huesos de las patas de ratones inmunodeficientes, los tumores formados por células que sobreexpresaban ADAR2 fueron más pequeños y menos invasivos, y los ratones desarrollaron menos metástasis en hígado y pulmón. La mutante inactiva no ofreció esa protección, lo que indica que la actividad de edición de ADAR2 es crucial.
Editar un interruptor de crecimiento en las células cancerosas
Para desentrañar cómo ADAR2 produce estos efectos, el equipo empleó secuenciación de ARN para cartografiar tanto los cambios en la expresión génica como los eventos de edición. Encontraron cientos de genes alterados de forma coherente con una menor malignidad y una mejor especialización ósea. Lo más llamativo fue que ADAR2 editó intensamente un gen llamado IGFBP7, que codifica una proteína capaz de potenciar las señales de crecimiento a través del receptor IGF1, una vía conocida por favorecer la supervivencia y proliferación de las células tumorales. ADAR2 convirtió un único aminoácido en IGFBP7, produciendo una variante proteica ligeramente distinta. En las células de osteosarcoma, esta forma editada se asoció con una activación más débil de la vía de señalización IGF1 y con menor actividad de impulsores de crecimiento downstream. Cuando las células fueron tratadas con la proteína IGFBP7 no editada, las vías de crecimiento se activaron, las células proliferaron más rápido y un factor de transcripción clave para el hueso disminuyó. En cambio, la forma editada no estimuló el crecimiento; por el contrario, potenció el factor relacionado con el hueso y favoreció la diferenciación frente a la división.
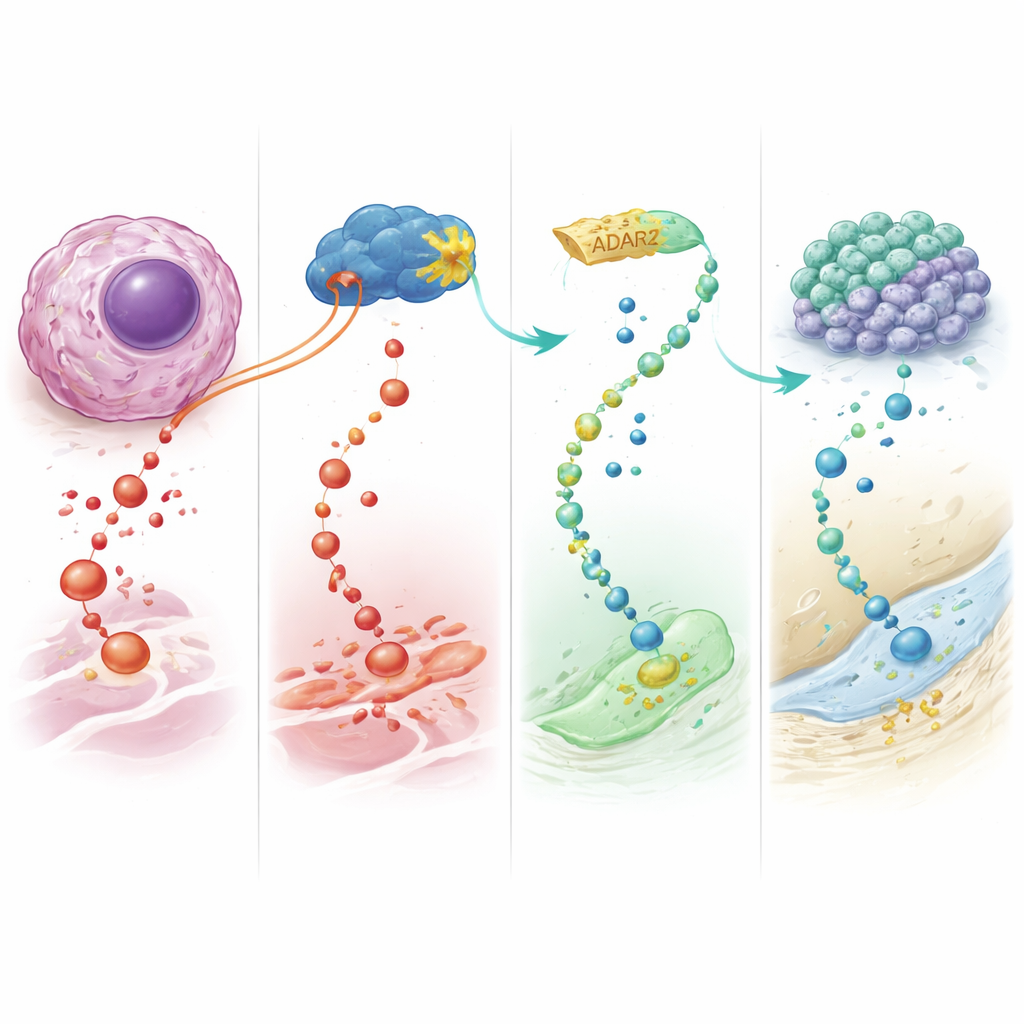
Replantear la terapia como reprogramación
En esencia, este trabajo revela a ADAR2 como un supresor tumoral natural en osteosarcoma que actúa reescribiendo mensajes de ARN específicos, especialmente los de IGFBP7. Potenciar ADAR2 dirige a las células óseas malignas lejos del crecimiento descontrolado y hacia una diferenciación terminal similar al hueso, al tiempo que las hace más sensibles a fármacos quimioterápicos existentes. Para los pacientes, la esperanza a largo plazo es una nueva clase de “terapias de diferenciación” que reprogramen, en lugar de simplemente destruir, las células cancerosas—mejorando potencialmente los resultados en un cáncer infantil donde se necesitan con urgencia mejores opciones.
Cita: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
Palabras clave: osteosarcoma, edición de ARN, ADAR2, diferenciación ósea, IGFBP7