Clear Sky Science · de
ADAR2 induziert die Differenzierung von Osteosarkomzellen durch Editieraktivität an IGFBP7: neue therapeutische Implikationen
Ein gefährlichen Knochenkrebs in Richtung Heilung lenken
Osteosarkom ist ein seltener, aber aggressiver Knochentumor, der vor allem Kinder und Jugendliche trifft. Trotz Operation und intensiver Chemotherapie fallen immer noch zu viele junge Patientinnen und Patienten Rückfällen zum Opfer oder entwickeln Lungenmetastasen. Diese Studie beleuchtet eine aufkommende Idee: Statt nur zu versuchen, Krebszellen zu töten, kann man sie vielleicht dazu bringen, sich zu „verabschieden“ und sich mehr wie normale, knochenbildende Zellen zu verhalten? Die Forschenden konzentrieren sich auf ein natürliches RNA‑Editierenzym namens ADAR2 und zeigen, wie die Steigerung seiner Aktivität Osteosarkomzellen in einen reiferen, weniger gefährlichen Zustand treiben kann.
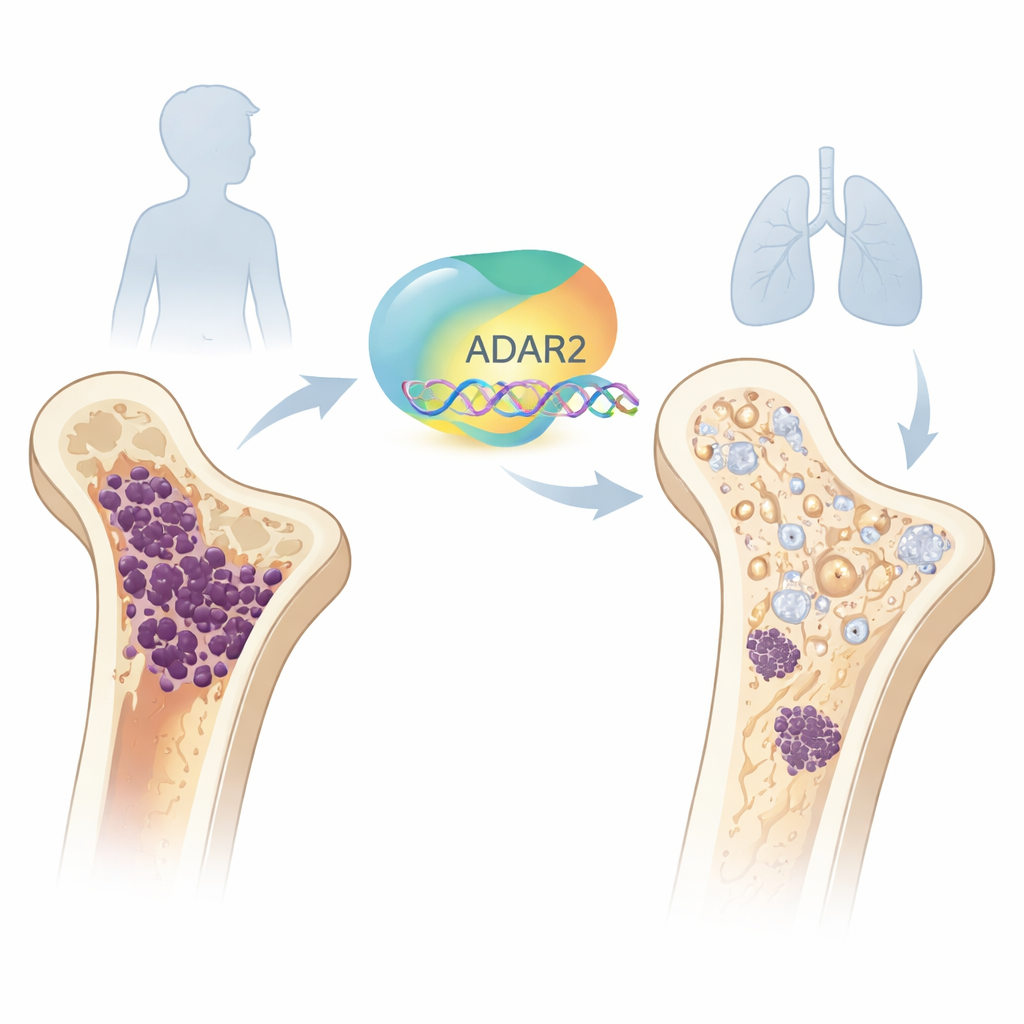
Ein molekularer Editor mit schützender Seite
In jeder Zelle werden Botschaften, die genetische Information tragen, als RNA verfasst. ADAR2 ist einer der „Editoren“ des Körpers, die diese Botschaften nachträglich dezent verändern können. Die Gruppe untersuchte zunächst die normale Knochenentwicklung und stellte fest, dass ADAR2 in frühen Stammzellen des Knochenmarks niedrig ist, aber mit der Reifung zu Osteoblasten—den knochenbildenden Zellen—ansteigt. Wenn sie ADAR2 in gesunden Stammzellen künstlich erhöhten, schalteten diese Zellen knochenbezogene Gene ein und verbesserten ihre Fähigkeit, mineralisierte Knochenmatrix zu bilden. Umgekehrt schwächte die Herunterregulierung von ADAR2 in gesunden Osteoblasten wichtige Knochenmarker und verringerte ihre knochenbildende Aktivität, was zeigt, dass ADAR2 für den normalen Knochenaufbau wichtig ist.
Niedriges ADAR2 kennzeichnet aggressivere Tumoren
Die Forschenden wandten sich dann Osteosarkomproben und Zelllinien zu. In Patientendatensätzen wiesen Tumoren deutlich weniger ADAR2 auf als gesunde Knochenmarkstammzellen, und Patientinnen und Patienten, deren Tumoren besonders niedrige ADAR2‑Werte zeigten, hatten eine schlechtere Überlebensrate und mehr Metastasen. In einem Mausmodell, in dem Osteosarkomzellen vom Knochen in die Lunge streuten, hatten die migrierenden Zellen ebenfalls deutlich niedrigere ADAR2‑Spiegel als die im Knochen verbliebenen. Zusammengenommen deuten diese Befunde darauf hin, dass der Verlust dieses molekularen Editors mit einem aggressiveren Krankheitsverlauf und schlechteren klinischen Ergebnissen verknüpft ist.
Krebszellen zum Erwachsenwerden zwingen
Um zu testen, ob die Wiederherstellung von ADAR2 Osteosarkom zähmen kann, konstruierten die Forschenden zwei menschliche Osteosarkomzelllinien so, dass sie entweder aktives ADAR2, eine inaktive Mutantenform oder eine Kontrolle überexprimierten. Zellen mit aktivem ADAR2 teilten sich langsamer, verweilten länger in einer Ruhephase des Zellzyklus und invasierten das umliegende Gewebe weniger. In einer Zelllinie, die teilweise knochenähnliches Verhalten zeigte, verstärkte aktives ADAR2 die Bildung mineralisierter Noduli stark und schaltete Gene ein, die mit voll ausgereiften Knochenzellen assoziiert sind, während Marker für Stammhaftigkeit und Bösartigkeit reduziert wurden. Wichtig ist: Als diese veränderten Zellen in die Knochen von immundefizienten Mäusen implantiert wurden, waren Tumoren aus ADAR2‑überexprimierenden Zellen kleiner und weniger invasiv, und die Tiere entwickelten weniger Leber‑ und Lungenmetastasen. Die inaktive Mutante schützte nicht, was darauf hindeutet, dass die Editieraktivität von ADAR2 entscheidend ist.
Ein Wachstums‑Schalter in Krebszellen wird editiert
Um aufzudecken, wie ADAR2 diese Effekte vermittelt, nutzte das Team RNA‑Sequenzierung, um sowohl Genexpressionsänderungen als auch Editierereignisse zu kartieren. Sie fanden Hunderte von Genen, die in einer Weise verändert waren, die zu verringerter Bösartigkeit und besserer Knochenspezialisierung passt. Am auffälligsten editierte ADAR2 stark ein Gen namens IGFBP7, das für ein Protein kodiert, das Wachstumssignale über den IGF1‑Rezeptor verstärken kann—einen Weg, von dem bekannt ist, dass er Überleben und Proliferation von Tumorzellen fördert. ADAR2 wandelte eine einzelne Aminosäure in IGFBP7 um und erzeugte so eine leicht veränderte Proteinvariante. In Osteosarkomzellen war diese editierte Form mit einer schwächeren Aktivierung der IGF1‑Signalkette und mit geringerer Aktivität von nachgeschalteten Wachstumstreibern verbunden. Wenn Zellen mit dem nicht editierten IGFBP7‑Protein behandelt wurden, wurden Wachstumswege aktiviert, die Zellen teilten sich schneller und ein wichtiger knochenbildender Transkriptionsfaktor nahm ab. Dagegen stimulierte die editierte Form das Wachstum nicht; stattdessen förderte sie den knochenbezogenen Faktor und begünstigte Differenzierung gegenüber Division.
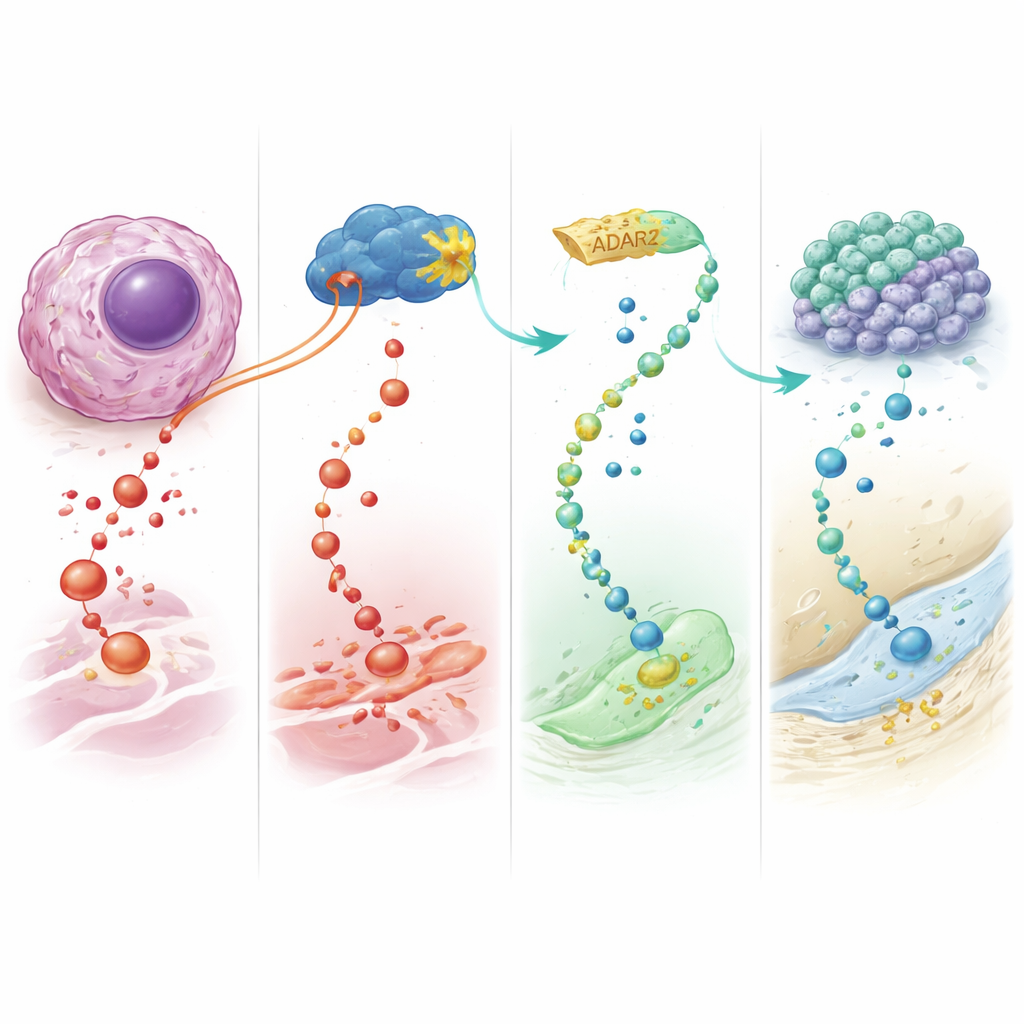
Therapie neu denken: Reprogrammierung statt Vernichtung
Im Kern zeigt diese Arbeit, dass ADAR2 ein natürlicher Tumorsuppressor im Osteosarkom ist, der durch das Umschreiben spezifischer RNA‑Botschaften wirkt, insbesondere der für IGFBP7. Die Verstärkung von ADAR2 lenkt maligne Knochenzellen weg von unkontrolliertem Wachstum und hin zu terminaler, knochenähnlicher Differenzierung, während sie sie zugleich empfindlicher für bestehende Chemotherapien macht. Für Patientinnen und Patienten besteht die langfristige Hoffnung in einer neuen Klasse von „Differenzierungstherapien“, die Krebszellen umprogrammieren statt nur zerstören—möglicherweise mit besseren Ergebnissen bei einer Kinderkrebsform, in der dringend bessere Optionen benötigt werden.
Zitation: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
Schlüsselwörter: Osteosarkom, RNA-Editierung, ADAR2, Knochen-Differenzierung, IGFBP7