Clear Sky Science · ar
ADAR2 يحفز تمايز خلايا سرطان العظم عبر نشاط التحرير على IGFBP7: تداعيات علاجية جديدة
تحويل سرطان عظمي خطير نحو الشفاء
الورم العظمي السُرِياني نادر لكنه عدواني وغالباً ما يصيب الأطفال والمراهقين. على الرغم من الجراحة والعلاجات الكيميائية القوية، لا يزال العديد من المرضى الصغار يتعرضون للانتكاس أو لتكوّن نقائل رئوية. تستقصي هذه الدراسة فكرة ناشئة: بدلاً من محاولة قتل الخلايا السرطانية فقط، هل يمكننا دفعها للنضوج لتتصرف مثل خلايا بناء العظم الطبيعية؟ يركز الباحثون على إنزيم تحرير طبيعي للحمض النووي الريبي يُسمى ADAR2 ويكشفون كيف أن تعزيز نشاطه يمكن أن يدفع خلايا الورم العظمي نحو حالة أكثر نضجاً وأقل خطورة.
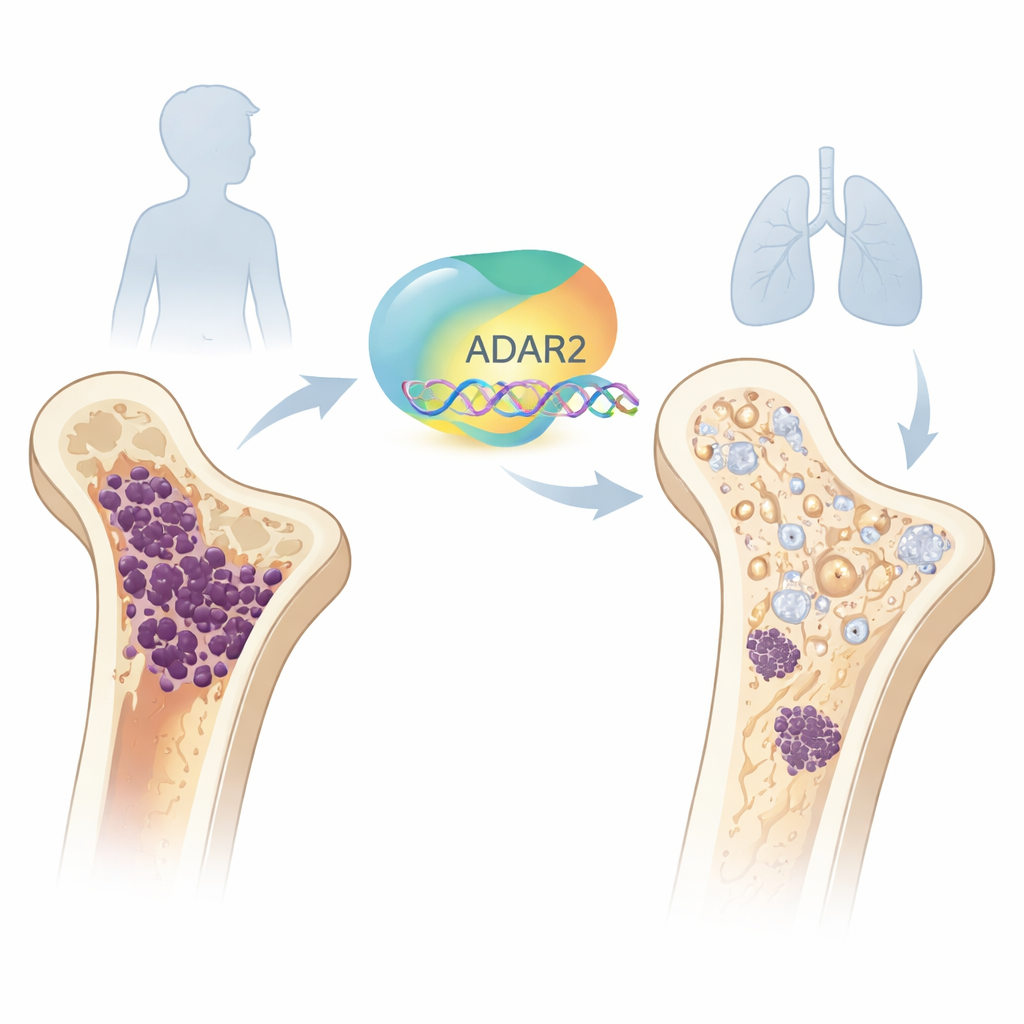
محرر جزيئي له جانب وقائي
داخل كل خلية تُكتب الرسائل الحاملة للمعلومات الوراثية بالحمض النووي الريبي. ADAR2 هو واحد من "المحررين" في الجسم الذين يمكنهم تغيير هذه الرسائل بشكل طفيف بعد كتابتها. نظرت المجموعة أولاً إلى تطور العظام الطبيعي ووجدت أن مستويات ADAR2 منخفضة في الخلايا الجذعية النخاعية المبكرة لكنها ترتفع مع نضوج هذه الخلايا إلى أوستيو بلاستس، وهي الخلايا التي تبني العظم. عندما زادوا ADAR2 صناعياً في الخلايا الجذعية السليمة، أطلقت هذه الخلايا جينات مرتبطة بالعظم وعززت قدرتها على تكوين مصفوفة عظمية متكلسة. وبالعكس، أدى خفض ADAR2 في أوستيو بلاستس السليمة إلى إضعاف مؤشرات عظمية رئيسية وتقليل نشاطها في تكوين العظم، ما يبيّن أن ADAR2 مهم لبناء العظم الطبيعي.
مستويات منخفضة من ADAR2 تميّز الأورام الأكثر عدوانية
توجه الباحثون بعد ذلك إلى عينات وسلالات خلايا الورم العظمي. عبر مجموعات بيانات المرضى، أظهرت الأورام مستويات أقل بكثير من ADAR2 مقارنة بخلايا النخاع العظمي السليمة، وكان المرضى الذين عُرف عن أورامهم أنها ذات ADAR2 منخفض بشكل خاص يعانون من بقاء أقل ونقائل أكثر. في نموذج فأري حيث تنتشر خلايا الورم العظمي من العظم إلى الرئة، كانت الخلايا المهاجرة أيضاً تظهر مستويات أدنى بشكل ملحوظ من ADAR2 مقارنة بتلك المتبقية في العظم. مجتمعة، تشير هذه النتائج إلى أن فقدان هذا المحرر الجزيئي يرتبط بمرض أكثر عدوانية ونتائج سريرية أسوأ.
إجبار الخلايا السرطانية على النضوج
لاختبار ما إذا كان استعادة ADAR2 يمكن أن تهدئ الورم العظمي، مهندست الفريق خليطين خلايا ورم عظمي بشري لإنتاج كميات مفرطة إما من ADAR2 النشط أو من نسخة طفيلية غير نشطة، أو من عنصر ضابط. الخلايا ذات ADAR2 النشط انقسمت بمعدل أبطأ، بقيت لفترة أطول في مرحلة السكون ضمن دورة الخلية، وغزت الأنسجة المحيطة أقل. في إحدى السلالات القادرة جزئياً على إظهار سلوك شبيه بالعظم، عزز ADAR2 النشط بقوة إنتاج العقيدات المتكلسة وشغّل جينات مرتبطة بالخلايا العظمية الناضجة تماماً، بينما خفّض مؤشرات مرتبطة بخصائص الجذعية والورمية. والأهم أن الخلايا المعدلة وزرعت في عظام ساق فئران ناقصة المناعة أنتجت أوراماً أصغر وأقل تغلغلاً عندما كانت تعبر عن ADAR2 مفرط الإنتاج، وطورت الفئران نقائل كبديّة ورئوية أقل. النسخة الطفيلية غير النشطة لم توفر هذا الحماية، مما يشير إلى أن نشاط التحرير الخاص بـ ADAR2 حاسم.
تحرير مفتاح نمو في الخلايا السرطانية
لكشف كيفية ممارسة ADAR2 لتأثيراته، استخدم الفريق تسلسل الحمض النووي الريبي لرسم تغيرات تعبير الجينات وأحداث التحرير. وجدوا مئات الجينات التي تغيرت بطرق تتوافق مع انخفاض الخباثة وتحسين التمايز العظمي. وأكثر ما لفت الانتباه أن ADAR2 حرر بقوة جيناً يُدعى IGFBP7، الذي يشفر بروتيناً يمكنه تعزيز إشارات النمو عبر مستقبل IGF1، وهو مسار معروف بتعزيز نجاة الخلايا الورمية وتكاثرها. حوّل ADAR2 حمض أميني واحد داخل IGFBP7، منتجاً متغيراً بروتينياً مختلفاً قليلاً. في خلايا الورم العظمي، ارتبط الشكل المحرر بتفعيل أضعف لسلسلة إشارة IGF1 وبنشاط أقل لعوامل الدفع النموية المتأخرة. عندما عوملت الخلايا ببروتين IGFBP7 غير المحرر، اشتغلت مسارات النمو، تكاثرت الخلايا أسرع، وانخفض عامل نسخي عظمي رئيسي. بالمقابل، الشكل المحرر فشل في تحفيز النمو، وعزز بدلاً من ذلك العامل المرتبط بالعظم وفضّل التمايز على التقسيم.
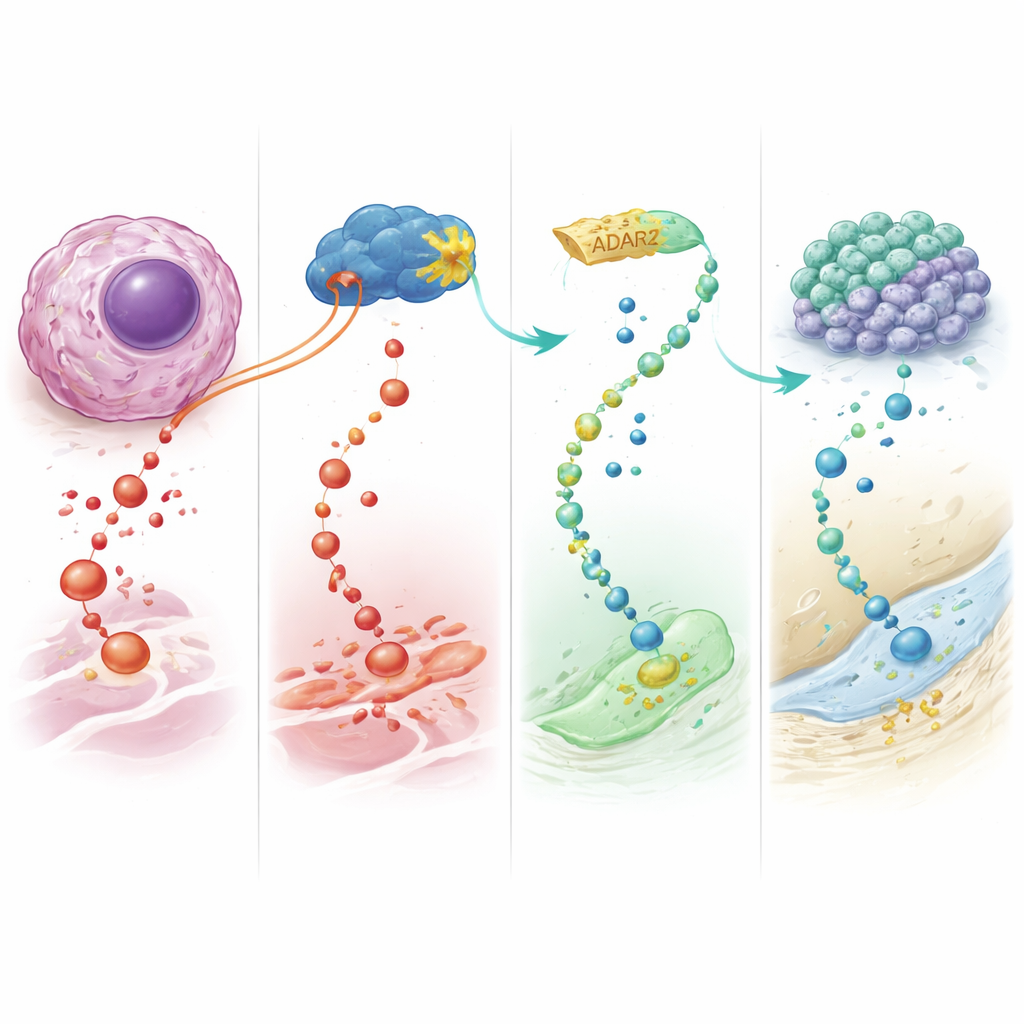
إعادة تأطير العلاج على أنه إعادة برمجة
باختصار، تكشف هذه الدراسة أن ADAR2 يعمل كمثبط ورم طبيعي في الورم العظمي عبر إعادة كتابة رسائل RNA محددة، لا سيما تلك الخاصة بـ IGFBP7. دفع ADAR2 يوجّه الخلايا العظمية الخبيثة بعيداً عن النمو غير المنضبط ونحو التمايز النهائي الشبيه بالعظم، كما يجعلهن أكثر حساسية للأدوية الكيميائية الحالية. للأشخاص المصابين، الأمل طويل المدى هو تطوير فئة جديدة من "علاجات التمايز" التي تعيد برمجة الخلايا السرطانية بدلاً من تدميرها فحسب — ما قد يحسن النتائج في سرطان الأطفال الذي يحتاج إلى خيارات أفضل بشكل عاجل.
الاستشهاد: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
الكلمات المفتاحية: ورم عظمي سُرِياني, تعديل الحمض النووي الريبي, ADAR2, تمايز العظام, IGFBP7