Clear Sky Science · fr
ADAR2 induit la différenciation des cellules d’ostéosarcome par son activité d’édition sur IGFBP7 : nouvelles implications thérapeutiques
Faire basculer un cancer osseux dangereux vers la guérison
L’ostéosarcome est un cancer osseux rare mais agressif qui touche principalement les enfants et les adolescents. Malgré la chirurgie et des chimiothérapies puissantes, trop de jeunes patients rechutent ou développent des métastases pulmonaires. Cette étude explore une idée émergente : plutôt que de chercher uniquement à tuer les cellules cancéreuses, peut‑on les inciter à mûrir et à se comporter davantage comme des cellules normales formant l’os ? Les chercheurs se concentrent sur une enzyme d’édition de l’ARN naturelle, ADAR2, et montrent comment augmenter son activité peut pousser les cellules d’ostéosarcome vers un état plus mature et moins dangereux.
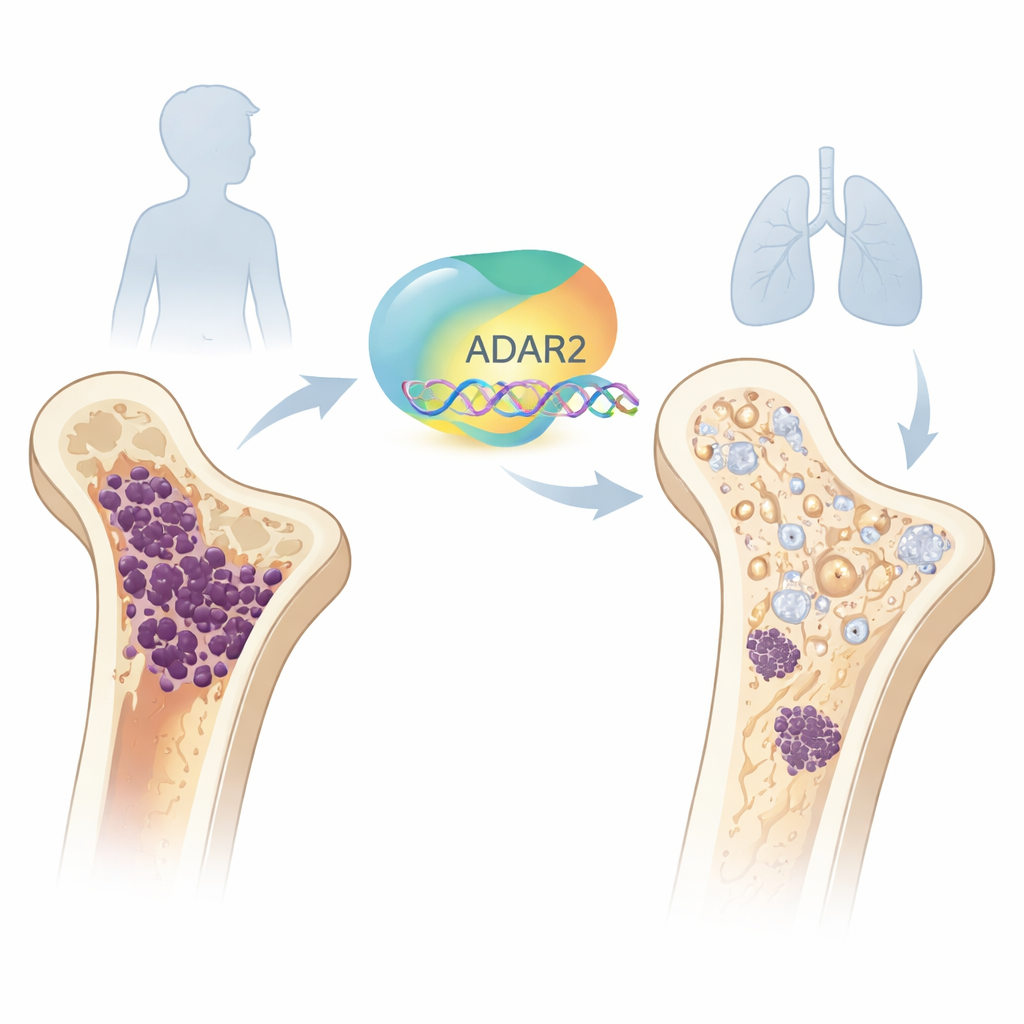
Un éditeur moléculaire au rôle protecteur
À l’intérieur de chaque cellule, les messages portant l’information génétique sont écrits en ARN. ADAR2 est l’un des « éditeurs » de l’organisme capables de modifier subtilement ces messages après leur transcription. L’équipe a d’abord étudié le développement osseux normal et constaté que les niveaux d’ADAR2 sont bas dans les cellules souches de la moelle osseuse au stade précoce, puis augmentent lorsque ces cellules mûrissent en ostéoblastes, les cellules qui construisent l’os. Lorsqu’ils ont artificiellement augmenté l’ADAR2 dans des cellules souches saines, ces cellules ont activé des gènes liés à l’os et amélioré leur capacité à former une matrice osseuse minéralisée. À l’inverse, diminuer ADAR2 chez des ostéoblastes sains affaiblissait des marqueurs osseux clés et réduisait leur activité de construction osseuse, montrant qu’ADAR2 est important pour l’ostéogenèse normale.
Un faible niveau d’ADAR2 signe des tumeurs plus agressives
Les chercheurs se sont ensuite intéressés à des échantillons et lignées cellulaires d’ostéosarcome. Dans les ensembles de données de patients, les tumeurs présentaient beaucoup moins d’ADAR2 que les cellules souches de la moelle osseuse saines, et les patients dont les tumeurs montraient des niveaux particulièrement bas d’ADAR2 avaient une survie plus faible et plus de métastases. Dans un modèle murin où des cellules d’ostéosarcome migrent de l’os vers le poumon, les cellules migrantes avaient aussi des niveaux d’ADAR2 nettement inférieurs à celles restant dans l’os. Ensemble, ces observations suggèrent que la perte de cet éditeur moléculaire est associée à une maladie plus agressive et à de moins bons résultats cliniques.
Forcer les cellules cancéreuses à mûrir
Pour tester si restaurer ADAR2 pouvait calmer l’ostéosarcome, l’équipe a modifié deux lignées cellulaires humaines d’ostéosarcome pour surexprimer soit ADAR2 actif, soit une version mutante inactive, soit un témoin. Les cellules exprimant ADAR2 actif se divisaient plus lentement, restaient plus longtemps en phase de repos du cycle cellulaire et envahissaient moins les tissus environnants. Dans une lignée capable d’un comportement partiellement ostéoïde, ADAR2 actif a fortement augmenté la production de nodules minéralisés et activé des gènes associés aux ostéocytes pleinement matures, tout en réduisant des marqueurs liés à la pluripotence et à la malignité. De façon importante, lorsque ces cellules modifiées ont été implantées dans les os des membres de souris immunodéficientes, les tumeurs formées par les cellules surexprimant ADAR2 étaient plus petites et moins invasives, et les souris développaient moins de métastases hépatiques et pulmonaires. La version mutante inactive n’offrait pas cette protection, indiquant que l’activité d’édition d’ADAR2 est cruciale.
Modifier un commutateur de croissance dans les cellules cancéreuses
Pour comprendre comment ADAR2 produit ces effets, l’équipe a utilisé le séquençage de l’ARN pour cartographier à la fois les changements d’expression génique et les événements d’édition. Ils ont trouvé des centaines de gènes altérés d’une manière cohérente avec une malignité réduite et une meilleure spécialisation osseuse. Plus frappant, ADAR2 éditait fortement un gène appelé IGFBP7, qui code pour une protéine capable d’amplifier les signaux de croissance via le récepteur IGF1, une voie connue pour favoriser la survie et la prolifération des cellules tumorales. ADAR2 a converti un seul acide aminé dans IGFBP7, produisant une variante protéique légèrement différente. Dans les cellules d’ostéosarcome, cette forme éditée était associée à une activation plus faible de la cascade de signalisation IGF1 et à une moindre activité des effecteurs de croissance en aval. Lorsque les cellules étaient traitées par la protéine IGFBP7 non éditée, les voies de croissance s’activaient, les cellules proliféraient plus vite et un facteur de transcription osseuse clé diminuait. En revanche, la forme éditée n’a pas stimulé la croissance, mais a renforcé le facteur lié à l’os et favorisé la différenciation au détriment de la division.
Repenser la thérapie comme reprogrammation
En substance, ce travail met en évidence ADAR2 comme un suppresseur tumoral naturel dans l’ostéosarcome agissant par la réécriture de messages ARN spécifiques, en particulier ceux d’IGFBP7. Augmenter ADAR2 oriente les cellules osseuses malignes loin d’une croissance incontrôlée et vers une différenciation terminale de type osseux, tout en les rendant plus sensibles aux médicaments chimiothérapeutiques existants. Pour les patients, l’espoir à long terme est une nouvelle classe de « thérapies de différenciation » qui reprogramment, plutôt que de simplement détruire, les cellules cancéreuses — améliorant potentiellement les résultats dans un cancer pédiatrique où de meilleures options sont urgemment nécessaires.
Citation: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
Mots-clés: ostéosarcome, édition de l’ARN, ADAR2, différenciation osseuse, IGFBP7