Clear Sky Science · nl
ADAR2 induceert de differentiatie van osteosarcoomcellen via bewerkingsactiviteit op IGFBP7: nieuwe implicaties voor therapie
Een gevaarlijke botkanker richting genezing sturen
Osteosarcoom is een zeldzame maar agressieve botkanker die vooral kinderen en tieners treft. Ondanks chirurgie en krachtige chemotherapie krijgen te veel jonge patiënten nog steeds een recidief of ontwikkelen ze longmetastasen. Deze studie onderzoekt een opkomend idee: in plaats van alleen maar te proberen kankercellen te doden, kunnen we ze ertoe brengen volwassen te worden en zich meer als normale botvormende cellen te gedragen? De onderzoekers richten zich op een natuurlijk RNA-bewerkend enzym genaamd ADAR2 en laten zien hoe het verhogen van diens activiteit osteosarcoomcellen kan aanzetten tot een meer rijpe, minder gevaarlijke toestand.
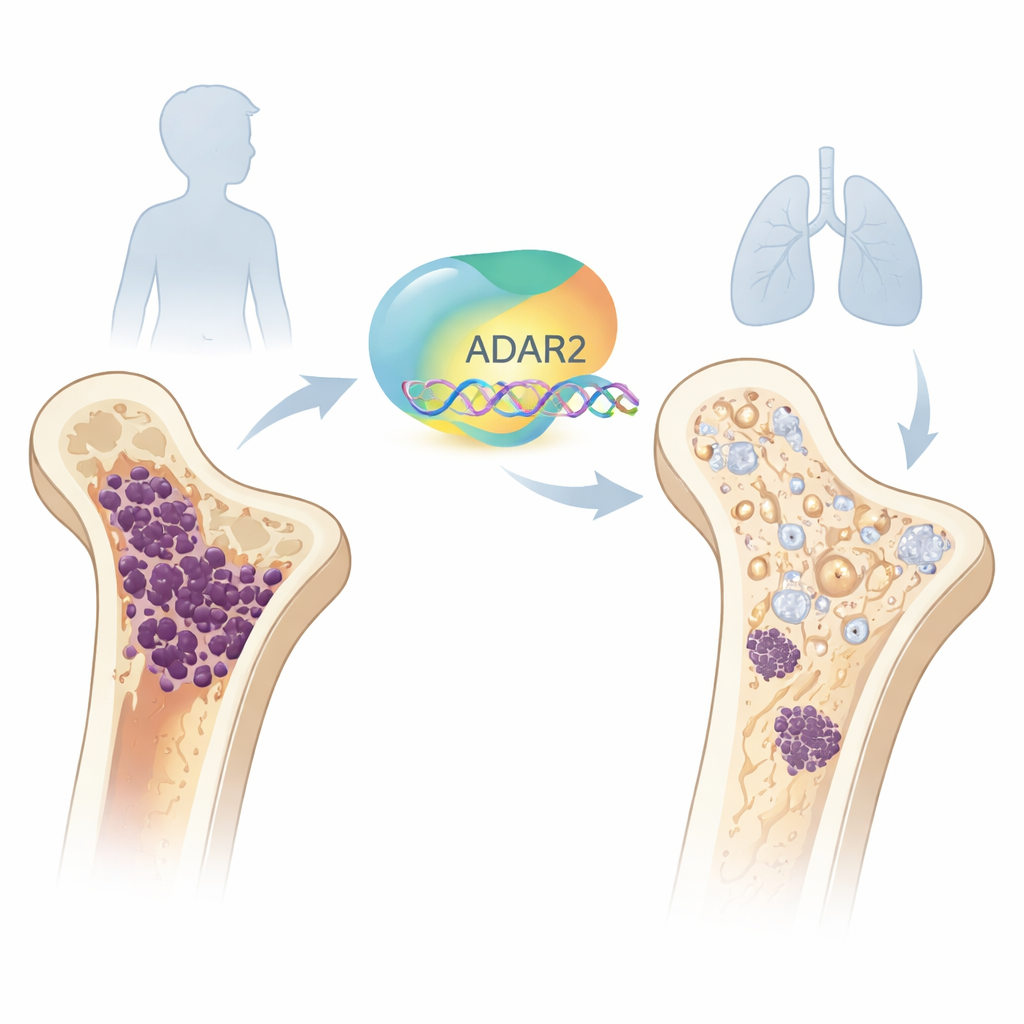
Een moleculair redacteur met een beschermende kant
In elke cel worden boodschappen die genetische informatie dragen in RNA geschreven. ADAR2 is een van de lichaamseigen "redacteuren" die deze boodschappen subtiel kan veranderen nadat ze zijn geschreven. Het team keek eerst naar normale botontwikkeling en vond dat ADAR2-niveaus laag zijn in vroege stamcellen uit het beenmerg, maar toenemen naarmate deze cellen rijpen tot osteoblasten, de cellen die bot opbouwen. Wanneer zij ADAR2 kunstmatig verhoogden in gezonde stamcellen, schakelden deze cellen botgerelateerde genen aan en namen hun capaciteit toe om gemineraliseerde botmatrix te vormen. Omgekeerd verzwakte het terugschakelen van ADAR2 in gezonde osteoblasten belangrijke botmarkers en verminderde hun botvormende activiteit, wat aantoont dat ADAR2 belangrijk is voor normaal botopbouw.
Laag ADAR2 duidt op agressievere tumoren
Vervolgens richtten de onderzoekers zich op osteosarcoommonsters en kweeklijnen. In patiëntendatasets hadden tumoren veel minder ADAR2 dan gezonde beenmergstamcellen, en patiënten wier tumoren bijzonder weinig ADAR2 toonden, hadden slechtere overleving en meer metastasen. In een muismodel waarin osteosarcoomcellen zich van bot naar long verspreidden, hadden de migrerende cellen eveneens duidelijk lagere ADAR2-niveaus dan die in het bot achterbleven. Gezamenlijk suggereren deze bevindingen dat het verlies van deze moleculaire redacteur samenhangt met een agressievere ziekte en slechtere klinische uitkomsten.
Kankercellen dwingen volwassen te worden
Om te testen of het herstellen van ADAR2 osteosarcoom kon temmen, maakten de onderzoekers twee menselijke osteosarcoomkweeklijnen die te veel van ofwel actieve ADAR2, een inactieve mutantversie, of een controle produceerden. Cellen met actieve ADAR2 deelden langzamer, bleven langer in een rustfase van de celcyclus en drongen minder gemakkelijk omringend weefsel binnen. In één kweeklijn met gedeeltelijk botachtig gedrag versterkte actieve ADAR2 sterk de productie van gemineraliseerde knobbeltjes en schakelde genen aan die geassocieerd zijn met volledig rijpe botcellen, terwijl markers voor stamcelkenmerken en maligniteit juist afnamen. Belangrijk is dat wanneer deze gemodificeerde cellen in de beenderen van immuundeficiënte muizen werden geïmplanteerd, tumoren gevormd door ADAR2-overexpressieve cellen kleiner en minder invasief waren, en de muizen minder lever- en longmetastasen ontwikkelden. De inactieve mutant bood deze bescherming niet, wat aangeeft dat de bewerkingsactiviteit van ADAR2 cruciaal is.
Een groeischakelaar bewerken in kankercellen
Om te achterhalen hoe ADAR2 deze effecten teweegbrengt, gebruikte het team RNA-sequencing om zowel veranderingen in genexpressie als bewerkingsevenementen in kaart te brengen. Ze vonden honderden genen die op manieren waren veranderd die passen bij verminderde maligniteit en betere botspecialisatie. Het meest opmerkelijk was dat ADAR2 zwaar een gen genaamd IGFBP7 bewerkte, dat codeert voor een eiwit dat groeisignalen via de IGF1-receptor kan versterken — een pad dat bekendstaat om tumorceldoverleving en proliferatie te bevorderen. ADAR2 veranderde één aminozuur in IGFBP7, waardoor een licht afwijkende eiwitvariant ontstond. In osteosarcoomcellen hing deze bewerkte vorm samen met zwakkere activatie van de IGF1-signaalketen en met lagere activiteit van downstream groeidrivers. Wanneer cellen werden behandeld met het onbewerkte IGFBP7-eiwit, gingen groeipaden aan, deelden cellen sneller en daalde een sleuteltranscriptiefactor voor bot. De bewerkte vorm daarentegen stimuleerde groei niet; in plaats daarvan versterkte hij de botgerelateerde factor en bevorderde differentiatie boven deling.
Therapie herdefiniëren als herprogrammering
In wezen toont dit werk ADAR2 als een natuurlijke tumorsuppressor in osteosarcoom die werkt door specifieke RNA-boodschappen te herschrijven, met name die voor IGFBP7. Het verhogen van ADAR2 stuurt kwaadaardige botcellen weg van ongecontroleerde groei en richting terminale botachtige differentiatie, en maakt ze tevens gevoeliger voor bestaande chemotherapeutica. Voor patiënten is de lange-termijnhoop een nieuwe klasse van "differentiatietherapieën" die kankercellen herprogrammeren in plaats van ze simpelweg te vernietigen — mogelijk met betere uitkomsten bij een kinderkanker waar dringend betere opties nodig zijn.
Bronvermelding: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
Trefwoorden: osteosarcoom, RNA-bewerking, ADAR2, botdifferentiatie, IGFBP7