Clear Sky Science · ja
ADAR2はIGFBP7の編集活性を介して骨肉腫細胞の分化を誘導する:治療への新たな示唆
危険な骨のがんを修復へと向ける
骨肉腫はまれだが攻撃的な骨のがんで、主に小児や十代の若者に発症します。手術と強力な化学療法があるにもかかわらず、多くの若年患者が再発したり肺転移をきたしたりします。本研究は新たな発想を探ります。すなわち、がん細胞をただ殺すのではなく、正常な骨形成細胞のように“成熟”させることはできないか、というものです。研究者たちは天然のRNA編集酵素であるADAR2に注目し、その活性を高めることで骨肉腫細胞をより成熟し、危険性の低い状態へと押しやる仕組みを明らかにします。
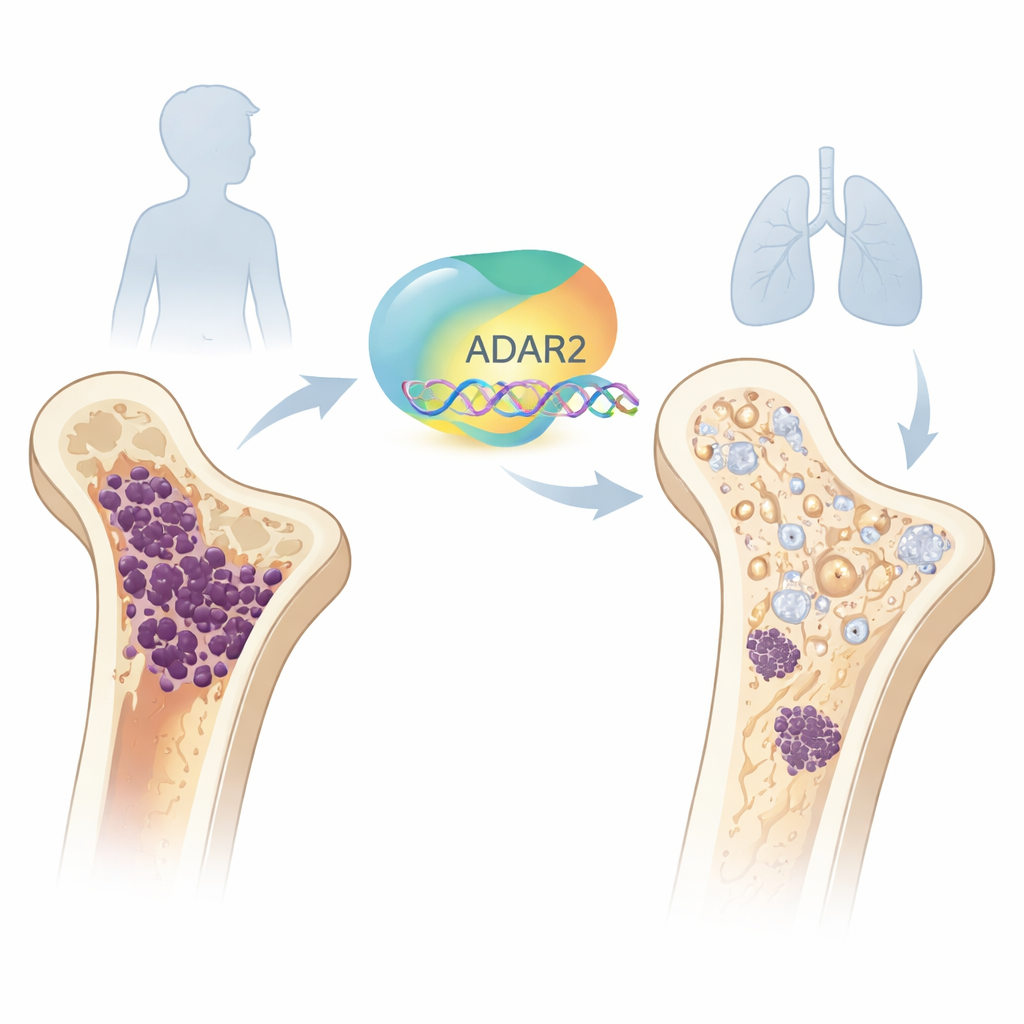
保護的な一面を持つ分子編集者
すべての細胞の中で、遺伝情報を運ぶメッセージはRNAに書き込まれます。ADAR2はこれらのメッセージを微妙に書き換える「編集者」の一つです。研究チームはまず正常な骨発生を調べ、骨髄由来の初期幹細胞ではADAR2のレベルが低いが、これらの細胞が骨を作るオステオブラストへ成熟するにつれてADAR2が上昇することを見出しました。健常な幹細胞でADAR2を人工的に増やすと、骨関連遺伝子が活性化し、石灰化した骨基質を形成する能力が高まりました。逆に健常オステオブラストでADAR2を低下させると、主要な骨マーカーが弱まり骨形成活性が低下し、ADAR2が正常な骨形成に重要であることが示されました。
低いADAR2はより攻撃的な腫瘍の印
次に研究者たちは骨肉腫のサンプルと細胞株に目を向けました。患者データセット全体で、腫瘍は健常な骨髄幹細胞に比べてADAR2が著しく少なく、特にADAR2が低い腫瘍を持つ患者は生存率が低く転移が多いことが示されました。骨から肺へと広がるマウスモデルでも、転移していく細胞は骨に残る細胞より明らかにADAR2レベルが低かった。これらの結果は、この分子編集酵素を失うことがより攻撃的な病態や臨床転帰の悪化と結びつくことを示唆します。
がん細胞に“成長させる”介入
ADAR2を回復させれば骨肉腫を抑えられるかを検証するために、チームは2つのヒト骨肉腫細胞株を改変し、活性型ADAR2、非活性変異型、または対照を過剰発現させました。活性型ADAR2を持つ細胞は増殖が遅く、細胞周期の休止相に長く留まり、周囲組織への侵襲性が低下しました。部分的に骨様の振る舞いを示すある細胞株では、活性ADAR2が石灰化した結節の産生を強力に促進し、完全に成熟した骨細胞に関連する遺伝子をオンにしながら、幹性や悪性に関連するマーカーを低下させました。重要なのは、これらの改変細胞を免疫不全マウスの脛骨に移植すると、ADAR2過剰発現細胞による腫瘍は小さく侵襲性も低く、肝臓や肺への転移も少なかったことです。非活性変異体はこの保護効果を示さず、ADAR2の編集活性が重要であることを示しています。
がん細胞の増殖スイッチを編集する
ADAR2がどのように効果を発揮するかを明らかにするため、チームはRNAシーケンシングを用いて遺伝子発現の変化と編集イベントをマップしました。悪性度の低下と骨分化の改善に一致するような数百の遺伝子変化が見つかりました。最も注目すべきは、ADAR2がIGFBP7という遺伝子を強く編集していたことです。IGFBP7はIGF1受容体を介して増殖シグナルを増強し得るタンパク質をコードしており、これは腫瘍細胞の生存と増殖を促す経路として知られています。ADAR2はIGFBP7のタンパク質中の1つのアミノ酸を置換し、わずかに異なるタンパク質バリアントを産生しました。骨肉腫細胞では、この編集された形はIGF1シグナル伝達の活性化を弱め、下流の成長ドライバーの活性を低下させました。未編集のIGFBP7タンパク質で処理すると成長経路は活性化し細胞増殖が促進され、主要な骨転写因子は減少しました。対照的に、編集された形は成長を刺激せず、むしろ骨関連因子を高めて分化を促し、分裂よりも成熟を支持しました。
治療を再プログラミングとして再定義する
要するに、本研究はADAR2を骨肉腫における天然の腫瘍抑制因子として提示し、特にIGFBP7のような特定のRNAメッセージを書き換えることで作用することを示しています。ADAR2を増強することで、悪性の骨細胞を制御不能な増殖から終末的な骨様分化へと導き、既存の化学療法薬に対する感受性も高めます。患者にとっての長期的な望みは、がん細胞を単に破壊するのではなく再プログラムする「分化療法」という新しい治療クラスの実現であり、小児がんという切実に改善が求められる領域で転帰を向上させる可能性があります。
引用: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
キーワード: 骨肉腫, RNA編集, ADAR2, 骨分化, IGFBP7