Clear Sky Science · pl
ADAR2 powoduje różnicowanie komórek osteosarcoma poprzez aktywność edycyjną na IGFBP7: nowe implikacje terapeutyczne
Skierowanie groźnego nowotworu kości ku uzdrowieniu
Osteosarcoma to rzadki, ale agresywny nowotwór kości, który dotyka głównie dzieci i nastolatków. Pomimo operacji i silnej chemioterapii zbyt wielu młodych pacjentów dalej doświadcza nawrotów lub rozwija przerzuty do płuc. W tym badaniu badacze rozważają nową koncepcję: zamiast wyłącznie próbować zabijać komórki nowotworowe, czy można nakłonić je, by dojrzały i zachowywały się bardziej jak normalne komórki budujące kość? Zespół koncentruje się na naturalnym enzymie edytującym RNA, ADAR2, i pokazuje, jak wzmocnienie jego aktywności może przesunąć komórki osteosarcomy w kierunku bardziej dojrzałego, mniej niebezpiecznego stanu.
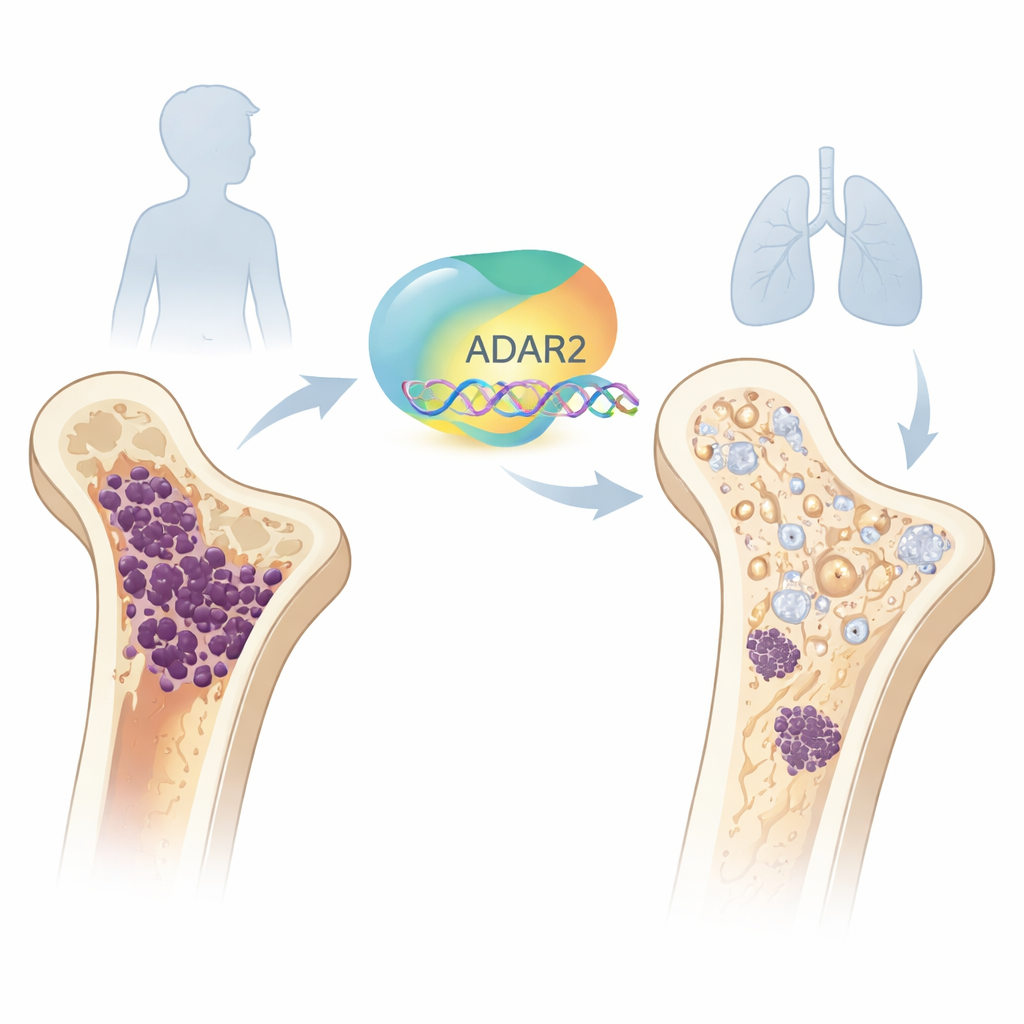
Molekularny redaktor z ochronną rolą
W każdej komórce informacje genetyczne przekazywane są za pomocą RNA. ADAR2 jest jednym z „redaktorów”, które mogą subtelnie zmieniać te komunikaty po ich zapisaniu. Zespół najpierw przyjrzał się prawidłowemu rozwojowi kości i stwierdził, że poziomy ADAR2 są niskie w wczesnych komórkach macierzystych szpiku kostnego, lecz rosną wraz z dojrzewaniem tych komórek do osteoblastów — komórek budujących kość. Gdy sztucznie zwiększono ADAR2 w zdrowych komórkach macierzystych, uruchamiały one geny związane z kością i zwiększały zdolność tworzenia zmineralizowanej macierzy kostnej. Odwrotnie, obniżenie ADAR2 w zdrowych osteoblastach osłabiło kluczowe markery kostne i zmniejszyło aktywność tworzenia kości, co pokazuje, że ADAR2 ma znaczenie dla prawidłowego budowania kości.
Niski poziom ADAR2 oznacza bardziej agresywne guzy
Badacze zwrócili następnie uwagę na próbki osteosarcomy i linie komórkowe. W analizach danych pacjentów guzy wykazywały znacznie mniej ADAR2 niż zdrowe komórki macierzyste szpiku kostnego, a u pacjentów, których guzy miały szczególnie niski poziom ADAR2, obserwowano gorsze przeżycie i więcej przerzutów. W modelu myszy, w którym komórki osteosarcomy rozprzestrzeniały się z kości do płuc, komórki migrujące także miały wyraźnie niższe poziomy ADAR2 niż te pozostające w kości. Razem te wyniki sugerują, że utrata tego molekularnego redaktora wiąże się z bardziej agresywną chorobą i gorszymi wynikami klinicznymi.
Zmuszanie komórek nowotworowych do „dorastania”
Aby sprawdzić, czy przywrócenie ADAR2 może okiełznać osteosarcomę, zespół przeprowadził inżynierię genetyczną w dwóch ludzkich liniach komórkowych osteosarcomy, by nadprodukowały aktywny ADAR2, nieaktywny mutant lub kontrolę. Komórki z aktywnym ADAR2 dzieliły się wolniej, dłużej pozostawały w fazie spoczynkowej cyklu komórkowego i mniej chętnie inwadowały otaczające tkanki. W jednej z linii, która zachowywała częściowe właściwości kostne, aktywny ADAR2 silnie zwiększył powstawanie zmineralizowanych grudek i uruchomił geny związane z w pełni dojrzałymi komórkami kostnymi, jednocześnie zmniejszając markery związane z „macierzystością” i złośliwością. Co istotne, gdy te zmodyfikowane komórki wszczepiono do kości kończyn immunodeficytnych myszy, guzy wywołane przez komórki nadekspresyjne dla ADAR2 były mniejsze i mniej inwazyjne, a u myszy rozwijało się mniej przerzutów do wątroby i płuc. Nieaktywny mutant nie zapewniał tej ochrony, co wskazuje, że aktywność edycyjna ADAR2 jest kluczowa.
Edycja przełącznika wzrostu w komórkach nowotworowych
Aby ustalić, jak ADAR2 wywołuje te efekty, zespół zastosował sekwencjonowanie RNA, mapując zarówno zmiany ekspresji genów, jak i zdarzenia edycyjne. Odkryli setki genów zmienionych w sposób zgodny ze zmniejszoną złośliwością i lepszym wyspecjalizowaniem kostnym. Najbardziej uderzającym odkryciem było intensywne edytowanie przez ADAR2 genu o nazwie IGFBP7, który koduje białko mogące wzmacniać sygnały wzrostowe przez receptor IGF1 — szlak znany z promowania przeżycia i proliferacji komórek nowotworowych. ADAR2 zamienił pojedynczy aminokwas w IGFBP7, tworząc nieco inną wariantę białka. W komórkach osteosarcomy ta edytowana forma wiązała się ze słabszą aktywacją łańcucha sygnalizacyjnego IGF1 i niższą aktywnością dalszych czynników napędzających wzrost. Gdy komórki traktowano nieedytowanym białkiem IGFBP7, szlaki wzrostu się aktywowały, komórki proliferowały szybciej, a kluczowy czynnik transkrypcyjny kości ulegał zmniejszeniu. W przeciwnym razie edytowana forma nie stymulowała wzrostu, za to zwiększała czynnik związany z kością i sprzyjała różnicowaniu zamiast podziałom.
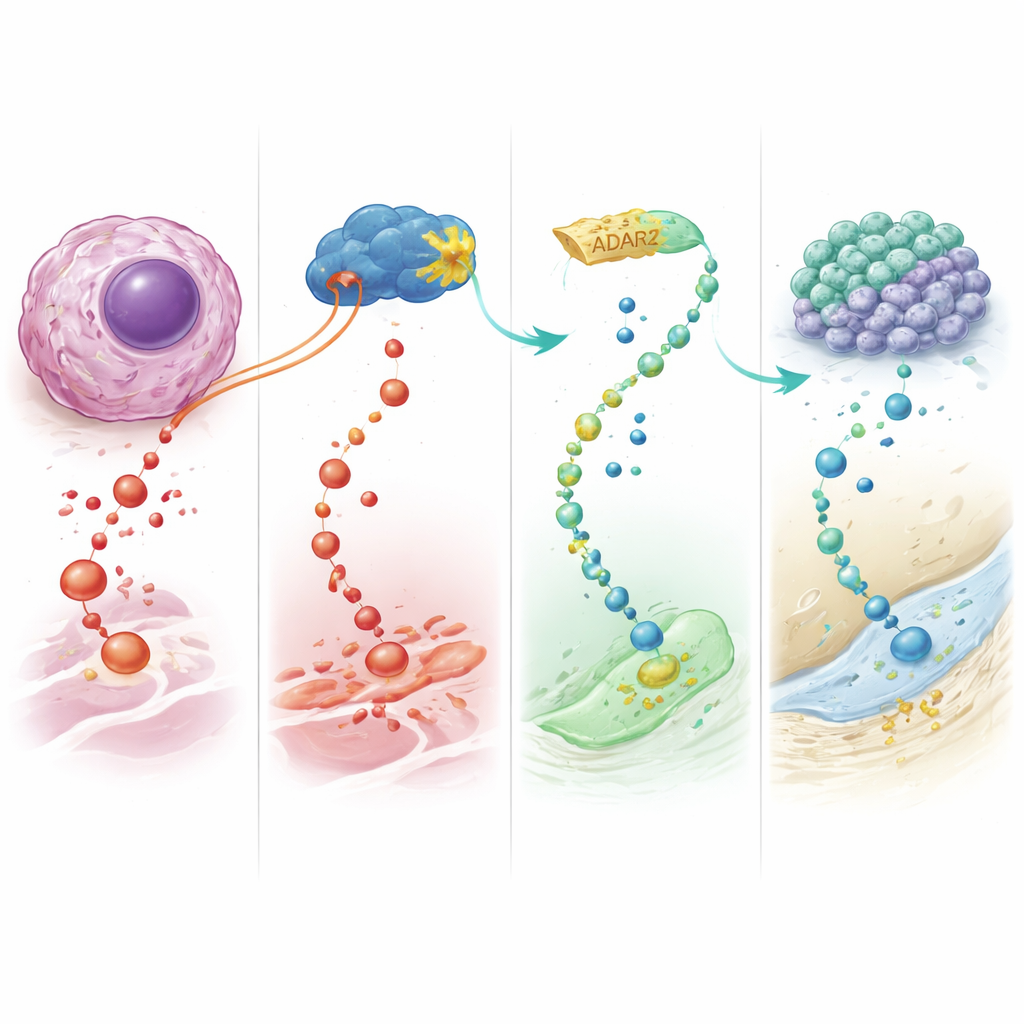
Przeformułowanie terapii jako reprogramowania
W istocie praca ta ukazuje ADAR2 jako naturalny supresor guza w osteosarcomie, działający przez przepisywanie określonych komunikatów RNA, w szczególności tych dotyczących IGFBP7. Wzmocnienie ADAR2 kieruje złośliwe komórki kostne z dala od niekontrolowanego wzrostu ku terminalnemu różnicowaniu kostnemu, a także zwiększa ich wrażliwość na istniejące leki chemioterapeutyczne. Dla pacjentów długoterminowa nadzieja wiąże się z nową klasą „terapii różnicujących”, które reprogramują, zamiast jedynie niszczyć, komórki nowotworowe — co potencjalnie może poprawić wyniki w nowotworze wieku dziecięcego, gdzie pilnie potrzebne są lepsze opcje leczenia.
Cytowanie: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
Słowa kluczowe: osteosarcoma, edycja RNA, ADAR2, różnicowanie kości, IGFBP7