Clear Sky Science · he
ADAR2 גורם להבדלה של תאי אוסטאוסרקומה באמצעות פעילות עריכה על IGFBP7: השלכות חדשות לטיפול
לפנות סוג מסוכן של סרטן עצם לכיוון ריפוי
אוסטאוסרקומה היא סרטן עצם נדיר אך אגרסיבי שמדביק בעיקר ילדים ונוער. למרות ניתוח וכימותרפיה מפרכת, עדיין רבים מהמטופלים הצעירים מושבים או מפתחים גרורות לריאות. המחקר בוחן רעיון עולה: במקום רק לנסות להרוג את תאי הסרטן, האם אפשר לגרום להם להתבגר ולהתנהג יותר כמו תאי בונה עצם נורמליים? החוקרים מתמקדים באנזים טבעי לעריכת RNA בשם ADAR2 וחשפו כיצד הגברת פעילותו יכולה לדחוף תאי אוסטאוסרקומה למצב בוגר יותר ופחות מסוכן.
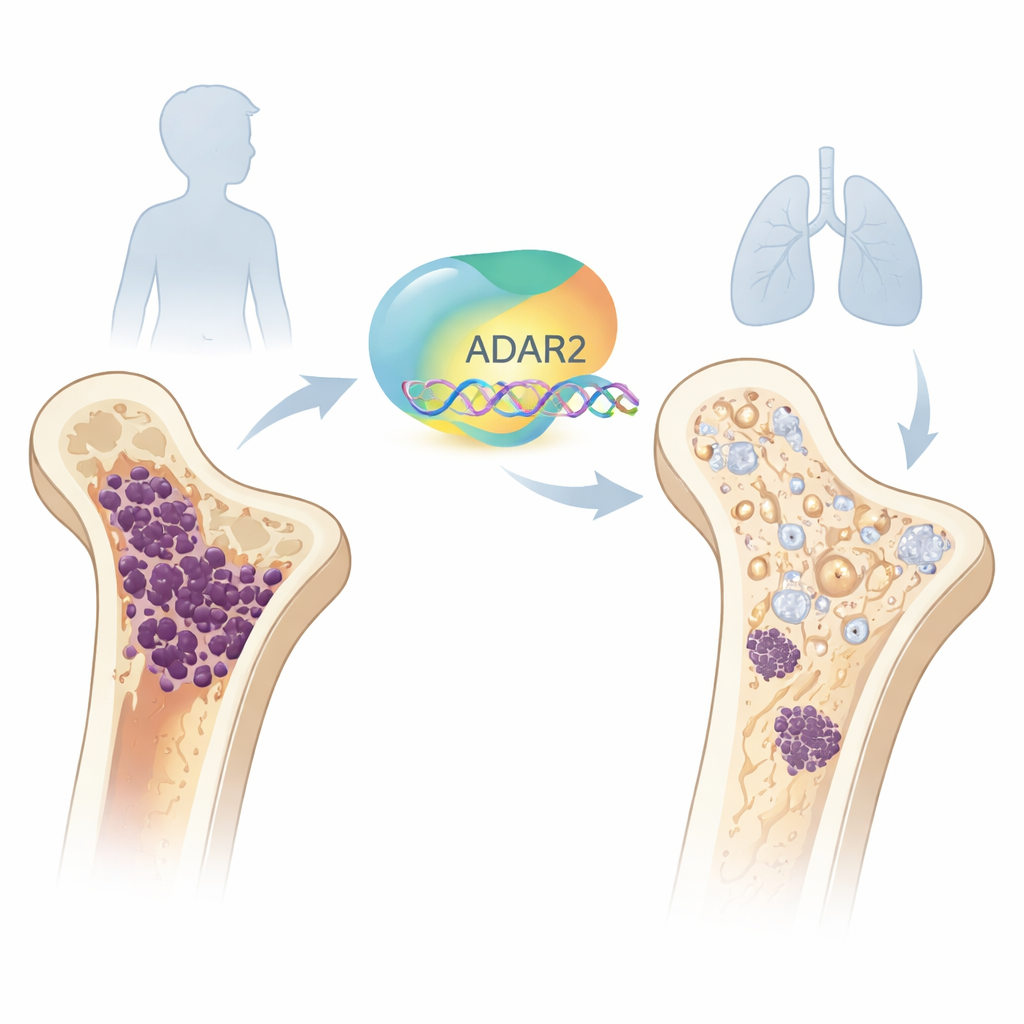
עורך מולקולרי עם צד מגונן
בתוך כל תא, ההודעות הנושאות מידע גנטי כתובות ב‑RNA. ADAR2 הוא אחד מה"עורכים" של הגוף שיכול לשנות בעדינות הודעות אלה לאחר שנכתבו. הצוות בחן תחילה התפתחות עצם נורמלית ומצא שרמות ADAR2 נמוכות בתאי גזע ממח העצם בשלבים מוקדמים, אך עולות ככל שהתאים מתבגרים לאוסטאובלסטים — התאים הבונים את העצם. כאשר הגבירו באופן מלאכותי את ADAR2 בתאי גזע בריאים, התאים הפעילו גנים הקשורים לעצם והגבירו את יכולתם לייצר מטריצת עצם מזוהמת במינרלים. להפך, השתקת ADAR2 באוסטאובלסטים בריאים החלישה סמני עצם מרכזיים והקטינה את פעילות ייצור העצם שלהם, מה שמראה כי ADAR2 חשוב לבנייה תקינה של העצם.
רמות נמוכות של ADAR2 מסמנות גידולים אגרסיביים יותר
החוקרים פנו לאחר מכן לדגימות אוסטאוסרקומה ולשורות תאים. בערכות נתוני חולים, לגידולים היו הרבה פחות ADAR2 מאשר בתאי גזע של מח עצם בריאים, והחולים שלגידוליהם היו רמות ADAR2 נמוכות במיוחד חיו פחות והציגו יותר גרורות. במודל עכבר שבו תאי אוסטאוסרקומה היגרו מהעצם אל הריאות, התאים המהגרים הראו גם הם רמות ADAR2 נמוכות משמעותית בהשוואה לאלה שנשארו בעצם. יחד, ממצאים אלה מרמזים שאובדן העורך המולקולרי קשור למחלה אגרסיבית יותר ותוצאות קליניות גרועות יותר.
לכפות על תאי הסרטן "להתבגר"
כדי לבדוק האם השבת ADAR2 יכולה לאלף את האוסטאוסרקומה, הצוות הנדס שתי שורות תאי אוסטאוסרקומה אנושיות כך שיפרוֹזו באופן יתר או לגרסה מוטנטית לא פעילה או לביקורת. תאים עם ADAR2 פעיל התחלקו לאט יותר, שהו זמן ארוך יותר בשלב מנוחה במחזור התאים ופחות חדרו רקמות מסביב. בשורה תאית אחת שהציגה יכולת חלקית להתנהגות דמוית עצם, ADAR2 פעיל הגביר במידה ניכרת את ייצור הנודולים הממינרלים והפעיל גנים המקושרים לתאי עצם בוגרים באופן מלא, תוך הקטנת סמנים המקושרים לשימור תכונות גזע ומלניגנטיות. חשוב לציין, כאשר תאים מהונדסים אלה הושתלו לעצמות רגל בעכברים חסרי חיסון, הגידולים שנוצרו על ידי תאים בעלי ביטוי יתר של ADAR2 היו קטנים ופחות פולשניים, והעכברים סבלו פחות מגרורות בכבד ובריאה. הגרסה המוטנטית הלא פעילה לא סיפקה את ההגנה הזו, מה שמצביע על כך שפעילות העריכה של ADAR2 היא קריטית.
עריכת מתג גדילה בתאי סרטן
כדי לחשוף כיצד ADAR2 מפעיל השפעות אלה, הצוות השתמש בריצוף RNA כדי למפות גם שינויים בביטוי גנים וגם אירועי עריכה. הם מצאו מאות גנים ששונו בצורה התואמת לפחות מלניגנטיות והעדפת התמחות עצם. הדבר הבולט ביותר היה ש‑ADAR2 ערך בעוצמה גן בשם IGFBP7, שמקודד לחלבון היכול להגביר אותות גדילה דרך קולטני IGF1 — מסלול הידוע בקידום הישרדות ותפוצה של תאי גידול. ADAR2 החליף חומצה אמינית אחת בתוך IGFBP7, וכתוצאה נוצר זן חלבוני מעט שונה. בתאי אוסטאוסרקומה, הצורה הערוכה הזו נקשרה להפעלה חלשה יותר של מי שרשרת האותות של IGF1 ולפעילות נמוכה יותר של מדחפי גדילה במורד הזרם. כאשר תאים טופלו בחלבון IGFBP7 הבלתי‑נערך, מסלולי הגדילה הופעלו, התאים התרבו מהר יותר ופקטור שעתוק מרכזי לעצם ירד. לעומת זאת, הצורה הערוכה לא עוררה את הגדילה, אלא הגברה של הגורם הקשור לעצם והעדפת הבחנה על פני חלוקה.
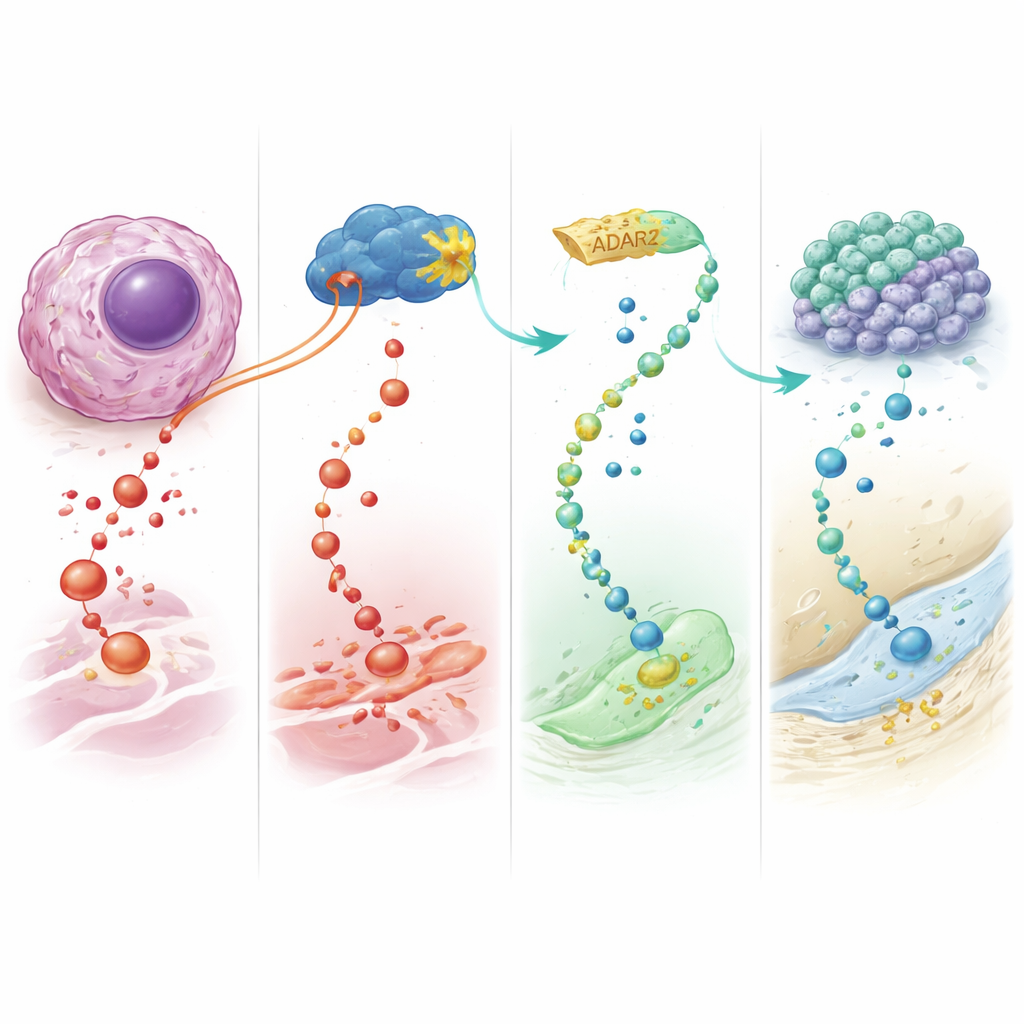
להציג טיפול מחדש כהשבת תכונות
בעיקרו של דבר, עבודה זו מצביעה על ADAR2 כמדכא גידולים טבעי באוסטאוסרקומה, הפועל על ידי כתיבה מחדש של הודעות RNA ספציפיות, במיוחד אלה של IGFBP7. הגברת ADAR2 מפנה תאי עצם ממאירים הרחק מהצמיחה הבלתי נשלטת וכלפי הבחנה סופית הדומה לעצם, ובמקביל עושה אותם רגישים יותר לתרופות הכימותרפיות הקיימות. עבור המטופלים, התקווה לטווח הארוך היא מחלקה חדשה של "טיפולים להבחנה" שמכווינים תכנות מחדש של תאי הסרטן במקום להשמידם בלבד — ובכך עשויים לשפר תוצאות בסרטן ילדים שבו דרושים פתרונות טובים יותר בדחיפות.
ציטוט: Rossi, M., Scotto di Carlo, F., Di Gregorio, J. et al. ADAR2 induces the differentiation of osteosarcoma cells by editing activity on IGFBP7: new implications for therapy. Bone Res 14, 38 (2026). https://doi.org/10.1038/s41413-026-00516-6
מילות מפתח: אוסטאוסרקומה, עריכת RNA, ADAR2, הבחנה של עצם, IGFBP7