Clear Sky Science · zh
成骨细胞中骨抑制蛋白sclerostin的环3与LRP4相互作用是其抑制骨形成所必需的
为什么造骨需要更聪明的开关
随着人们寿命延长,脆弱的骨骼和骨折问题日益凸显,现已有几种强效药物可刺激骨生成。然而,其中一种用于阻断抑骨蛋白sclerostin的抗体在部分患者中与严重心血管问题相关。本研究剖析了sclerostin抑制骨形成的精细机制,并揭示了一种在保持其对心血管系统保护作用的同时,在骨细胞中关闭其“制动器”的方法。
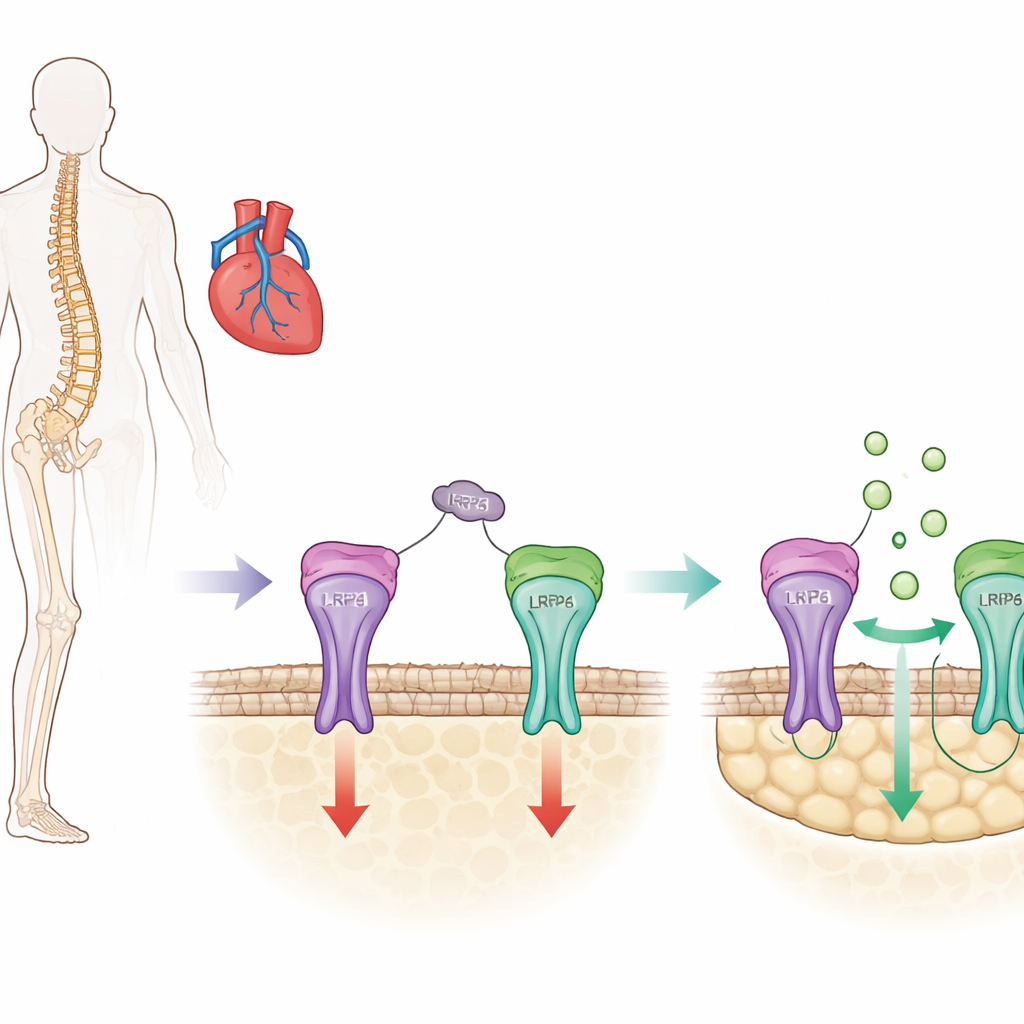
一个关键的骨骼制动器与隐含的另一面
骨组织持续更新,特化细胞不断构建新组织,同时其他细胞去除旧组织。sclerostin是一种主要由骨细胞产生的蛋白,通过抑制促进生长的Wnt/β-连环蛋白(β-catenin)通路,在成骨细胞(成骨细胞)中起到制动作用。现有的抗骨质疏松药物如romosozumab通过阻断sclerostin来解除这一制动,从而迅速增加骨量。然而,临床试验提示,广泛阻断sclerostin也可能干扰其在血管和心脏中的保护功能,增加部分人群心肌梗死和中风的风险。
聚焦一个微小的环
sclerostin在其结构中含有三个小的环状区域,该研究团队此前的工作表明,其中被称为环3的区域有助于sclerostin抑制骨形成,但对其在血管中的保护作用并非必需。本项研究进一步探究环3如何具体介导骨抑制作用。研究者发现,环3可与成骨细胞表面的受体LRP4结合。该结合像一个锚,将sclerostin定位,使其能接触到邻近的另一受体LRP6,后者直接控制Wnt/β-连环蛋白通路。通过生化结合实验和计算机建模,他们定位出了LRP4蛋白上对环3构成关键接触点的特定氨基酸残基。
破坏锚点以释放骨生长
基于这一结构学洞见,团队设计了两种工具以破坏环3–LRP4锚点:一种是通过基因改造在LRP4关键氨基酸上做出细微改变的变体(称为Lrp4m),另一种是模拟LRP4中环3结合区域、可与sclerostin竞争结合的短合成肽(LRP4-Pep)。在体外培养的成骨细胞中,这两种策略都削弱了sclerostin与LRP6的结合能力,减弱了其对Wnt/β-连环蛋白信号的抑制,并保留了细胞成熟与沉积矿物质的能力。计算机模拟支持了这一模型,显示正常LRP4会将sclerostin保持在接近LRP6的位置,而突变型则无法稳定该接触。
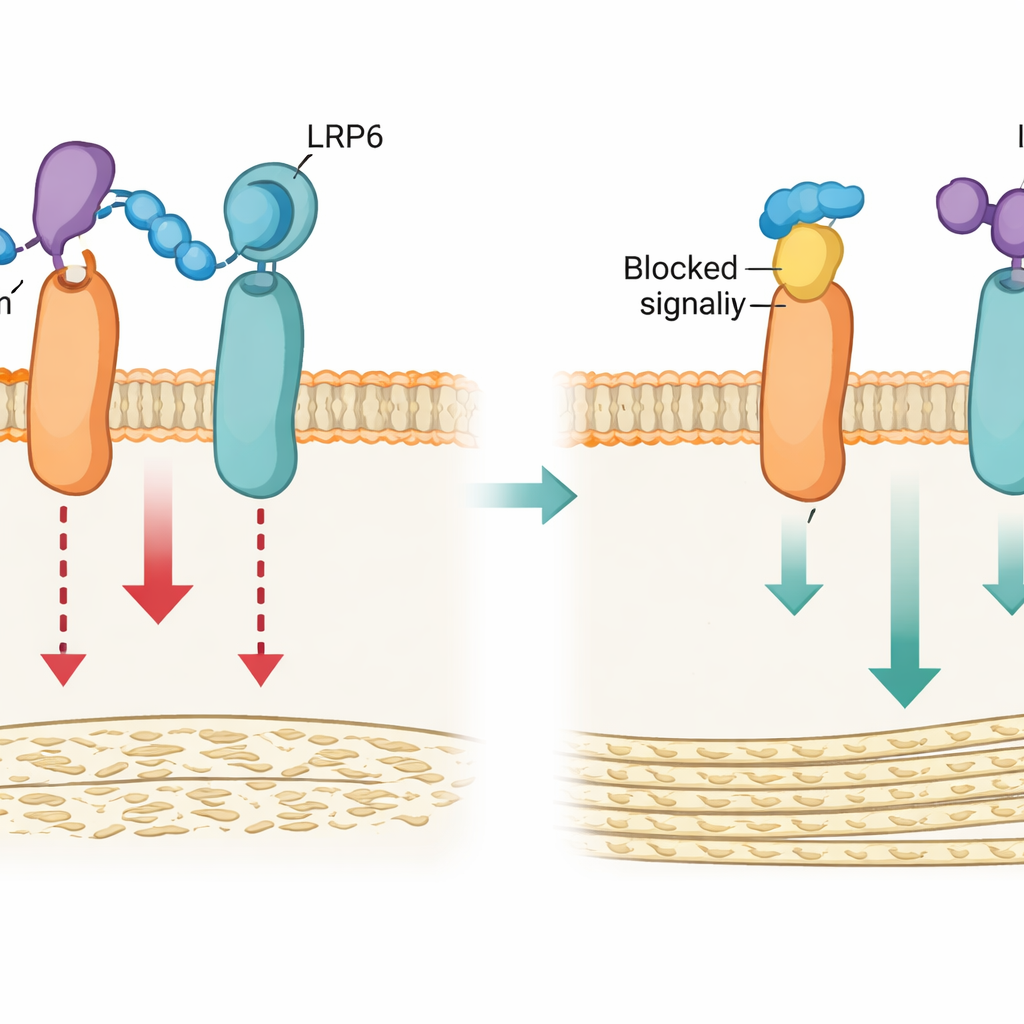
小鼠中更强壮的骨骼且无额外风险
研究者随后转入小鼠模型以验证在活体中破坏环3–LRP4相互作用是否能改善骨健康。全身携带Lrp4m突变的小鼠发育出更致密、更强壮的骨骼,内部结构改良,血液中骨形成标志物升高,且未见肌肉损害。当同样的突变存在于基因缺失sclerostin的小鼠时,并无附加效应,但重新引入sclerostin时显示其抑骨能力在Lrp4m小鼠中明显减弱。同样,在过度表达sclerostin的模型小鼠或已出现雌激素缺乏相关骨质减少的小鼠中,反复给予LRP4-Pep肽按剂量增加可剂量依赖地提高骨量、改善骨质量并增强力学强度,而在缺失sclerostin的情况下则无可检测效应。
迈向更安全的促骨治疗
综上所述,这些发现表明,sclerostin的环3与成骨细胞中的LRP4之间的相互作用是将sclerostin定位到LRP6并关闭骨形成所需的锚点。通过选择性破坏该锚点——无论是通过精确突变还是定制肽——研究者在小鼠中提高了骨生成和强度,同时未直接阻断那些对心血管保护似乎重要的sclerostin区域。对患者而言,这项工作指向了新一代的促骨疗法思路:不是完全抑制sclerostin,而是将其在骨中的作用与对心血管有益的功能解耦。
引用: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
关键词: 骨质疏松, sclerostin, 骨形成, LRP4, Wnt信号