Clear Sky Science · ar
تفاعل حلقة 3-LRP4 مع السكليروستين في الخلايا البانية للعظم مطلوب لكي يثبط السكليروستين تكوّن العظم
لماذا يحتاج بناء العظام إلى مفتاح أكثر دقّة
العظام الهشة والكسور تمثل مشكلة متزايدة مع طول عمر الناس، وتوجد الآن أدوية قوية تحفّز نمو العظم. ومع ذلك، ارتبط دواء واحد مثل مضاد للأجسام المضادة يقطع بروتينًا يثبط العظم يسمى السكليروستين بمشكلات قلبية خطيرة لدى بعض المرضى. تبيّن هذه الدراسة التفاصيل الدقيقة لكيفية إبطاء السكليروستين لتكوّن العظم وتكشف طريقة لإيقاف فرملة العظم في خلايا العظم مع الحفاظ على أدواره الوقائية في الجهاز القلبي الوعائي.
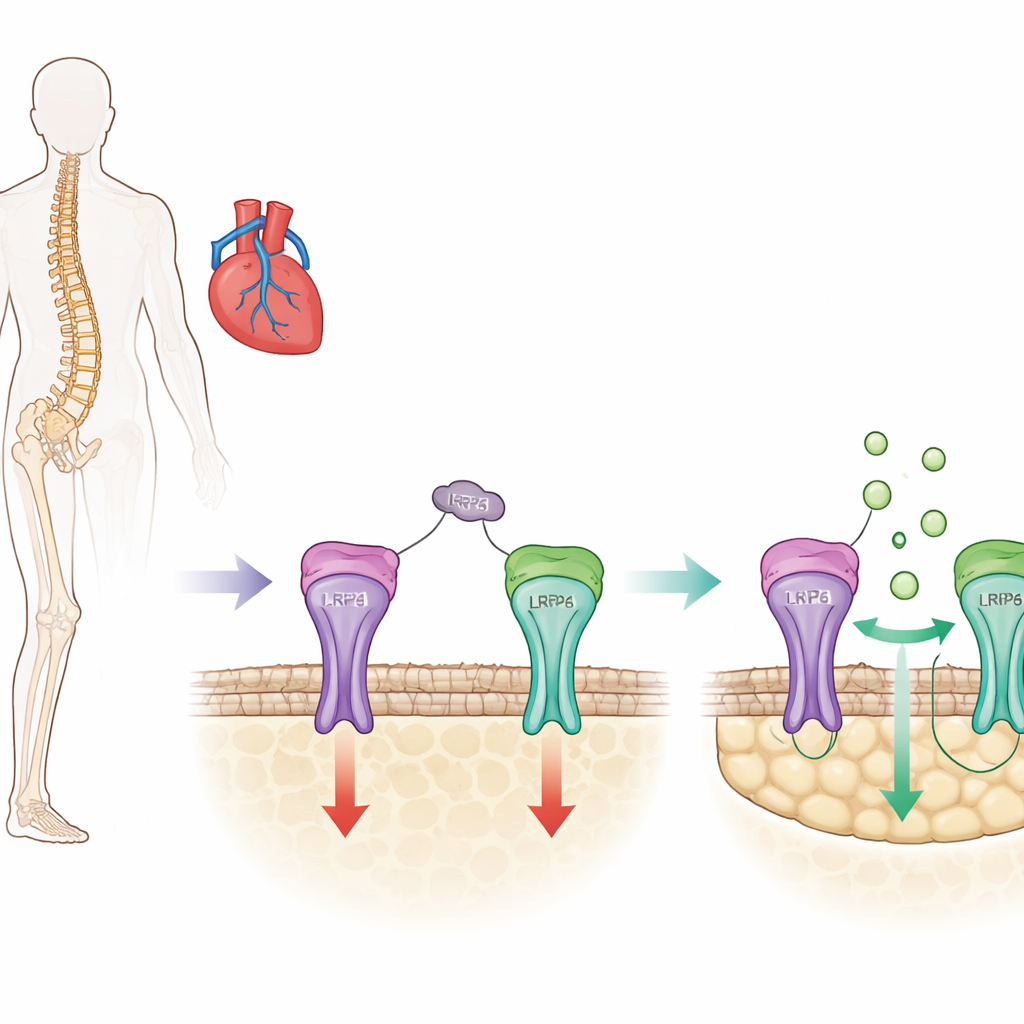
مكبح رئيسي للعظم له جانب مخفي
العظم يتجدد باستمرار إذ تبني خلايا متخصّصة نسيجًا جديدًا بينما تزيل أخرى المادة القديمة. السكليروستين هو بروتين يُنتج بشكل أساسي بواسطة خلايا العظم ويعمل كمكبح لهذه العملية من خلال كبح مسار محفّز للنمو يعرف باسم إشارة Wnt/β‑catenin في خلايا بناء العظم (الأوستيوبلاست). الأدوية الحالية لهشاشة العظام مثل روموسوزوماب تعمل عن طريق حجب السكليروستين، رافعةً هذا المكبح مما يزيد كتلة العظم بسرعة. ومع ذلك، أشارت تجارب سريرية إلى أن الحجب الواسع للسكليروستين قد يخلّ أيضًا بوظائفه الوقائية في الأوعية الدموية والقلب، مما يزيد خطر النوبة القلبية والسكتة لدى بعض الأفراد.
تقريب النظر إلى حلقة صغيرة
يحتوي السكليروستين على ثلاث مناطق صغيرة على شكل حلقات في بنيته، وأظهرت أعمال سابقة من هذه المجموعة أن إحداها، المسماة حلقة 3، تساهم في قمع السكليروستين لتكوّن العظم لكنها ليست ضرورية لوظائفه الوقائية في الأوعية الدموية. في الدراسة الحالية، طرح الباحثون سؤالًا حول الكيفية الدقيقة التي تسهم بها حلقة 3 في تثبيط العظم. اكتشفوا أن حلقة 3 ترتبط بمستقبل على سطح خلية العظم يُدعى LRP4. تعمل هذه الارتباطات كمرساة تضع السكليروستين بحيث يمكنه الوصول إلى مستقبل مجاور آخر، LRP6، الذي يسيطر مباشرة على مسار Wnt/β‑catenin. باستخدام اختبارات ربط بيوكيميائية ونمذجة حاسوبية، حدّدوا الأحماض الأمينية المحددة على بروتين LRP4 التي تعد نقاط اتصال أساسية للحلقة 3.
كسر المرساة لتحرير نمو العظم
مسلحين بهذه الرؤى البنيوية، صمّم الفريق نوعين من الأدوات لتعطيل مرساة حلقة 3–LRP4: نسخة جينية غيّرت بشكل طفيف الأحماض الأمينية الأساسية في LRP4 (تُسمى Lrp4m)، وببتيد صناعي قصير (LRP4‑Pep) يحاكي منطقة ربط حلقة 3 في LRP4 ويتنافس على ربط السكليروستين. في خلايا الأوستيوبلاست المزروعة، أضعفت كلتا الإستراتيجيتين قدرة السكليروستين على الارتباط بـLRP6، وخفّضتا تثبيطه لمسار Wnt/β‑catenin، وحافظتا على قدرة الخلايا على النضج وترسيب المعادن. دعمت المحاكاة الحاسوبية هذه الصورة، مبينةً أن LRP4 الطبيعي يحتفظ بالسكليروستين قريبًا من LRP6، بينما الشكل المتحوّر يفشل في تثبيت هذا الاتصال.
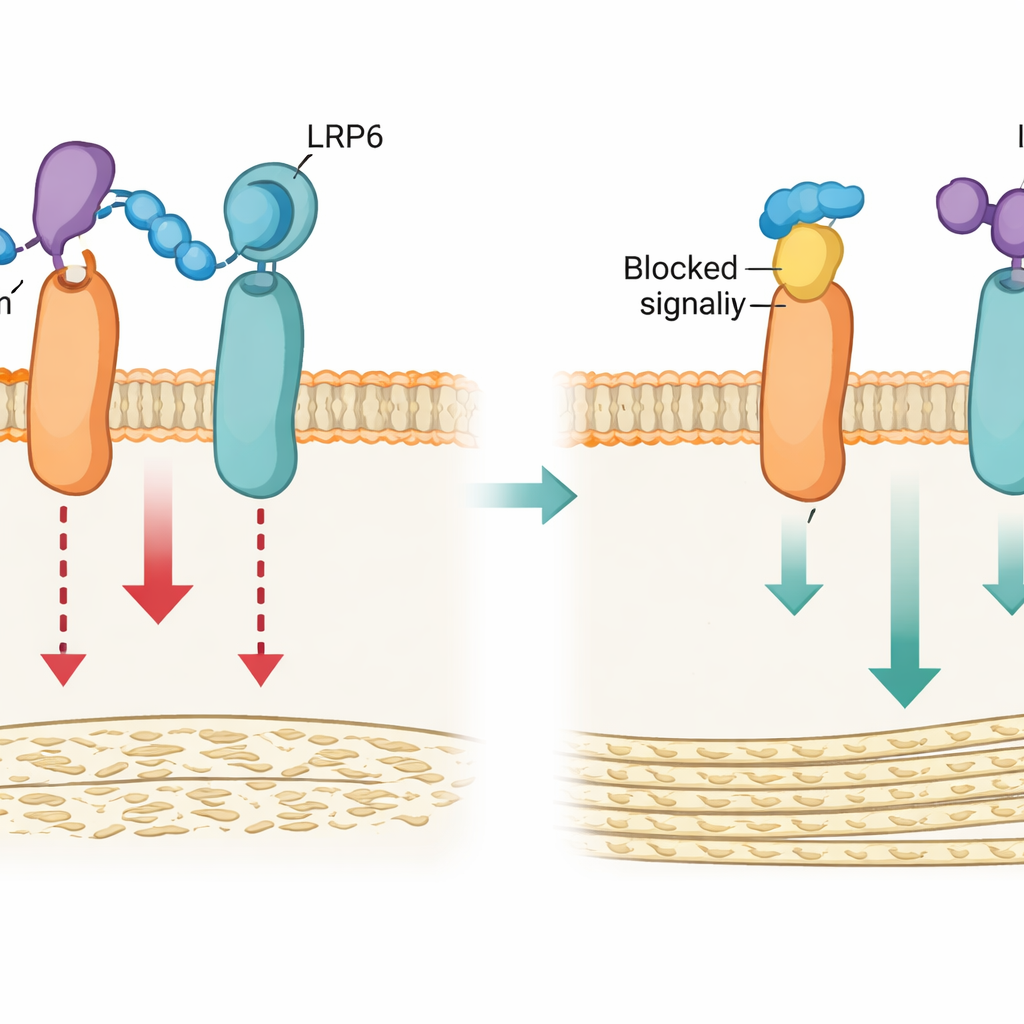
عظام أقوى لدى الفئران دون مخاطر إضافية
ثم انتقل الباحثون إلى نماذج الفئران لتأكيد أن تعطيل تفاعل حلقة 3–LRP4 يحسّن صحة العظام في الحيوانات الحية. أظهرت الفئران التي تحمل طفرات Lrp4m في جميع أنحاء الجسم عظامًا أكثف وأقوى، مع بنية داخلية محسنة ومستويات دم أعلى من مؤشرات تكوين العظم، وبدون أذى ملحوظ للعضلات. عندما وُجدت نفس الطفرة في فئران تفتقر جينيًا إلى السكليروستين، لم يكن هناك تأثير إضافي، لكن إعادة إدخال السكليروستين أظهرت أن قدرته على كبح العظم كانت أضعف بكثير في حيوانات Lrp4m. وبالمثل، في فئران مهندسة لإنتاج كميات زائدة من السكليروستين أو في فئران تعاني بالفعل فقدان العظم المرتبط بنقص الإستروجين، أدت المعالجة المتكررة بببتيد LRP4‑Pep إلى زيادة كتلة العظم بشكل معتمد على الجرعة، وتحسّن جودة العظم، وعزّزت القوة الميكانيكية، ومع ذلك لم يكن لها تأثير قابل للكشف عندما غاب السكليروستين.
نحو علاجات بنيوية آمنة أكثر
تُظهر هذه النتائج مجتمعة أن تفاعلًا بين حلقة 3 في السكليروستين وLRP4 في الأوستيوبلاست هو المرساة التي يحتاجها السكليروستين ليلتقط LRP6 ويوقف تكوّن العظم. من خلال تعطيل هذه المرساة انتقائيًا—سواء عبر طفرات دقيقة أو ببتيد مصمّم—تمكن الباحثون من تعزيز بناء العظم وقوّته في الفئران دون حجب الأجزاء من السكليروستين التي تبدو مهمة للحماية القلبية الوعائية. بالنسبة للمرضى، يشير هذا العمل إلى جيل جديد من علاجات تقوية العظم التي لا تهدف إلى إسكات السكليروستين تمامًا، بل إلى فصل تأثيراته في العظم عن أدواره المفيدة في القلب والأوعية الدموية.
الاستشهاد: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
الكلمات المفتاحية: هشاشة العظام, السكليروستين, تكوين العظم, LRP4, إشارة Wnt