Clear Sky Science · pt
Interação entre o loop3 de esclerostina e LRP4 em osteoblastos necessária para a inibição da formação óssea pela esclerostina
Por que a construção óssea precisa de um interruptor mais inteligente
Ossos frágeis e fraturas são uma preocupação crescente à medida que as pessoas vivem mais, e existem medicamentos novos e potentes para estimular o crescimento ósseo. No entanto, um desses fármacos — um anticorpo que bloqueia uma proteína que inibe os ossos chamada esclerostina — foi associado a problemas cardíacos graves em alguns pacientes. Este estudo desvenda os detalhes de como a esclerostina desacelera a formação óssea e revela uma maneira de desativar seu freio nas células ósseas, preservando ao mesmo tempo seus papéis protetores no sistema cardiovascular.
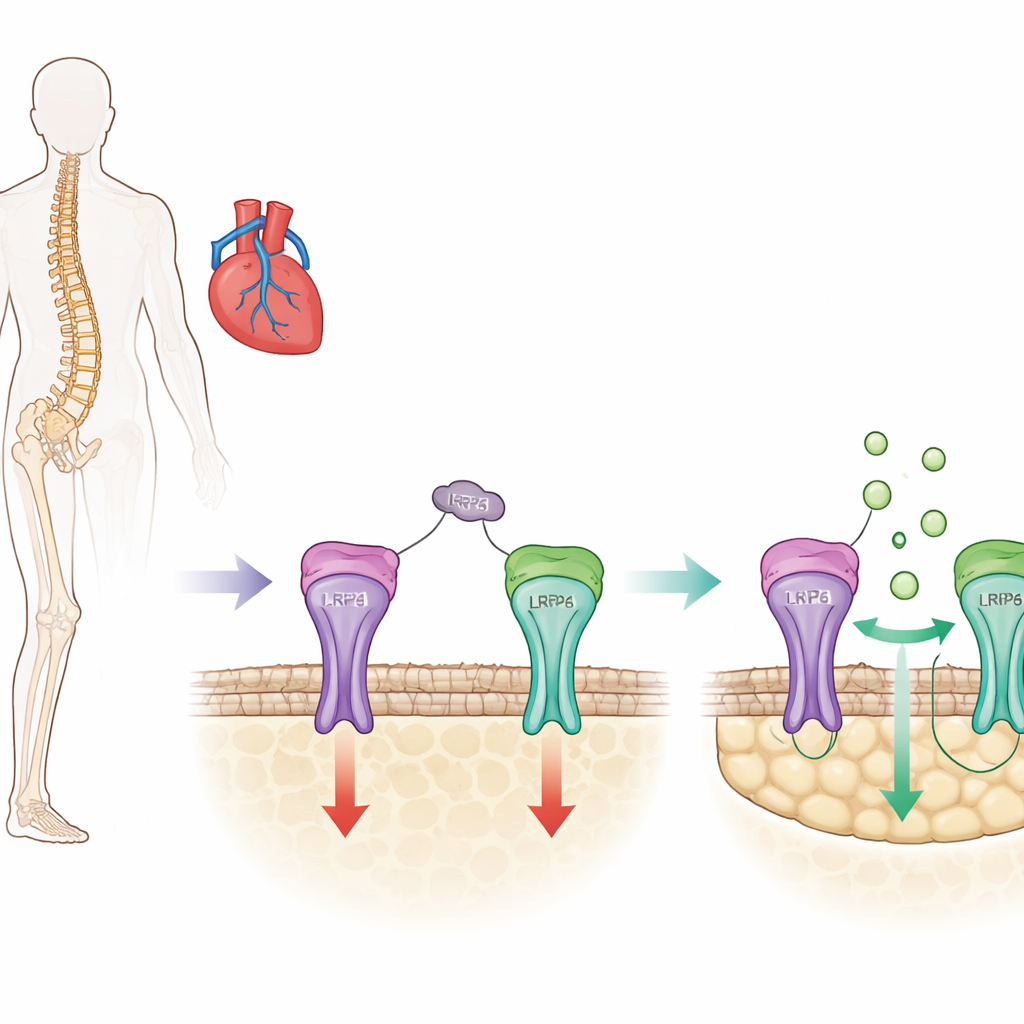
Um freio ósseo importante com um lado oculto
O osso é constantemente renovado: células especializadas constroem tecido novo enquanto outras removem material antigo. A esclerostina é uma proteína produzida principalmente por células ósseas que atua como um freio nesse processo, atenuando uma via promotora de crescimento conhecida como sinalização Wnt/β-catenina em células formadoras de osso (osteoblastos). Medicamentos atuais para osteoporose, como o romosozumabe, atuam bloqueando a esclerostina, levantando esse freio e aumentando rapidamente a massa óssea. No entanto, ensaios clínicos sugerem que o bloqueio amplo da esclerostina pode também perturbar funções protetoras em vasos sanguíneos e no coração, aumentando o risco de infarto e AVC em alguns indivíduos.
Aproximando-se de um loop minúsculo
A esclerostina tem três pequenas regiões em forma de laço em sua estrutura, e trabalhos anteriores deste grupo mostraram que uma delas, chamada loop3, ajuda a esclerostina a suprimir a formação óssea, mas não é necessária para seus efeitos protetores nos vasos. No presente estudo, os pesquisadores investigaram exatamente como o loop3 contribui para a inibição óssea. Eles descobriram que o loop3 se liga a um receptor na superfície das células ósseas chamado LRP4. Essa ligação age como uma âncora que posiciona a esclerostina para que ela possa alcançar outro receptor próximo, LRP6, que controla diretamente a via Wnt/β-catenina. Usando testes bioquímicos de ligação e modelagem computacional, eles identificaram aminoácidos específicos na proteína LRP4 que são pontos de contato essenciais para o loop3.
Quebrando a âncora para liberar o crescimento ósseo
Munidos desse entendimento estrutural, a equipe projetou duas abordagens para interromper a âncora loop3–LRP4: uma versão genética que alterou sutilmente os aminoácidos-chave em LRP4 (chamada Lrp4m) e um peptídeo sintético curto (LRP4-Pep) que imita a região de LRP4 que se liga ao loop3 e compete pela esclerostina. Em osteoblastos em cultura, ambas as estratégias enfraqueceram a capacidade da esclerostina de se ligar ao LRP6, reduziram sua supressão da sinalização Wnt/β-catenina e preservaram a capacidade das células de maturar e depositar mineral. Simulações computacionais corroboraram esse quadro, mostrando que o LRP4 normal mantém a esclerostina próximo ao LRP6, enquanto a forma mutada falha em estabilizar esse contato.
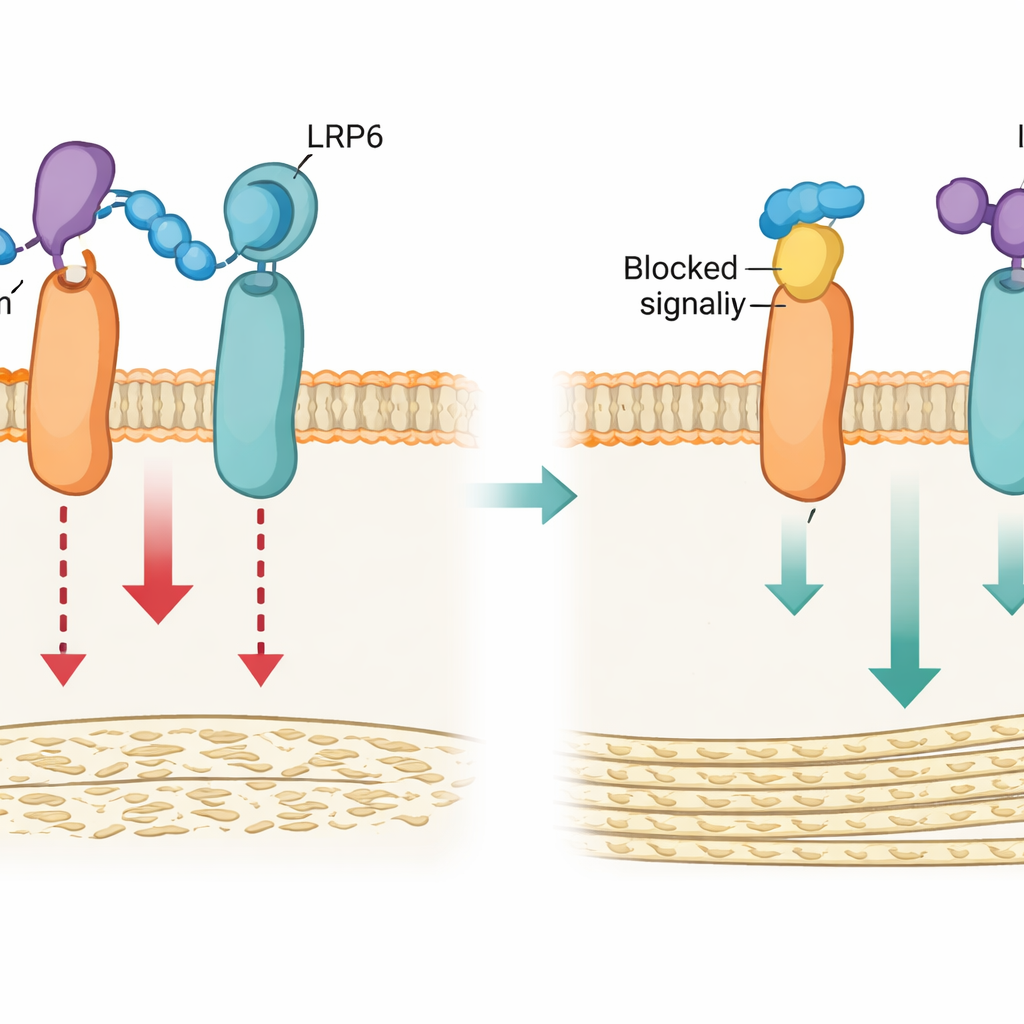
Ossos mais fortes em camundongos sem riscos adicionais
Os pesquisadores então avançaram para modelos murinos para confirmar que interromper a interação loop3–LRP4 melhora a saúde óssea em animais vivos. Camundongos portadores da mutação Lrp4m por todo o corpo desenvolveram ossos mais densos e fortes, com arquitetura interna melhorada e níveis sanguíneos mais altos de marcadores de formação óssea, sem dano mensurável ao músculo. Quando a mesma mutação estava presente em camundongos geneticamente desprovidos de esclerostina, não houve efeito adicional, mas a reintrodução de esclerostina mostrou que seu poder de suprimir os ossos era muito menor em animais Lrp4m. De maneira similar, em camundongos geneticamente projetados para superproduzir esclerostina ou em modelos com perda óssea relacionada à deficiência de estrogênio, o tratamento repetido com o peptídeo LRP4-Pep aumentou a massa óssea de forma dependente da dose, melhorou a qualidade óssea e aumentou a resistência mecânica, mas não teve efeito detectável quando a esclerostina estava ausente.
Rumo a terapias anabólicas ósseas mais seguras
Em conjunto, esses achados mostram que a interação entre o loop3 da esclerostina e LRP4 em osteoblastos é a âncora necessária para que a esclerostina se ligue ao LRP6 e desligue a formação óssea. Ao interromper seletivamente essa âncora — seja por mutações precisas ou por um peptídeo desenhado — os pesquisadores conseguiram estimular a construção óssea e a resistência em camundongos sem bloquear diretamente as partes da esclerostina que parecem importantes para a proteção cardiovascular. Para pacientes, esse trabalho aponta para uma nova geração de tratamentos para fortalecer os ossos que não visam silenciar a esclerostina por completo, mas dissociar seus efeitos no osso de seus papéis benéficos no coração e nos vasos sanguíneos.
Citação: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
Palavras-chave: osteoporose, esclerostina, formação óssea, LRP4, sinalização Wnt