Clear Sky Science · fr
Interaction boucle3-LRP4 ostéoblastique requise par la sclérostine pour inhiber la formation osseuse
Pourquoi la construction osseuse a besoin d’un interrupteur plus fin
La fragilité osseuse et les fractures deviennent une préoccupation croissante à mesure que la population vieillit, et de nouveaux médicaments puissants existent désormais pour stimuler la croissance osseuse. Pourtant, l’un de ces traitements — un anticorps qui bloque une protéine inhibitrice de l’os appelée sclérostine — a été associé à de graves problèmes cardiaques chez certains patients. Cette étude décrypte les détails fins de la manière dont la sclérostine ralentit la formation osseuse et révèle une façon de désactiver son frein dans les cellules osseuses tout en préservant ses rôles protecteurs dans le système cardiovasculaire.
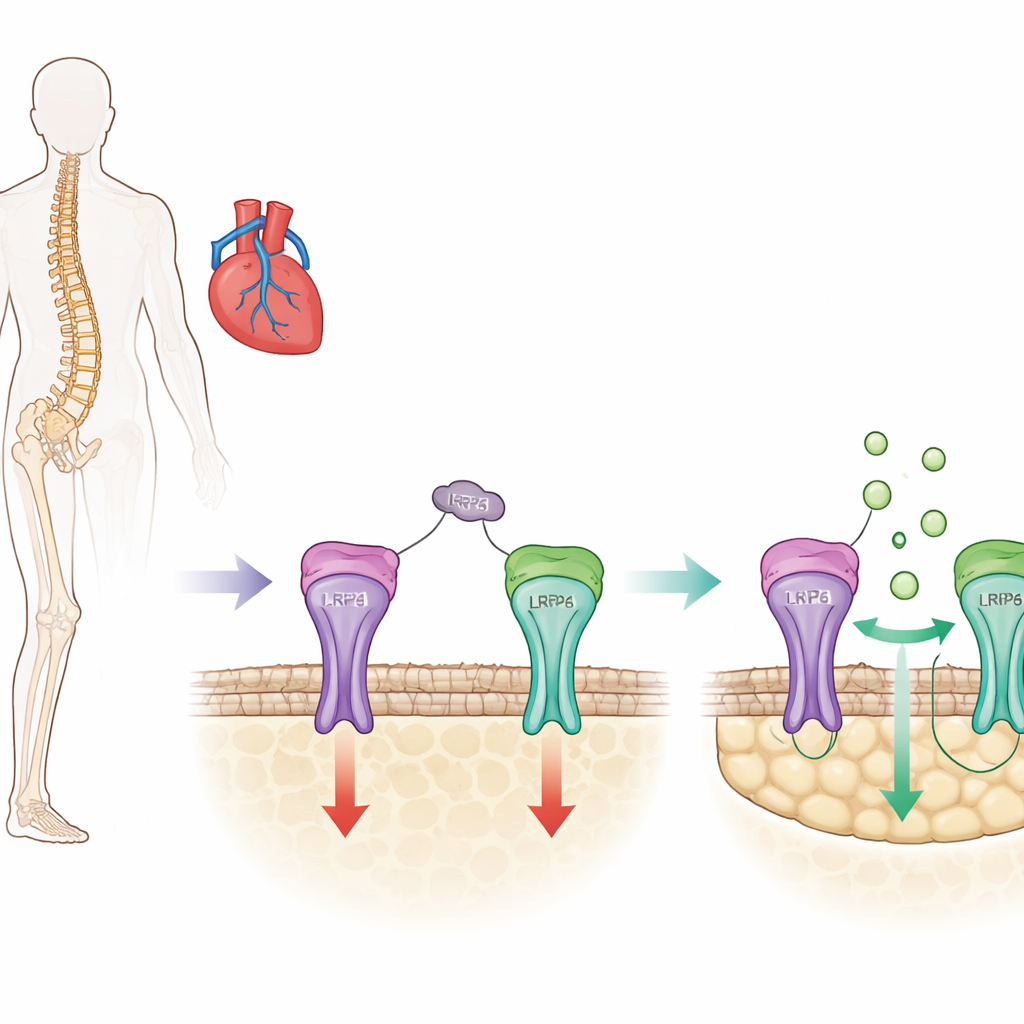
Un frein osseux clé avec un côté caché
L’os se renouvelle en permanence : des cellules spécialisées construisent du tissu neuf pendant que d’autres éliminent le matériau ancien. La sclérostine est une protéine produite principalement par les cellules osseuses qui agit comme un frein à ce processus de construction en atténuant une voie favorisant la croissance connue sous le nom de signalisation Wnt/β-caténine dans les ostéoblastes. Les traitements actuels contre l’ostéoporose, tels que le romosozumab, bloquent la sclérostine, lèvent ce frein et augmentent rapidement la masse osseuse. Cependant, des essais cliniques ont suggéré qu’un blocage large de la sclérostine pourrait aussi perturber ses fonctions protectrices dans les vaisseaux sanguins et le cœur, augmentant le risque d’infarctus et d’accident vasculaire cérébral chez certains individus.
Zoom sur une minuscule boucle
La sclérostine comporte trois petites régions en forme de boucle dans sa structure, et des travaux antérieurs de ce groupe ont montré que l’une d’elles, appelée boucle3, aide la sclérostine à supprimer la formation osseuse mais n’est pas nécessaire pour ses effets protecteurs dans les vaisseaux. Dans la présente étude, les chercheurs ont cherché à savoir précisément comment la boucle3 contribue à l’inhibition osseuse. Ils ont découvert que la boucle3 se lie à un récepteur à la surface des cellules osseuses appelé LRP4. Cette liaison agit comme une ancre qui positionne la sclérostine de sorte qu’elle puisse atteindre un autre récepteur voisin, LRP6, qui contrôle directement la voie Wnt/β-caténine. En utilisant des tests biochimiques de liaison et de la modélisation informatique, ils ont identifié des acides aminés spécifiques sur la protéine LRP4 qui sont des points de contact essentiels pour la boucle3.
Briser l’ancre pour libérer la croissance osseuse
Grâce à cette insight structurel, l’équipe a conçu deux types d’outils pour perturber l’ancre boucle3–LRP4 : une version génétique qui modifiait subtilement les acides aminés clés de LRP4 (appelée Lrp4m), et un court peptide synthétique (LRP4-Pep) qui imite la région de LRP4 qui se lie à la boucle3 et entre en compétition pour la sclérostine. Dans des ostéoblastes en culture, les deux stratégies ont affaibli la capacité de la sclérostine à se lier à LRP6, réduit sa suppression de la signalisation Wnt/β-caténine, et préservé la capacité des cellules à mûrir et à déposer du minéral. Les simulations informatiques ont confirmé ce tableau, montrant que LRP4 normal maintient la sclérostine près de LRP6, tandis que la forme mutée ne stabilise pas ce contact.
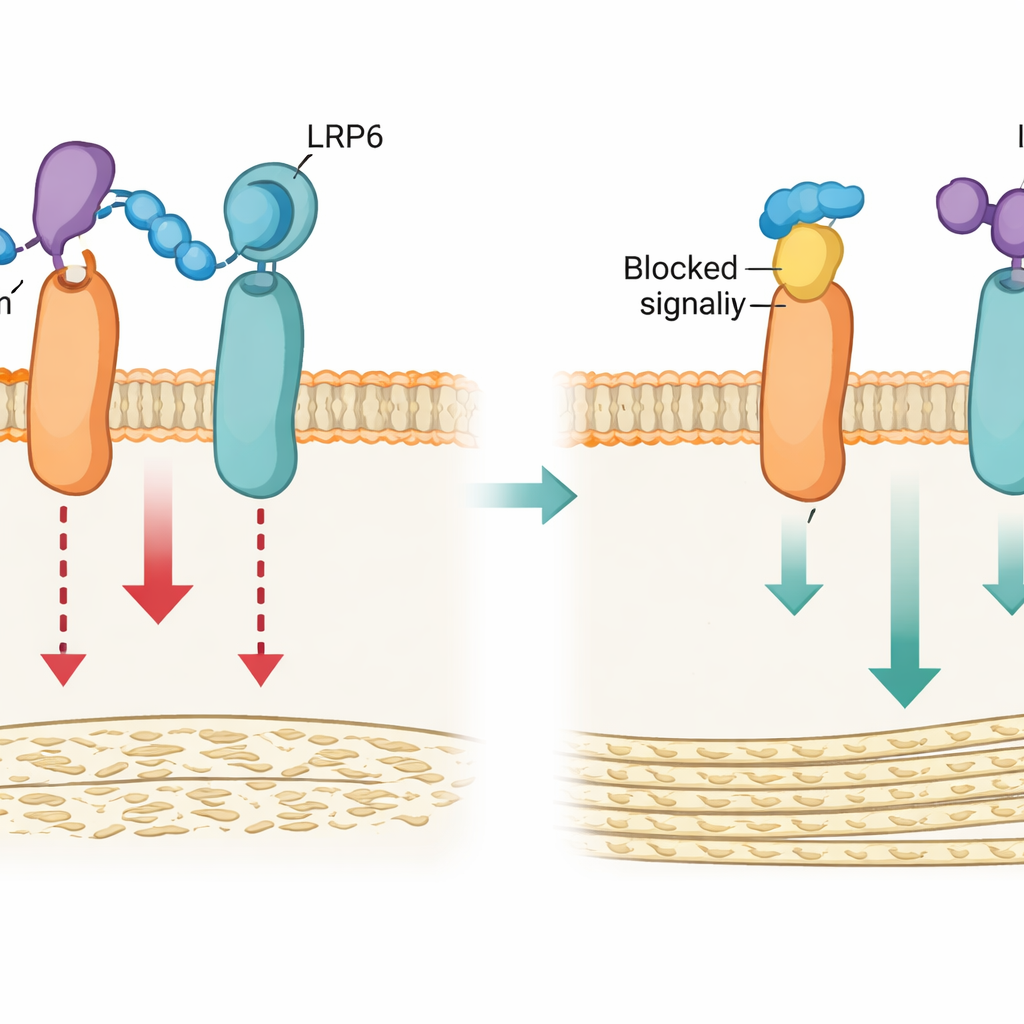
Des os plus solides chez la souris sans risques supplémentaires
Les chercheurs sont ensuite passés à des modèles murins pour confirmer que la perturbation de l’interaction boucle3–LRP4 améliore la santé osseuse in vivo. Les souris porteuses de la mutation Lrp4m dans tout l’organisme ont développé des os plus denses et plus solides, avec une architecture interne améliorée et des taux sanguins plus élevés de marqueurs de formation osseuse, sans atteinte musculaire mesurable. Lorsque la même mutation était présente chez des souris dépourvues génétiquement de sclérostine, il n’y avait pas d’effet additionnel, mais la réintroduction de la sclérostine montrait que son pouvoir suppressif sur l’os était beaucoup plus faible chez les animaux Lrp4m. De même, chez des souris conçues pour surproduire la sclérostine ou chez des souris ayant une perte osseuse liée à une carence en œstrogènes, des traitements répétés par le peptide LRP4-Pep augmentaient la masse osseuse de façon dépendante de la dose, amélioraient la qualité osseuse et renforçaient la résistance mécanique, sans effet détectable lorsque la sclérostine était absente.
Vers des thérapies anaboliques osseuses plus sûres
Pris ensemble, ces résultats montrent qu’une interaction entre la boucle3 de la sclérostine et LRP4 dans les ostéoblastes constitue l’ancre dont la sclérostine a besoin pour s’attacher à LRP6 et arrêter la formation osseuse. En perturbant sélectivement cette ancre — soit par des mutations précises, soit par un peptide sur mesure — les chercheurs ont pu stimuler la construction osseuse et la solidité chez la souris sans bloquer directement les parties de la sclérostine qui semblent importantes pour la protection cardiovasculaire. Pour les patients, ce travail ouvre la voie à une nouvelle génération de traitements renforçant l’os qui visent non pas à faire taire totalement la sclérostine, mais à dissocier ses effets sur l’os de ses rôles bénéfiques dans le cœur et les vaisseaux sanguins.
Citation: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
Mots-clés: ostéoporose, sclérostine, formation osseuse, LRP4, signalisation Wnt