Clear Sky Science · nl
Osteoblastische sclerostine lus3-LRP4-interactie vereist door sclerostine om botvorming te remmen
Waarom botopbouw een slimmer schakelaartje nodig heeft
Brosser wordende botten en breuken vormen een groeiende zorg nu mensen ouder worden, en er bestaan krachtige nieuwe geneesmiddelen die botgroei stimuleren. Toch is één zodanig middel — een antilichaam dat een botremmend eiwit genaamd sclerostine blokkeert — in verband gebracht met ernstige hartproblemen bij sommige patiënten. Deze studie werkt de fijne details uit van hoe sclerostine de botvorming vertraagt en laat zien hoe je de rem in botcellen kunt uitschakelen terwijl je de beschermende functies in het cardiovasculaire systeem behoudt.
Een belangrijke botrem met een verborgen kant
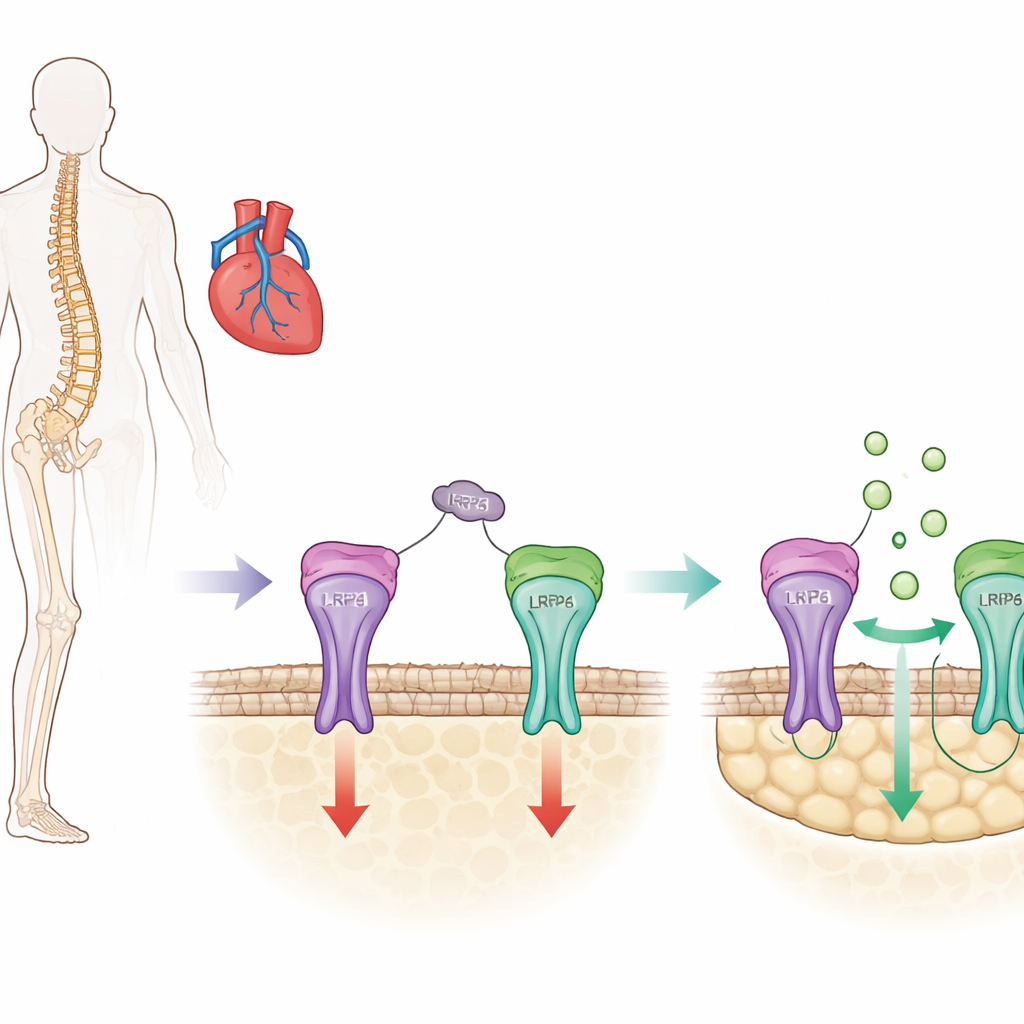
Bot wordt voortdurend vernieuwd doordat gespecialiseerde cellen nieuw weefsel opbouwen terwijl andere het oude verwijderen. Sclerostine is een eiwit dat vooral door botcellen wordt gemaakt en fungeert als een rem op dit opbouwproces door het groeibevorderende Wnt/β-cateninepad in botvormende cellen (osteoblasten) te onderdrukken. Huidige osteoporosemiddelen zoals romosozumab werken door sclerostine te blokkeren, waardoor deze rem wordt opgeheven en de botmassa snel toeneemt. Klinische onderzoeken suggereren echter dat brede blokkade van sclerostine ook beschermende functies in bloedvaten en het hart kan verstoren, en zo het risico op hartaanval en beroerte bij sommige mensen verhoogt.
Inzoomen op een klein lusje
Sclerostine heeft drie kleine lusvormige regio’s in zijn structuur, en eerder werk van deze groep toonde aan dat één daarvan, lus3 genoemd, helpt sclerostine botvorming te onderdrukken maar niet nodig is voor de beschermende effecten in bloedvaten. In de huidige studie onderzochten de onderzoekers precies hoe lus3 bijdraagt aan de botrem. Ze ontdekten dat lus3 bindt aan een receptor op het celoppervlak van botcellen genaamd LRP4. Deze binding werkt als een anker dat sclerostine positioneert zodat het een andere nabijgelegen receptor, LRP6, kan bereiken, die rechtstreeks het Wnt/β-cateninepad reguleert. Met biochemische bindingsproeven en computermodellering identificeerden ze specifieke aminozuren op het LRP4-eiwit die essentiële contactpunten voor lus3 vormen.
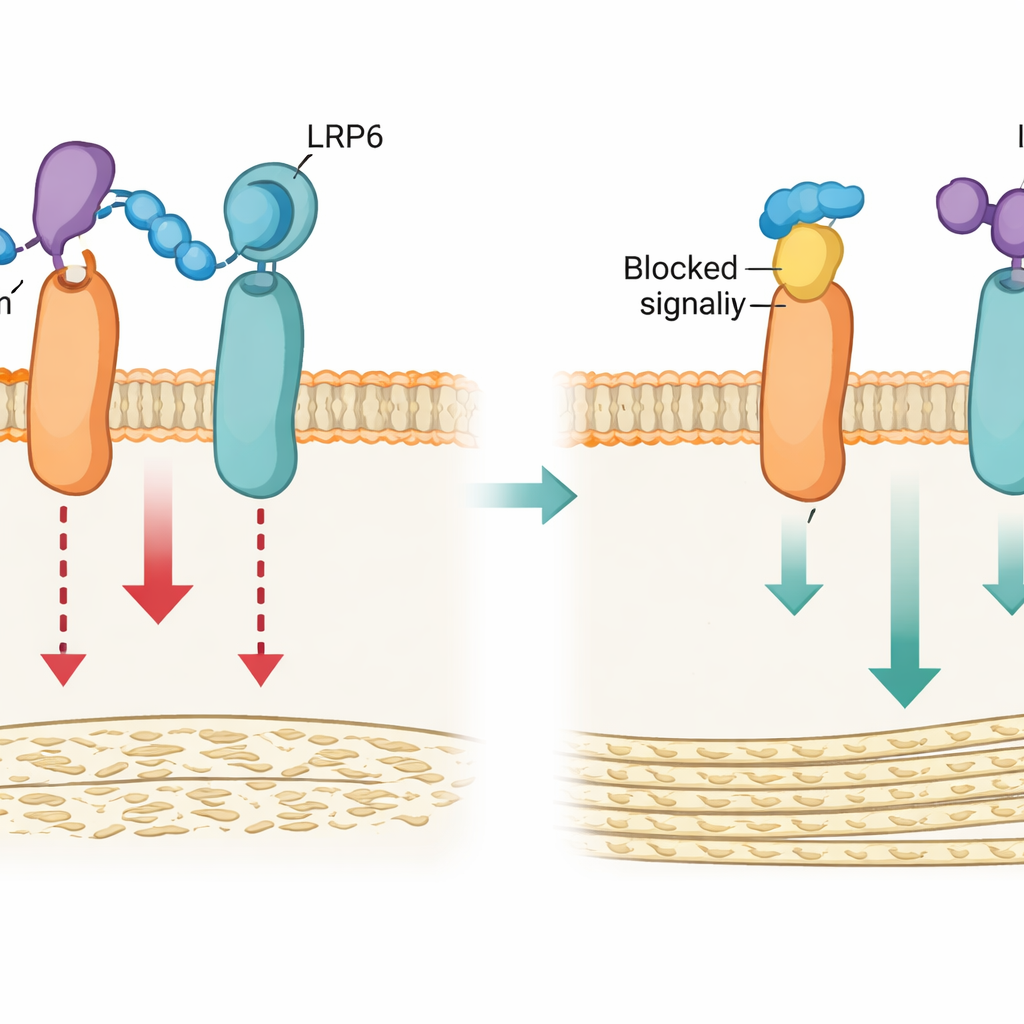
Het anker verbreken om botgroei vrij te geven
Gewapend met dit structurele inzicht ontwikkelde het team twee soorten middelen om het lus3–LRP4-anker te verstoren: een genetische variant die de sleutelaminozuren in LRP4 subtiel veranderde (genoemd Lrp4m), en een kort synthetisch peptide (LRP4-Pep) dat het lus3-bindende gebied van LRP4 nabootst en concurreert om sclerostine. In gekweekte osteoblasten verzwakten beide strategieën de mogelijkheid van sclerostine om aan LRP6 te binden, verminderden ze de onderdrukking van Wnt/β-catenine-signaalvoering, en behielden ze het vermogen van de cellen om te rijpen en mineraal te deponeren. Computersimulaties ondersteunden dit beeld: normale LRP4 houdt sclerostine dicht bij LRP6, terwijl de gemuteerde vorm dit contact niet stabiliseert.
Sterkere botten bij muizen zonder extra risico’s
De onderzoekers gingen vervolgens over naar muismodellen om te bevestigen dat het verstoren van de lus3–LRP4-interactie de botgezondheid in levende dieren verbetert. Muizen met de Lrp4m-mutatie in het hele lichaam ontwikkelden dichtere, sterkere botten, met verbeterde interne architectuur en hogere bloedspiegels van merkers voor botvorming, zonder meetbare schade aan spierweefsel. Wanneer dezelfde mutatie aanwezig was in muizen die genetisch geen sclerostine produceren, was er geen extra effect, maar het herintroduceren van sclerostine toonde dat de botonderdrukkende werking ervan veel zwakker was in Lrp4m-dieren. Evenzo verhoogde herhaalde behandeling met het LRP4-Pep-peptide, in muizen die teveel sclerostine produceerden of in muizen met gevestigde botverlies door oestrogeendeficiëntie, dosisafhankelijk de botmassa, verbeterde de botkwaliteit en vergrootte de mechanische sterkte — terwijl er geen detecteerbaar effect was wanneer sclerostine afwezig was.
Op weg naar veiligere bot-anabole therapieën
Samen laten deze bevindingen zien dat de interactie tussen sclerostine lus3 en LRP4 in osteoblasten het anker is dat sclerostine nodig heeft om zich aan LRP6 vast te klampen en botvorming af te schakelen. Door dit anker selectief te verstoren — hetzij via nauwkeurige mutaties of een doelgericht peptide — konden de onderzoekers botopbouw en -sterkte bij muizen verhogen zonder direct de delen van sclerostine te blokkeren die belangrijk lijken voor cardiovasculaire bescherming. Voor patiënten wijst dit werk op een nieuwe generatie botversterkende behandelingen die niet beogen sclerostine volledig te laten zwijgen, maar om zijn effecten in bot te ontkoppelen van zijn gunstige rollen in hart en bloedvaten.
Bronvermelding: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
Trefwoorden: osteoporose, sclerostine, botvorming, LRP4, Wnt-signaaltransductie