Clear Sky Science · ru
Взаимодействие ломтика 3 склеростина с LRP4 в остеобластах необходимо склеростину для подавления образования кости
Почему для наращивания кости нужен более умный переключатель
Хрупкие кости и переломы становятся всё более актуальной проблемой по мере увеличения продолжительности жизни, и сегодня существуют мощные препараты, стимулирующие рост кости. Однако один из таких препаратов — антитело, блокирующее белок‑ингибитор костеобразования склеростин — у некоторых пациентов связывают с серьёзными сердечно‑сосудистыми осложнениями. В этом исследовании подробно разобрали, как именно склеростин замедляет образование кости, и показали способ выключить его «тормоз» в клетках кости, сохранив при этом защитные функции этого белка в системе кровообращения.
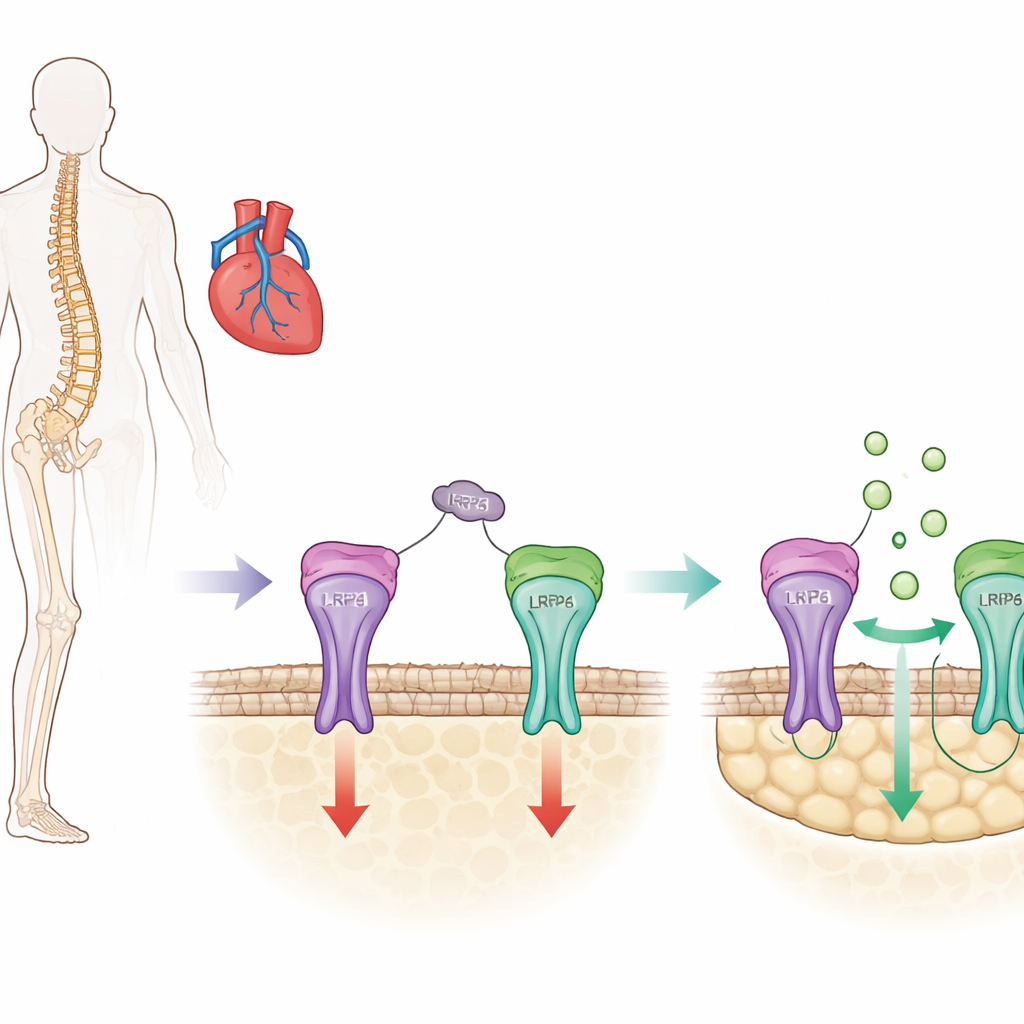
Ключевой костный «тормоз» с неожиданной стороной
Кость постоянно обновляется: специализированные клетки создают новую ткань, а другие удаляют старую. Склеростин — белок, в основном производимый клетками кости, — действует как тормоз этого процесса, снижая активность стимулирующего роста пути Wnt/β‑катенин в остеобластах (клетках, формирующих кость). Современные препараты при остеопорозе, такие как ромосозумаб, действуют путём блокирования склеростина, что приводит к снятию этого «тормоза» и быстрому увеличению массы кости. Однако клинические испытания показали, что широкая блокада склеростина может нарушать и его защитные функции в сосудах и сердце, повышая у некоторых пациентов риск инфаркта и инсульта.
Приближаемся к крошечной петле
У склеростина есть три небольших петельных региона в структуре, и предыдущие работы этой группы показали, что одна из них, называемая петлёй 3, помогает склеростину подавлять образование кости, но не нужна для его защитных эффектов в сосудах. В настоящем исследовании учёные выясняли, как именно петля 3 вносит вклад в ингибирование кости. Они обнаружили, что петля 3 связывается с рецептором на поверхности остеобласта — LRP4. Это связывание действует как якорь, который позиционирует склеростин так, чтобы он мог достать до другого соседнего рецептора, LRP6, непосредственно контролирующего путь Wnt/β‑катенин. С помощью биохимических тестов связывания и компьютерного моделирования они выделили конкретные аминокислоты в белке LRP4, являющиеся ключевыми контактными точками для петли 3.
Разорвать якорь, чтобы освободить рост кости
Овладев этой структурной информацией, команда создала два инструмента для нарушения связи петли 3 с LRP4: генетическую версию, которая тонко изменила ключевые аминокислоты в LRP4 (обозначенную Lrp4m), и короткий синтетический пептид (LRP4‑Pep), имитирующий область LRP4, связывающую петлю 3, и конкурирующий за связывание со склеростином. В культурах остеобластов обе стратегии ослабляли способность склеростина связываться с LRP6, уменьшали его подавление сигнального пути Wnt/β‑катенин и сохраняли способность клеток созревать и откладывать минерал. Компьютерные симуляции поддержали эту картину: нормальный LRP4 удерживает склеростин вблизи LRP6, тогда как мутантный вариант не стабилизирует этот контакт.
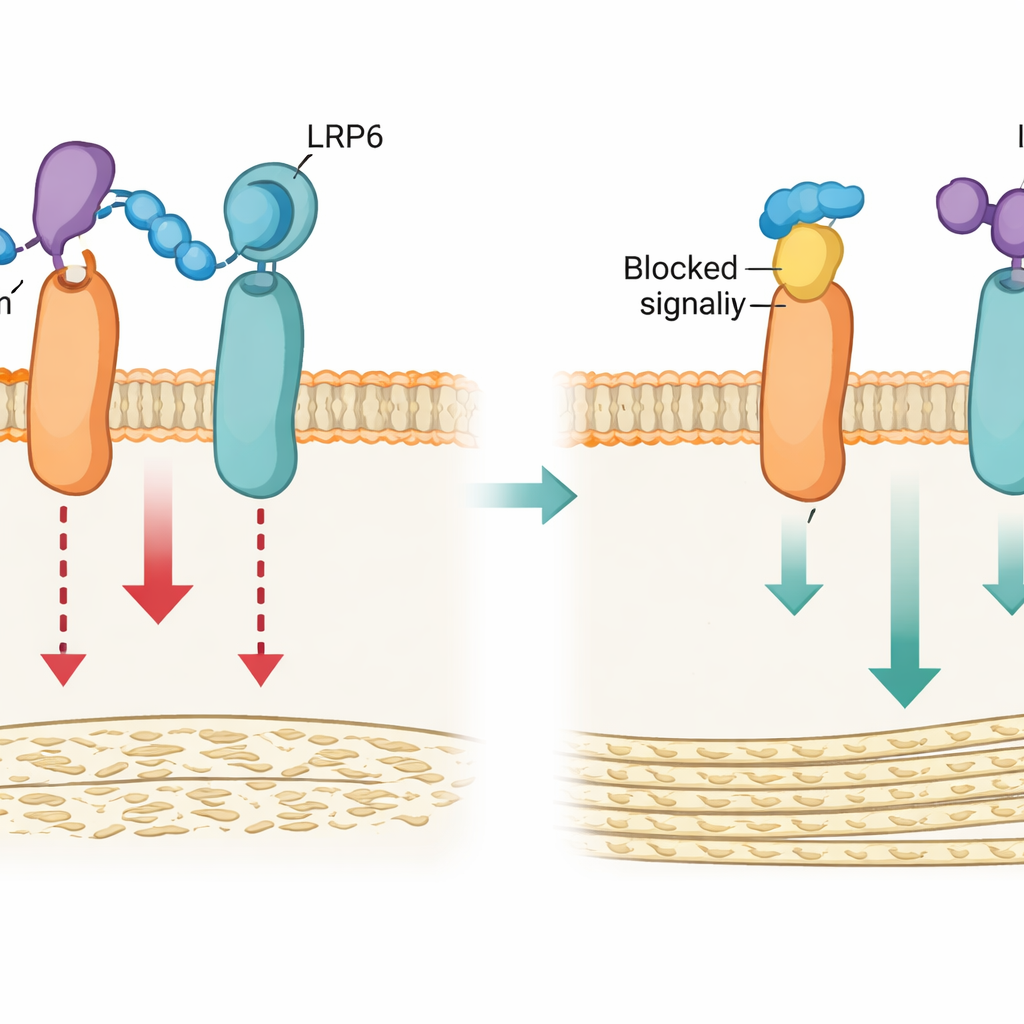
Крепче кости у мышей без дополнительных рисков
Затем исследователи перешли к моделям на мышах, чтобы подтвердить, что нарушение взаимодействия петли 3 с LRP4 улучшает состояние кости у живых животных. Мыши с мутацией Lrp4m по всему организму развивали более плотные, более прочные кости с улучшенной внутренней архитектурой и повышенным уровнем в крови маркеров костеобразования, без измеримого вреда мышцам. Когда та же мутация была в наличии у мышей, генетически лишённых склеростина, дополнительного эффекта не наблюдалось, но при повторном введении склеростина его способность подавлять кость была значительно ослаблена у животных с Lrp4m. Аналогично, у мышей, генетически перепроизводящих склеростин, или у животных с уже установленной потерей кости из‑за дефицита эстрогенов, многократное лечение пептидом LRP4‑Pep дозозависимо увеличивало массу кости, улучшало её качество и механическую прочность, но не оказывало заметного эффекта при отсутствии склеростина.
К шагу к более безопасным анэаболическим терапиям для костей
В сумме, эти данные показывают, что взаимодействие между петлёй 3 склеростина и LRP4 в остеобластах служит якорем, который необходим склеростину, чтобы подойти к LRP6 и выключить образование кости. Селективно нарушая этот якорь — либо через точные мутации, либо с помощью нацеленного пептида — исследователи смогли усилить формирование кости и её прочность у мышей, не блокируя напрямую те участки склеростина, которые, по всему видимому, важны для сердечно‑сосудистой защиты. Для пациентов это означает направление для нового поколения препаратов, усиливающих кость не путём полного подавления склеростина, а разъединяя его эффекты в кости от полезных ролей в сердце и сосудах.
Цитирование: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
Ключевые слова: остеопороз, склеростин, образование кости, LRP4, Wnt-сигнальный путь