Clear Sky Science · pl
Interakcja pętli 3 sclerostyny z LRP4 w osteoblastach wymagana, by sclerostyna hamowała tworzenie kości
Dlaczego budowanie kości potrzebuje mądrzejszego wyłącznika
Kruche kości i złamania stają się coraz większym problemem w miarę wydłużania się życia, a nowoczesne leki potrafią pobudzać wzrost kości. Jednak jeden z takich preparatów — przeciwciało blokujące białko hamujące kości, sclerostynę — wiązano u części pacjentów z poważnymi problemami sercowo-naczyniowymi. To badanie rozkłada na czynniki pierwsze mechanizm działania sclerostyny i pokazuje sposób, by wyłączyć jej hamulec w komórkach kości, zachowując jednocześnie jej ochronne role w układzie krążenia.
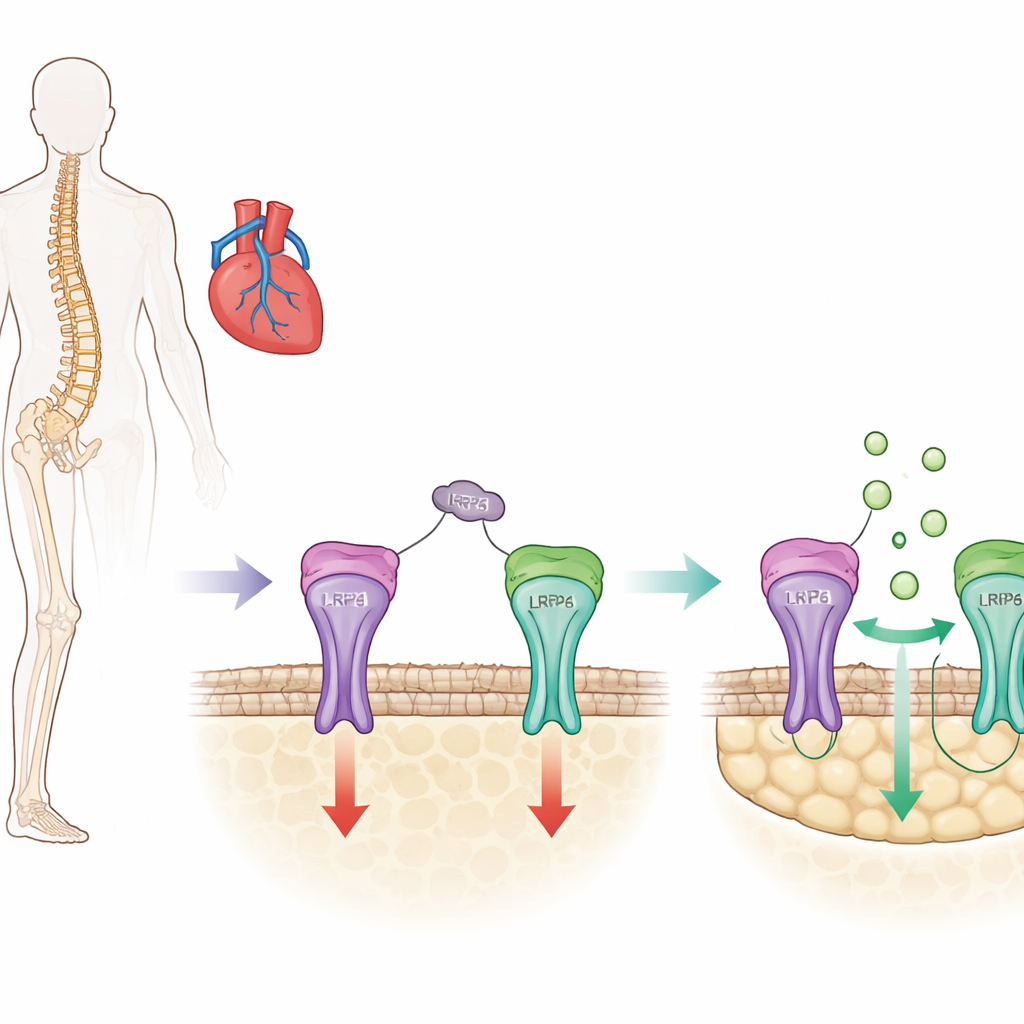
Kluczowy hamulec kości z ukrytą stroną
Kość jest nieustannie odnawiana: jedne wyspecjalizowane komórki wytwarzają nową tkankę, a inne usuwają starą. Sclerostyna to białko produkowane głównie przez komórki kostne, które działa jak hamulec tego procesu, tłumiąc szlak promujący wzrost znany jako sygnalizacja Wnt/β-katenina w komórkach tworzących kość (osteoblastach). Obecne leki na osteoporozę, takie jak romosozumab, blokują sclerostynę, podnosząc kurtynę tego hamulca i szybko zwiększając masę kostną. Jednak badania kliniczne sugerują, że szerokie blokowanie sclerostyny może także zaburzać jej ochronne funkcje w naczyniach krwionośnych i sercu, zwiększając u niektórych osób ryzyko zawału czy udaru.
Zbliżenie się do maleńkiej pętli
Sclerostyna ma w swojej strukturze trzy małe pętle, a wcześniejsze prace zespołu wykazały, że jedna z nich — nazwana pętlą 3 — pomaga sclerostynie tłumić tworzenie kości, ale nie jest potrzebna do jej ochronnych efektów w naczyniach. W obecnym badaniu naukowcy postawili pytanie, w jaki sposób pętla 3 przyczynia się do hamowania kości. Odkryli, że pętla 3 wiąże się z receptorem na powierzchni komórki kostnej zwanym LRP4. To wiązanie działa jak kotwica, pozycjonując sclerostynę tak, by mogła sięgnąć innego pobliskiego receptora, LRP6, który bezpośrednio kontroluje szlak Wnt/β-katenina. Dzięki testom biochemicznym i modelowaniu komputerowemu zidentyfikowali konkretne aminokwasy w białku LRP4, które stanowią istotne punkty kontaktu dla pętli 3.
Przerwanie kotwicy, uwolnienie wzrostu kości
Posiadając tę strukturalną wiedzę, zespół stworzył dwa rodzaje narzędzi do zakłócenia kotwicy pętla3–LRP4: wersję genetyczną, która subtelnie zmienia kluczowe aminokwasy w LRP4 (nazwaną Lrp4m), oraz krótki syntetyczny peptyd (LRP4-Pep) naśladujący region wiążący pętlę 3 w LRP4 i konkurujący o sclerostynę. W hodowlach osteoblastów obie strategie osłabiły zdolność sclerostyny do wiązania LRP6, zmniejszyły jej tłumienie sygnalizacji Wnt/β-katenina i zachowały zdolność komórek do dojrzewania i deponowania minerału. Symulacje komputerowe potwierdziły ten obraz: normalne LRP4 utrzymuje sclerostynę blisko LRP6, podczas gdy zmieniona forma nie stabilizuje tego kontaktu.
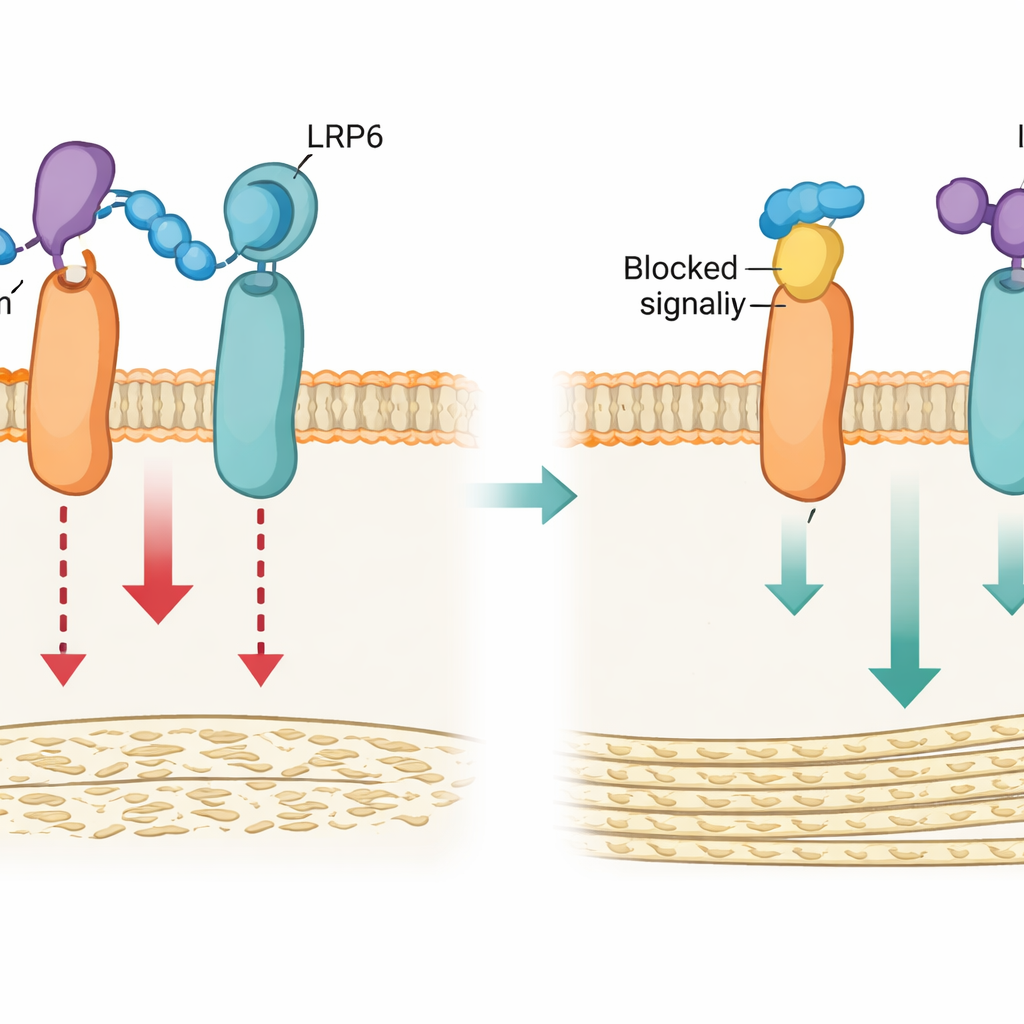
Mocniejsze kości u myszy bez dodatkowego ryzyka
Następnie badacze przeszli do modeli mysich, aby potwierdzić, że zakłócenie interakcji pętla3–LRP4 poprawia zdrowie kości in vivo. Myszy noszące mutację Lrp4m w całym organizmie rozwinęły gęstsze, silniejsze kości, z poprawioną architekturą wewnętrzną i wyższymi poziomami markerów tworzenia kości we krwi, bez wykrywalnych szkód dla mięśni. Gdy ta sama mutacja występowała u myszy genetycznie pozbawionych sclerostyny, nie obserwowano dodatkowego efektu, ale przy ponownym wprowadzeniu sclerostyny jej zdolność do tłumienia kości była znacznie osłabiona u zwierząt Lrp4m. Podobnie u myszy inżynierowanych do nadprodukcji sclerostyny lub u myszy z utratą kości związaną z niedoborem estrogenu, powtarzane leczenie peptydem LRP4-Pep zwiększało masę kostną, poprawiało jakość kości i wzmacniało wytrzymałość mechaniczną w sposób zależny od dawki, jednak nie wywoływało efektu, gdy sclerostyny brakowało.
W kierunku bezpieczniejszych terapii anabolicznych kości
Łącznie te wyniki pokazują, że interakcja między pętlą 3 sclerostyny a LRP4 w osteoblastach stanowi kotwicę, której sclerostyna potrzebuje, by dosięgnąć LRP6 i wyłączyć tworzenie kości. Poprzez selektywne zerwanie tej kotwicy — albo przez precyzyjne mutacje, albo poprzez dopasowany peptyd — badacze mogli zwiększyć budowę i wytrzymałość kości u myszy, nie blokując bezpośrednio części sclerostyny, które wydają się ważne dla ochrony sercowo-naczyniowej. Dla pacjentów praca ta wskazuje na nową generację terapii wzmacniających kości, które nie mają na celu całkowitego wyciszenia sclerostyny, lecz rozdzielenie jej efektów w kości od korzystnych ról w sercu i naczyniach krwionośnych.
Cytowanie: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
Słowa kluczowe: osteoporoza, sclerostyna, tworzenie kości, LRP4, szlak Wnt