Clear Sky Science · es
Bucle 3 de la interacción esclerostina-LRP4 en osteoblastos necesario para que la esclerostina inhiba la formación ósea
Por qué la construcción ósea necesita un interruptor más inteligente
Los huesos frágiles y las fracturas son una preocupación creciente a medida que la gente vive más tiempo, y ya existen fármacos potentes que estimulan el crecimiento óseo. Sin embargo, uno de esos medicamentos —un anticuerpo que bloquea una proteína que inhibe el hueso llamada esclerostina— se ha asociado con problemas cardíacos graves en algunos pacientes. Este estudio desentraña los detalles finos de cómo la esclerostina frena la formación ósea y revela una forma de desconectar su freno en las células óseas preservando al mismo tiempo sus funciones protectoras en el sistema cardiovascular.
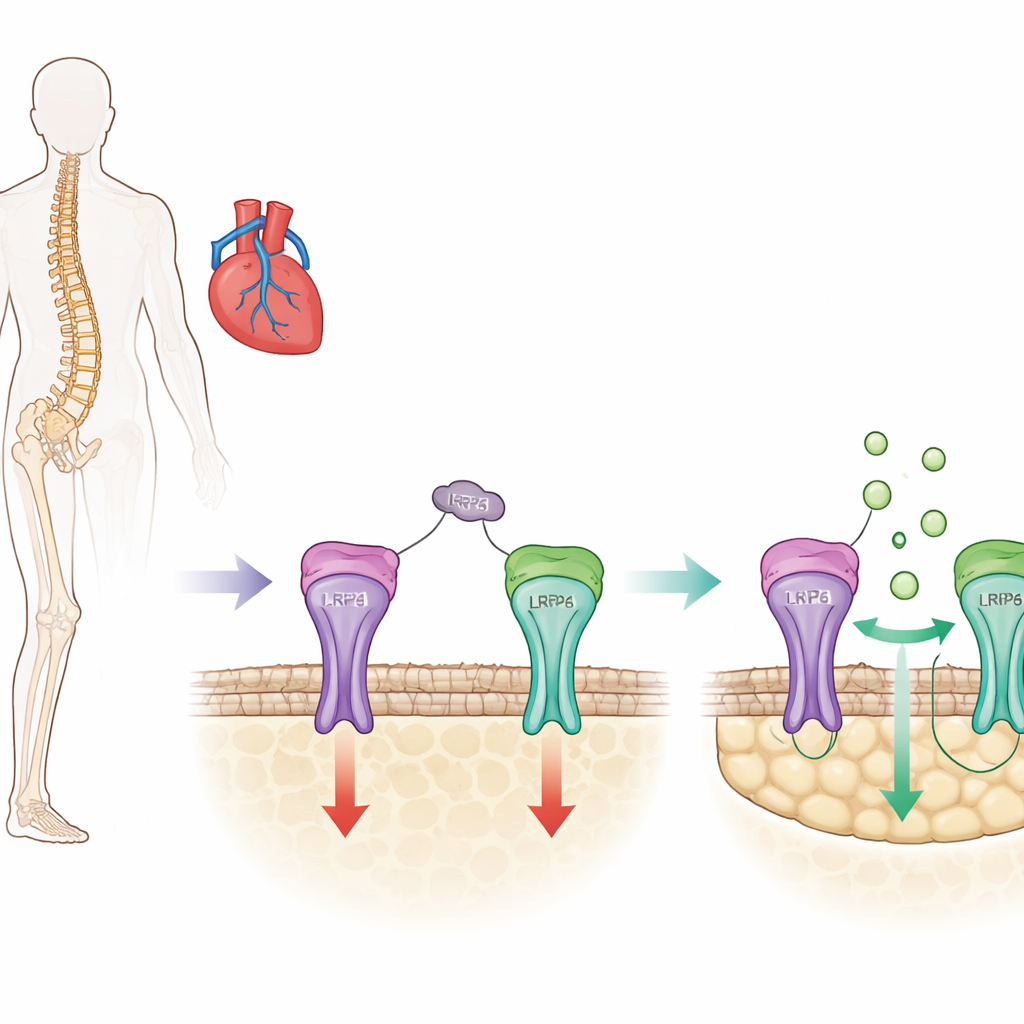
Un freno clave del hueso con un lado oculto
El hueso se renueva constantemente: células especializadas construyen tejido nuevo mientras otras eliminan el material viejo. La esclerostina es una proteína producida principalmente por células óseas que actúa como un freno de este proceso al atenuar una vía promotora del crecimiento conocida como señalización Wnt/β-catenina en las células formadoras de hueso (osteoblastos). Fármacos actuales para la osteoporosis, como el romosozumab, actúan bloqueando la esclerostina, levantando ese freno y aumentando rápidamente la masa ósea. No obstante, los ensayos clínicos han sugerido que un bloqueo amplio de la esclerostina también puede alterar funciones protectoras en los vasos sanguíneos y el corazón, incrementando el riesgo de infarto y accidente cerebrovascular en algunos individuos.
Acercando la lupa a un pequeño bucle
La esclerostina tiene tres pequeñas regiones en forma de bucle en su estructura, y trabajos previos de este grupo mostraron que una de ellas, llamada bucle3, ayuda a la esclerostina a suprimir la formación ósea pero no es necesaria para sus efectos protectores en los vasos sanguíneos. En el presente estudio, los investigadores preguntaron exactamente cómo contribuye el bucle3 a la inhibición ósea. Descubrieron que el bucle3 se une a un receptor en la superficie de las células óseas llamado LRP4. Esta unión actúa como un ancla que posiciona la esclerostina de modo que pueda alcanzar otro receptor cercano, LRP6, que controla directamente la vía Wnt/β-catenina. Mediante ensayos bioquímicos de unión y modelado por ordenador, identificaron aminoácidos específicos en la proteína LRP4 que son puntos de contacto esenciales para el bucle3.
Romper el ancla para liberar el crecimiento óseo
Con esta visión estructural, el equipo diseñó dos tipos de herramientas para interrumpir el ancla bucle3–LRP4: una versión genética que alteraba sutilmente los aminoácidos clave en LRP4 (denominada Lrp4m), y un péptido sintético corto (LRP4-Pep) que imita la región de LRP4 que se une al bucle3 y compite por la esclerostina. En osteoblastos en cultivo, ambas estrategias debilitaron la capacidad de la esclerostina para unirse a LRP6, redujeron su supresión de la señalización Wnt/β-catenina, y preservaron la capacidad de las células para madurar y depositar mineral. Las simulaciones por ordenador apoyaron este panorama, mostrando que LRP4 normal mantiene la esclerostina cerca de LRP6, mientras que la forma mutada no estabiliza este contacto.
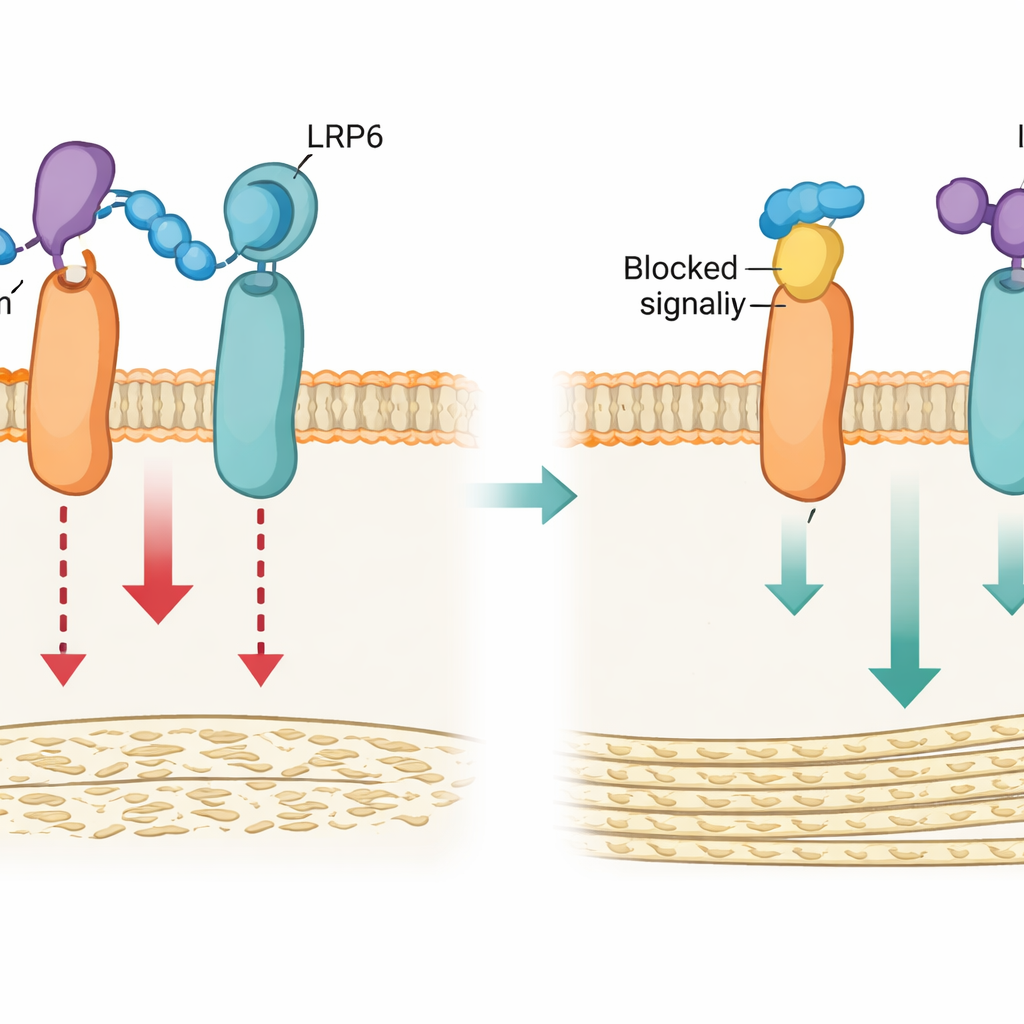
Huesos más fuertes en ratones sin riesgos añadidos
Los investigadores pasaron luego a modelos de ratón para confirmar que interrumpir la interacción bucle3–LRP4 mejora la salud ósea en animales vivos. Los ratones portadores de la mutación Lrp4m en todo el organismo desarrollaron huesos más densos y fuertes, con una arquitectura interna mejorada y niveles sanguíneos más altos de marcadores de formación ósea, sin daño medible en el músculo. Cuando la misma mutación estuvo presente en ratones que carecen genéticamente de esclerostina, no hubo un efecto adicional, pero al reintroducir esclerostina se observó que su capacidad para suprimir el hueso era mucho más débil en animales Lrp4m. De igual modo, en ratones diseñados para sobreproducir esclerostina o en ratones con pérdida ósea establecida relacionada con deficiencia de estrógenos, el tratamiento repetido con el péptido LRP4-Pep aumentó la masa ósea de forma dependiente de la dosis, mejoró la calidad ósea y la resistencia mecánica, sin impacto detectable cuando la esclerostina estaba ausente.
Hacia terapias anabólicas óseas más seguras
En conjunto, estos hallazgos muestran que la interacción entre el bucle3 de la esclerostina y LRP4 en osteoblastos es el ancla que la esclerostina necesita para engancharse a LRP6 y cerrar la formación ósea. Al interrumpir selectivamente este ancla —ya sea mediante mutaciones precisas o un péptido diseñado—, los investigadores pudieron potenciar la construcción ósea y la resistencia en ratones sin bloquear directamente las partes de la esclerostina que parecen importantes para la protección cardiovascular. Para los pacientes, este trabajo apunta a una nueva generación de tratamientos fortalecedores del hueso que no buscan silenciar la esclerostina por completo, sino separar sus efectos en el hueso de sus roles beneficiosos en el corazón y los vasos sanguíneos.
Cita: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
Palabras clave: osteoporosis, esclerostina, formación ósea, LRP4, señalización Wnt