Clear Sky Science · it
Interazione loop3-LRP4 osteoblastica di sclerostina necessaria perché la sclerostina inibisca la formazione ossea
Perché la costruzione dell’osso ha bisogno di un interruttore più intelligente
Le ossa fragili e le fratture sono una preoccupazione crescente man mano che le persone vivono più a lungo, e oggi esistono farmaci potenti per stimolare la crescita ossea. Tuttavia, uno di questi medicinali — un anticorpo che blocca una proteina inibitrice dell’osso chiamata sclerostina — è stato collegato a gravi problemi cardiaci in alcuni pazienti. Questo studio analizza i dettagli di come la sclerostina rallenti la formazione ossea e rivela un modo per disattivare il suo freno nelle cellule ossee preservandone al contempo i ruoli protettivi nel sistema cardiovascolare.
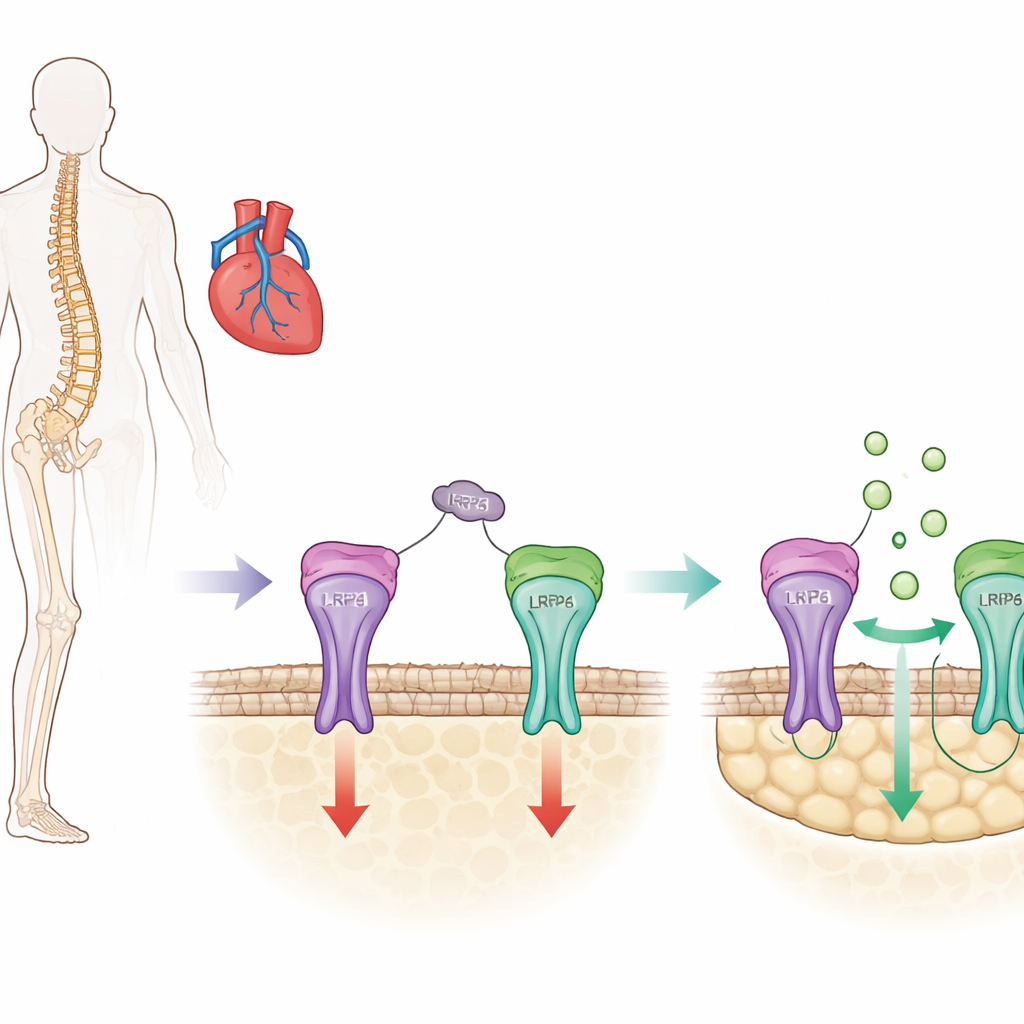
Un freno chiave dell’osso con un lato nascosto
L’osso si rinnova costantemente: cellule specializzate costruiscono nuovo tessuto mentre altre rimuovono il materiale vecchio. La sclerostina è una proteina prodotta principalmente dalle cellule ossee che agisce come un freno su questo processo di costruzione attenuando una via di crescita nota come segnalazione Wnt/β-catenina nelle cellule che formano l’osso (osteoblasti). Farmaci per l’osteoporosi attuali, come il romosozumab, agiscono bloccando la sclerostina, sollevando questo freno e aumentando rapidamente la massa ossea. Tuttavia, gli studi clinici hanno suggerito che un blocco ampio della sclerostina può anche disturbare funzioni protettive nei vasi sanguigni e nel cuore, aumentando il rischio di infarto e ictus in alcuni individui.
Zoom su un anellino minuscolo
La sclerostina presenta tre piccole regioni ad anello nella sua struttura, e lavori precedenti di questo gruppo hanno mostrato che una di esse, chiamata loop3, aiuta la sclerostina a sopprimere la formazione ossea ma non è necessaria per i suoi effetti protettivi nei vasi. Nel presente studio i ricercatori hanno chiesto esattamente come il loop3 contribuisca all’inibizione ossea. Hanno scoperto che loop3 si lega a un recettore sulla superficie delle cellule ossee chiamato LRP4. Questo legame funge da ancora che posiziona la sclerostina in modo che possa raggiungere un altro recettore vicino, LRP6, che controlla direttamente la via Wnt/β-catenina. Attraverso test biochimici di legame e modellizzazione al computer, hanno identificato specifici amminoacidi sulla proteina LRP4 che sono punti di contatto essenziali per loop3.
Spezzare l’ancora per liberare la crescita ossea
Con questa intuizione strutturale, il team ha progettato due strumenti per interrompere l’ancora loop3–LRP4: una versione genetica che alterava in modo sottile gli amminoacidi chiave in LRP4 (chiamata Lrp4m), e un breve peptide sintetico (LRP4-Pep) che imita la regione di LRP4 che lega loop3 e compete per la sclerostina. Negli osteoblasti coltivati, entrambe le strategie hanno indebolito la capacità della sclerostina di legarsi a LRP6, ridotto la sua soppressione della segnalazione Wnt/β-catenina e preservato la capacità delle cellule di maturare e depositare minerali. Le simulazioni al computer hanno confermato questo quadro, mostrando che il LRP4 normale trattiene la sclerostina vicino a LRP6, mentre la forma mutata non riesce a stabilizzare questo contatto.
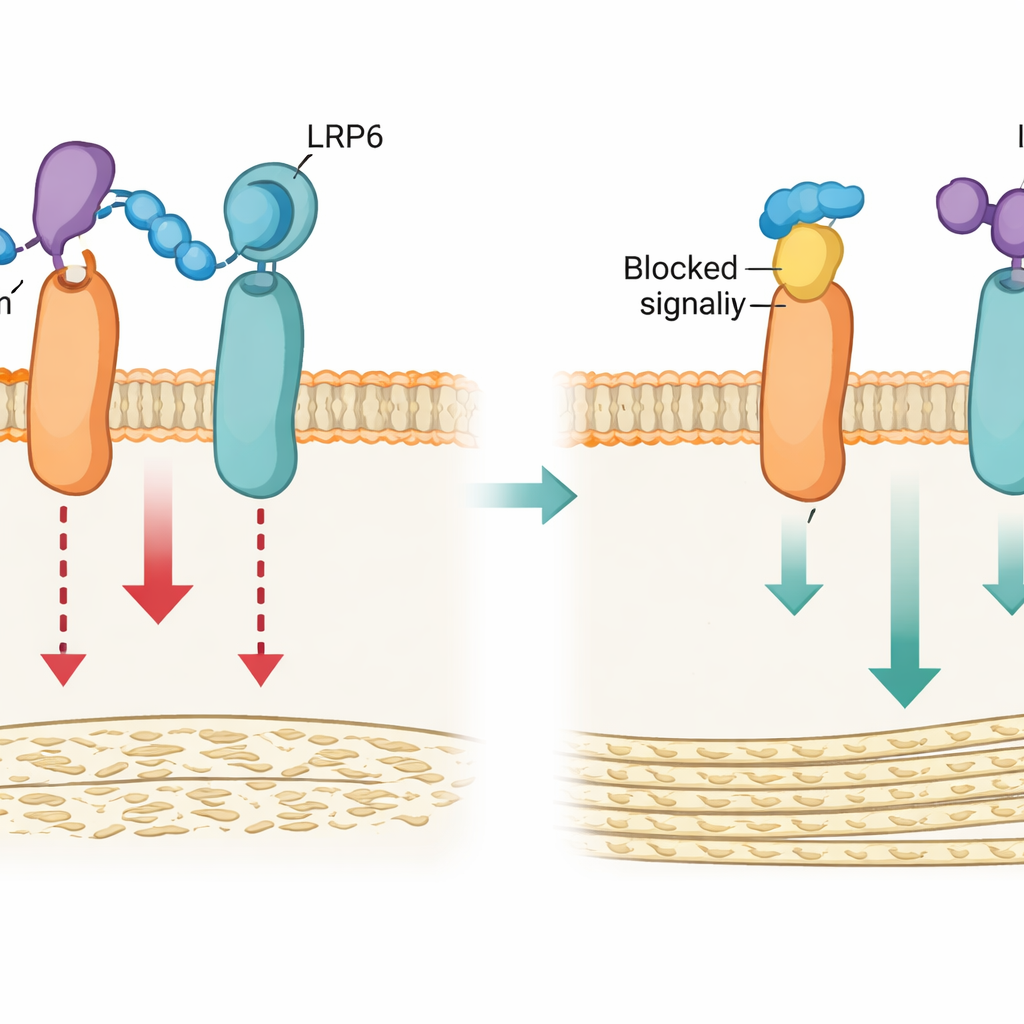
Ossa più robuste nei topi senza rischi aggiuntivi
I ricercatori sono poi passati a modelli murini per confermare che interrompere l’interazione loop3–LRP4 migliora la salute ossea in animali vivi. I topi portatori della mutazione Lrp4m in tutto l’organismo hanno sviluppato ossa più dense e più forti, con un’architettura interna migliorata e livelli ematici più alti di marcatori di formazione ossea, senza danni misurabili al muscolo. Quando la stessa mutazione era presente in topi privi geneticamente di sclerostina, non si osservava un effetto aggiuntivo, ma la reintroduzione di sclerostina ha mostrato che il suo potere soppressivo sull’osso era molto più debole negli animali Lrp4m. Allo stesso modo, in topi ingegnerizzati per sovraprodurre sclerostina o in topi con perdita ossea correlata a carenza di estrogeni, trattamenti ripetuti con il peptide LRP4-Pep hanno aumentato la massa ossea in modo dose-dipendente, migliorato la qualità ossea e la resistenza meccanica, pur non avendo impatto rilevabile quando la sclerostina era assente.
Verso terapie anaboliche ossee più sicure
Nel complesso, questi risultati mostrano che l’interazione tra il loop3 della sclerostina e LRP4 negli osteoblasti è l’ancora necessaria affinché la sclerostina si leghi a LRP6 e spenga la formazione ossea. Disgregando selettivamente quest’ancora — sia tramite mutazioni mirate sia con un peptide su misura — i ricercatori sono riusciti ad aumentare la costruzione e la forza ossea nei topi senza bloccare direttamente le parti della sclerostina che sembrano importanti per la protezione cardiovascolare. Per i pazienti, questo lavoro indica una nuova generazione di terapie per rafforzare l’osso che non mirano a silenziare completamente la sclerostina, ma a separarne gli effetti nell’osso dai ruoli benefici nel cuore e nei vasi sanguigni.
Citazione: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
Parole chiave: osteoporosi, sclerostina, formazione ossea, LRP4, segnalazione Wnt