Clear Sky Science · he
האינטראקציה של סקלרוסטין לופ3-LRP4 בתאי האוסטאובלסטים נחוצה לסקלרוסטין כדי לעכב בניית עצם
מדוע בניית עצם זקוקה למתג חכם יותר
עצמות שבריריות ושברים מהווים דאגה גוברת ככל שאנשים חיים זמן רב יותר, וכבר קיימות תרופות חזקות שמעודדות גדילת עצם. יחד עם זאת, אחת מהתרופות — נוגדן החוסם חלבון מעכב עצם הנקרא סקלרוסטין — נקשרה לבעיות לב חמורות בחלק מהחולים. המחקר הזה מפענח את הפרטים הדקים של האופן שבו סקלרוסטין מאט את בניית העצם ומראה דרך לכבות את הבלם בתאי העצם תוך שמירה על תפקידיו המגנים במערכת כלי הדם והלב.
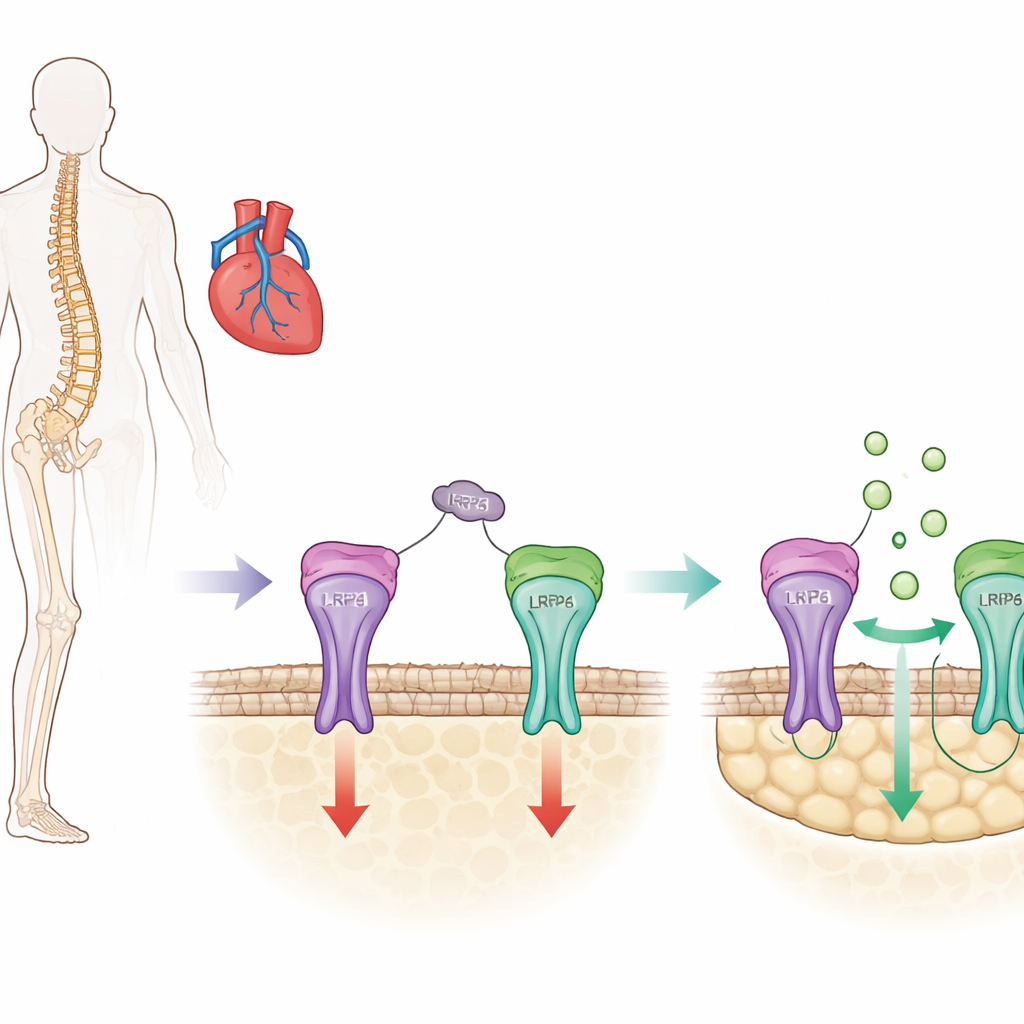
בלם עצם מרכזי עם צד נסתר
העצם מתחדשת כל הזמן כאשר תאים מתמחים בונים רקמה חדשה בעוד אחרים מסירים חומר ישן. סקלרוסטין הוא חלבון שמיוצר בעיקר על ידי תאי עצם ופועל כבלם על תהליך הבנייה על ידי דיכוי מסלול מקדם גדילה הידוע כאיתות Wnt/β-catenin בתאי בוני העצם (אוסטאובלסטים). תרופות לטיפול באוסטאופורוזיס כמו רומוסוזומאב פועלות על ידי חסימת סקלרוסטין, הרמת הבלם והגדלה מהירה של מסת העצם. עם זאת, ניסויים קליניים הצביעו על כך שחסימה נרחבת של סקלרוסטין עלולה גם לשבש פונקציות מגן בכלי דם ולב, ולהעלות בסיכון התקף לב ושבץ בחלק מהאנשים.
התמקדות בלולאה זעירה
לסקלרוסטין יש שלוש אזורי לולאה קטנטנים במבנה שלו, ועבודות קודמות של הקבוצה הראו שאחת מהן, המכונה לופ3, מסייעת לסקלרוסטין לדכא בניית עצם אך אינה דרושה לפעולותיו המגנות בכלי הדם. במחקר הנוכחי שאלו החוקרים בדיוק כיצד לופ3 תורמת לעיכוב העצם. הם גילו שלופ3 נקשרת לקולטן על פני התא האוסטאובלסטי הנקרא LRP4. קשירה זו פועלת כעוגן שממקם את הסקלרוסטין כך שיוכל להגיע לקולטן סמוך אחר, LRP6, שמווסת ישירות את מסלול Wnt/β-catenin. באמצעות בדיקות קשירה ביוכימיות ודגמי מחשב הם זיהו חומצות אמינו ספציפיות בחלבון LRP4 שהן נקודות מגע חיוניות ללופ3.
שבירת העוגן כדי לשחרר צמיחת עצם
מצוידים בתובנה מבנית זו, הצוות הנדס שתי אסטרטגיות לשבש את העוגן לופ3–LRP4: גרסה גנטית ששינתה בעדינות את חומצות האמינו המרכזיות ב-LRP4 (נקראת Lrp4m), ופפטיד סינטטי קצר (LRP4-Pep) שמחקה את אזור הקשירה של LRP4 ומתחרה על קשירת סקלרוסטין. בתאי אוסטאובלסטים בתרבית, שתי האסטרטגיות החלישו את יכולת הסקלרוסטין להיקשר ל-LRP6, הפחיתו את דיכוי איתות Wnt/β-catenin ושמרו על יכולת התאים להבשיל ולהטיל מינרל. סימולציות מחשב תמכו בתמונה הזו והראו ש-LRP4 רגיל מחזיק את סקלרוסטין קרוב ל-LRP6, בעוד שהצורה המוטנטית אינה מצליחה לייצב את המגע הזה.
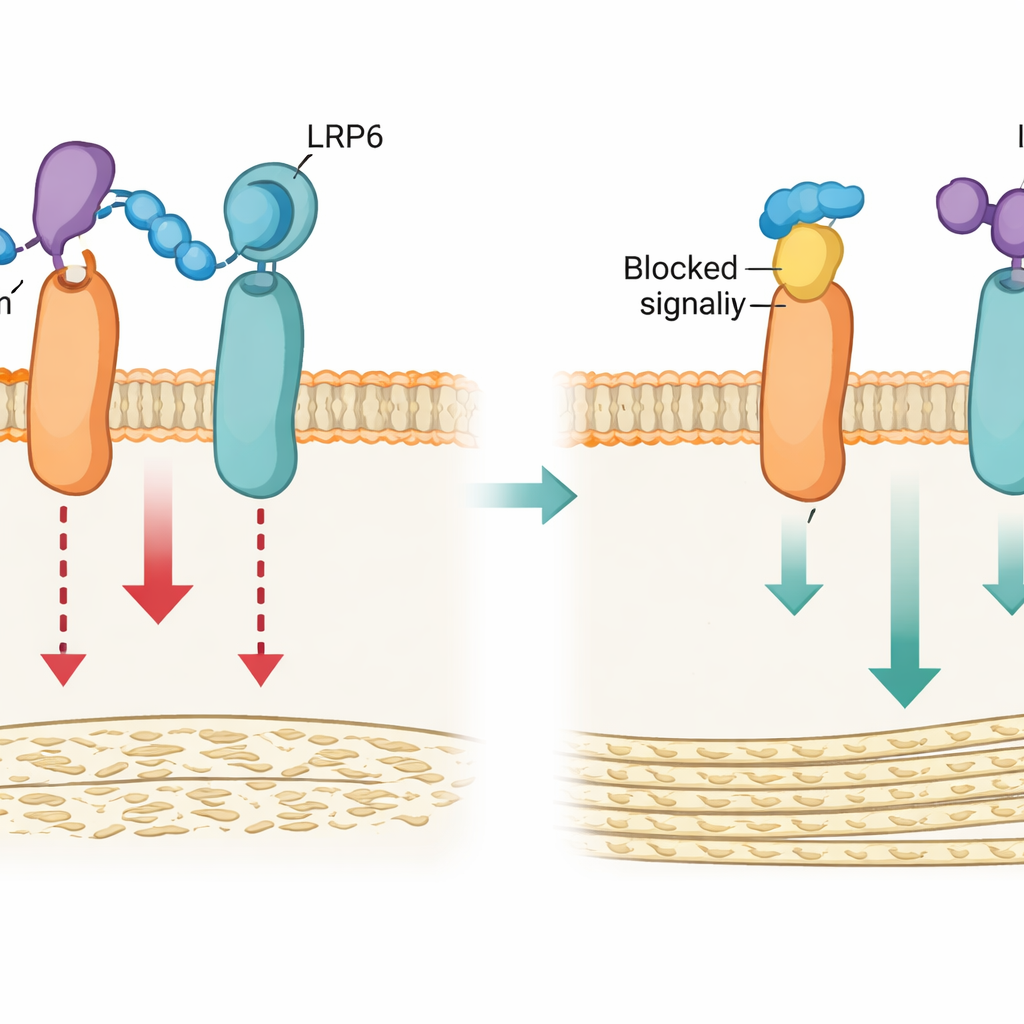
עצמות חזקות יותר בעכברים ללא סיכונים נוספים
בהמשך הועברו הניסויים למדגמי עכבר כדי לאשר ששיבוש האינטראקציה לופ3–LRP4 משפר את בריאות העצם בחיות חיות. עכברים שנשאבו את המוטציה Lrp4m בכל רקמות הגוף פיתחו עצמות צפופות וחזקות יותר, עם ארכיטקטורה פנימית משופרת ורמות דם גבוהות יותר של סימני בניית עצם, ללא נזק מדיד לשריר. כאשר אותה מוטציה נוכחה בעכברים החסרים גנטית את הסקלרוסטין, לא נצפה אפקט נוסף, אך כאשר הוחזר סקלרוסטין נצפה שיכולתו לדכא עצם הייתה חלשה בהרבה בעכברי Lrp4m. באותו אופן, בעכברים מהונדסים להפיק יותר מדי סקלרוסטין או בעכברים עם אובדן עצם הקשור למחסור באסטרוגן, טיפול חוזר בפפטיד LRP4-Pep במינונים תלויי מידה הגדיל את מסת העצם, שיפר את איכות העצם והגביר את החוסן המכני, ועדיין לא נצפה אפקט כאשר סקלרוסטין היה נעדר.
לקראת טיפולים אנאבוליים לעצם בטוחים יותר
ביחד, ממצאים אלה מראים שאינטראקציה בין לופ3 של סקלרוסטין ו-LRP4 באוסטאובלסטים היא העוגן שסקלרוסטין זקוק לו כדי להתחבר ל-LRP6 ולכבות בניית עצם. על ידי שיבוש בררני של העוגן הזה — בין אם באמצעות מוטציות מדויקות או פפטיד מותאם — הצליחו החוקרים להגביר בניית עצם וחוזק בעכברים בלי לחסום ישירות את חלקי הסקלרוסטין שנראים חשובים להגנה הלבבית. עבור מטופלים, עבודה זו מצביעה על דור חדש של טיפולים מחזקים עצם שמטרתם אינה להשתיק את הסקלרוסטין לחלוטין, אלא לפצל את השפעותיו בעצם מהתפקידים המועילים שלו בלב וכלי הדם.
ציטוט: Wang, L., Tao, X., Jiang, H. et al. Osteoblastic sclerostin loop3-LRP4 interaction required by sclerostin to inhibit bone formation. Bone Res 14, 45 (2026). https://doi.org/10.1038/s41413-026-00511-x
מילות מפתח: אוסטאופורוזיס, סקלרוסטין, בניית עצם, LRP4, אותות Wnt