Clear Sky Science · zh
肿瘤来源的DNA通过促进网织红细胞清除引发癌症相关贫血
为何癌症相关贫血重要
贫血是癌症患者常见且令人虚弱的问题。当红细胞数量不足或功能受损时,患者会感到疲惫、气短,且更难耐受治疗。临床长期观察到肿瘤以某种方式扰乱机体的红细胞稳态,但其中确切机制一直不清楚。这项研究揭示了一个令人意外的罪魁祸首:从肿瘤逸出的游离DNA片段进入血流并直接损伤未成熟红细胞,为理解并可能治疗癌症相关贫血提供了新的视角。
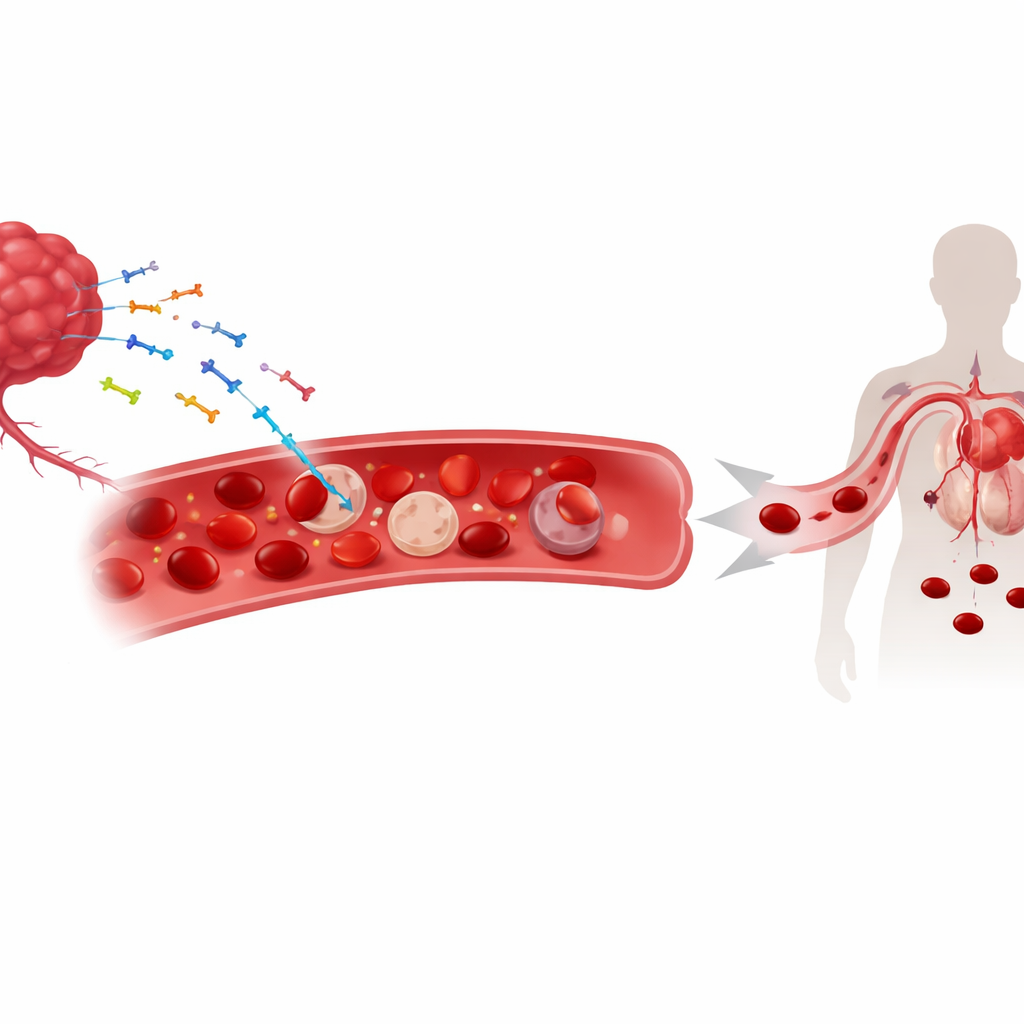
血液中的游离肿瘤DNA
随着肿瘤生长,它们会将核DNA和线粒体DNA等遗传物质片段释放到循环中。这些“细胞游离”DNA片段已被用作追踪癌症的生物标志物。研究人员发现,相当一部分肿瘤来源的DNA并非只是漂浮在血浆中,而是附着在红细胞表面。在肺癌、皮肤癌和结肠癌小鼠模型以及若干实体瘤患者中,红细胞表面结合的DNA含量增高与血红蛋白水平下降和贫血加重密切相关。这种关联在非癌性贫血中并不明显,提示DNA结合是癌症情境中的一种特征,而非红细胞减少的一般后果。
未成熟红细胞首当其冲
红细胞最初以未成熟形式出现,称为网织红细胞,它们在循环中短暂存在以完成成熟过程。研究团队发现,肿瘤来源的DNA选择性地作用于这些年轻细胞。在小鼠和癌症患者中,使用荧光染料和显微镜观察显示,超过95%的DNA阳性红细胞携带未成熟标志。这些被DNA包裹的网织红细胞形状异常、膜粗糙、血红蛋白和血红素含量降低,均表明其发育受阻。当用酶切除附着的DNA或用特殊溶液洗去时,这些细胞的特征得以部分恢复并继续向成熟方向发展。
从表面损伤到过早清除
为什么细胞表面的DNA会造成如此严重的影响?研究表明,它使年轻红细胞成为轰然被清除的主要目标。结合DNA的网织红细胞表现出“红细胞凋亡”(eryptosis)的特征,包括细胞内钙离子激增和膜上“吃我”信号的暴露。在体外和动物实验中,脾脏和肝脏巨噬细胞——负责清除老化或受损红细胞的免疫细胞——倾向吞噬DNA包裹的网织红细胞而非正常细胞。用切割DNA的酶DNase I处理红细胞或肿瘤小鼠,可去除表面结合的DNA并显著减少这种加速的清除,使红细胞在循环中存留更久。
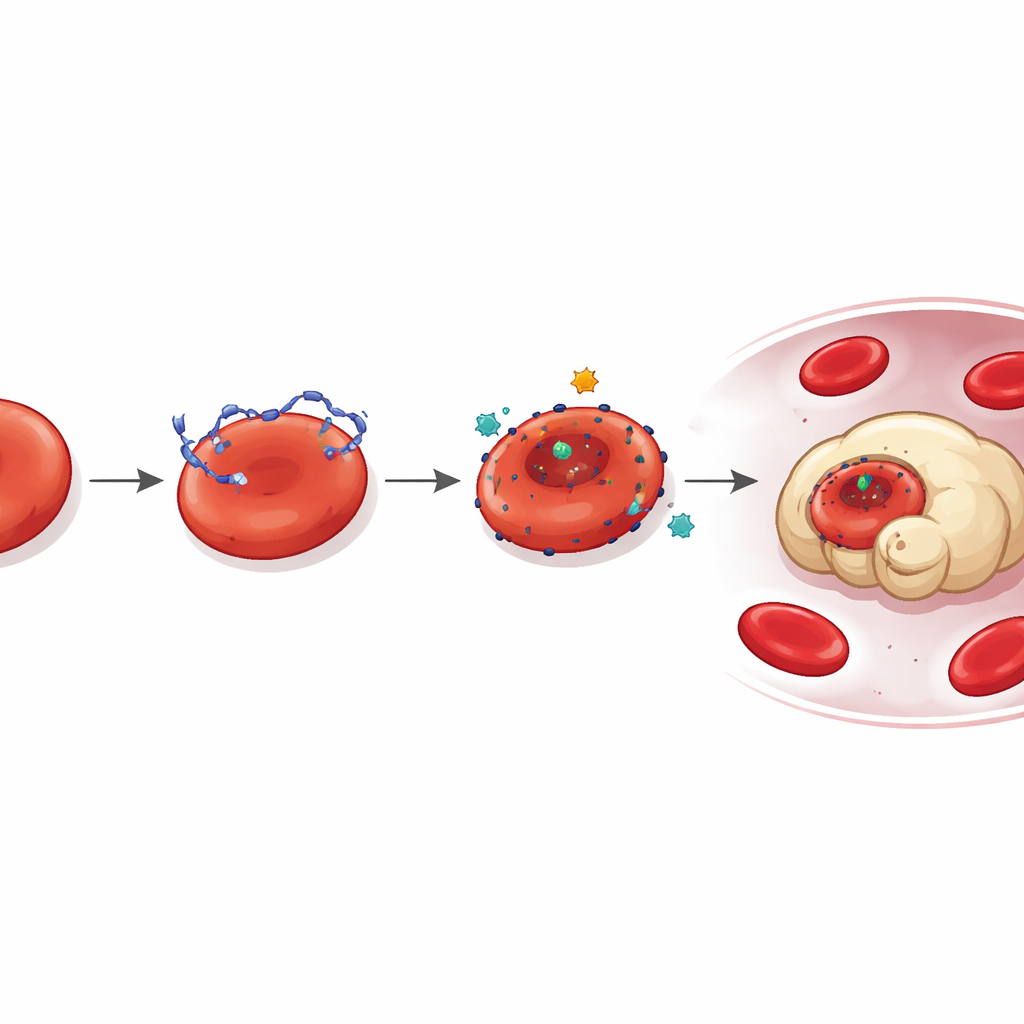
DNA的隐蔽停靠位点
进一步探究如何使DNA首先附着在网织红细胞上,蛋白质组学分析指向了LONP1——一种通常位于线粒体的蛋白——作为关键因子。在带瘤小鼠和癌症患者中,LONP1错误定位到循环网织红细胞的外表面,成为肿瘤来源DNA的高亲和力停靠点。表面携带LONP1的细胞结合更多DNA、变形更明显,并更快被巨噬细胞吞噬。阻断LONP1活性或降低其水平可减少DNA结合及随之而来的损伤,揭示了一条由肿瘤诱导的通路:错位的LONP1与游离DNA共同破坏未成熟红细胞。
将有害信号转为治疗靶点
由于目前许多针对癌症相关贫血的治疗仅着眼于增加红细胞生成,往往手段粗糙并带来诸如血栓或免疫系统不良影响等风险。这项工作提出了一种更精确的策略:阻止肿瘤来源的DNA首先破坏网织红细胞。小鼠实验中,单独使用DNase I治疗通过清除红细胞表面的有害DNA就能提高血红蛋白水平且不加速肿瘤生长。当DNase I与促红细胞生成素(刺激红细胞生成的激素)联合使用时,产生了更强的协同效应:既制造出更多红细胞,又减少了早期被清除的细胞。对于患者而言,这种以DNA为中心的癌症相关贫血视角为开发既能恢复红细胞平衡又不削弱抗肿瘤免疫的治疗方案打开了大门。
引用: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
关键词: 癌症相关贫血, 肿瘤来源DNA, 网织红细胞, 红细胞清除, DNase I治疗