Clear Sky Science · sv
Tumor‑deriverat DNA driver anemi associerad med cancer genom att främja avlägsnande av retikulocyter
Varför cancerrelaterad anemi är viktig
Anemi är ett vanligt och utmattande problem för personer med cancer. När de röda blodkropparna är för få eller för svaga känner patienterna trötthet, andfåddhet och sämre förmåga att tolerera behandling. Läkare har länge vetat att tumörer på något sätt rubbar kroppens balans av röda blodkroppar, men de exakta orsakerna har varit oklara. Denna studie avslöjar en överraskande bov: lösa DNA‑bitar som läcker ut från tumörer till blodbanan och direkt skadar unga röda blodkroppar, vilket ger en ny förklaring och potentiellt nya behandlingsmöjligheter för cancerassocierad anemi.
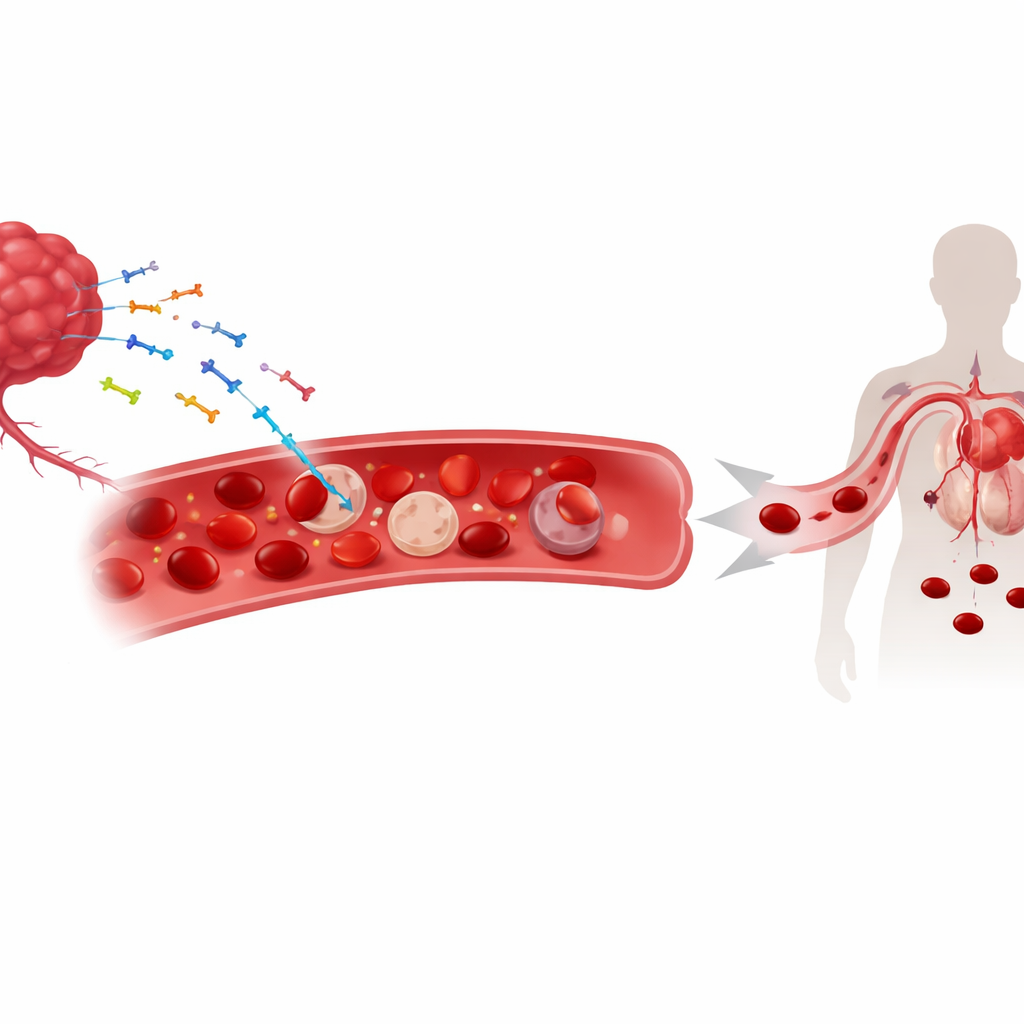
Vandrande tumör‑DNA i blodomloppet
När tumörer växer sprider de fragment av sitt genetiska material — både nukleärt och mitokondrie‑DNA — i cirkulationen. Dessa bitar av ”cellfritt” DNA används redan som biomarkörer för att följa cancer. Forskarna fann att en betydande del av detta tumör‑deriverade DNA inte bara flyter i plasman; istället fäster det på ytan av röda blodkroppar. I musemodeller för lung‑, hud‑ och koloncancer och hos patienter med flera solida tumörer korrelerade högre mängder DNA bundet till röda blodkroppar starkt med lägre hemoglobinnivåer och svårare anemi. Denna koppling syntes inte vid icke‑cancerrelaterad anemi, vilket tyder på att DNA‑bindning är en särskiljande egenskap i cancersammanhang snarare än en allmän följd av lågt antal röda blodkroppar.
De unga röda cellerna tar smällen
Röda blodkroppar föds som omogna former kallade retikulocyter, som cirkulerar kort tid medan de slutför sin mognad. Teamet upptäckte att tumör‑deriverat DNA selektivt riktar in sig på dessa unga celler. Med hjälp av fluorescerande färgningar och mikroskopi i möss och cancerpatienter visade de att över 95 procent av DNA‑positiva röda celler bar omognadsmarkörer. Dessa DNA‑belagda retikulocyter hade onormal form, förgröddade membraner och minskat hemoglobin‑ och hem‑innehåll — alla tecken på att deras utveckling ställts på ända. När det bundna DNA:t avlägsnades med enzymer eller sköljdes bort med särskilda lösningar återfick cellerna mer normala drag och fortsatte längre i sin mognadsprocess.
Från ytskada till förtida rensning
Varför spelar DNA på cellytan så stor roll? Studien visar att det förvandlar unga röda celler till lättare mål för destruktion. Retikulocyter bundna till DNA visade kännetecken för ”eryptos”, en programmerad dödsprocess för röda celler, inklusive kalciumpyser inuti cellen och exponering av ”ät mig”‑signaler på membranet. I laboratorie‑ och djurförsök åtog sig mjälte‑ och levermakrofager — immunceller som rensar åldrade eller skadade röda celler — föredömligt de DNA‑belagda retikulocyterna framför normala. Behandling av röda celler eller tumörbärande möss med DNA‑klyvande enzymet DNas I avlägsnade det bundna DNA:t och minskade kraftigt denna accelererade rensning, vilket gjorde att röda celler överlevde längre i cirkulationen.
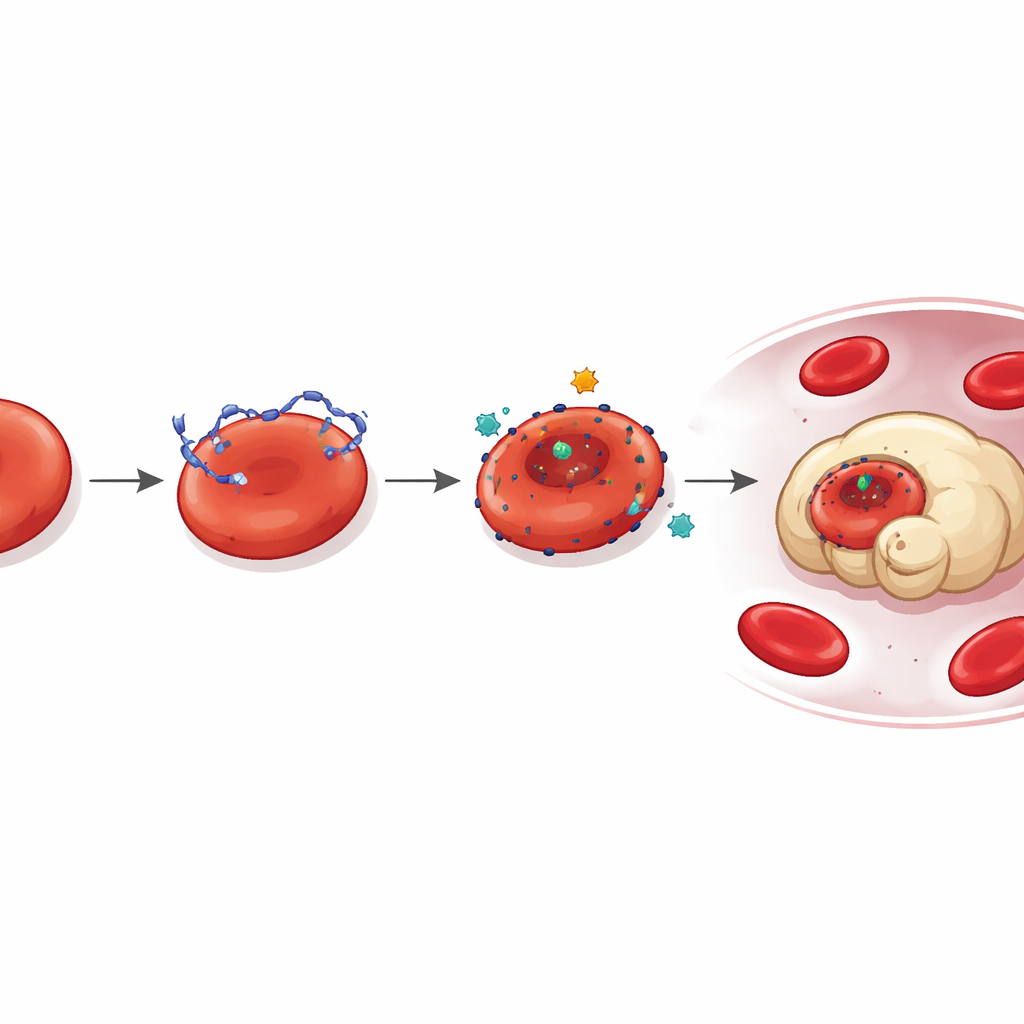
En dold angöringsplats för DNA
När forskarna grävde djupare frågade de hur DNA fäster vid retikulocyter från början. Proteomanalys pekade ut LONP1, ett protein som normalt finns i mitokondrier, som en nyckelspelare. Hos tumörbärande möss och cancerpatienter blev LONP1 felplacerat till den yttre ytan av cirkulerande retikulocyter. Där fungerade det som en högaffinitets‑ankringsplats för tumör‑deriverat DNA. Celler med ytantigen LONP1 band mer DNA, visade större deformitet och slukades snabbare av makrofager. Att blockera LONP1:s aktivitet eller minska dess mängd minskade DNA‑bindningen och den därav följande skadan, vilket avslöjar en tumörinducerad väg där felplacerat LONP1 och vandrande DNA tillsammans saboterar unga röda celler.
Att vända en skadlig signal till ett behandlingsmål
Eftersom många nuvarande behandlingar för cancerrelaterad anemi fokuserar enbart på att öka antalet röda blodkroppar kan de vara grova verktyg som medför risker som blodproppar eller oönskade effekter på immunförsvaret. Detta arbete föreslår en mer precis strategi: förhindra att tumör‑deriverat DNA förstör retikulocyter från första början. Hos möss ökade DNas I‑terapi ensam hemoglobinnivåerna utan att påskynda tumörtillväxt genom att rensa bort skadligt DNA från blodcellsytor. I kombination med erytropoietin, ett hormon som stimulerar produktion av röda blodkroppar, gav DNas I ännu starkare, synergistiska förbättringar: fler röda celler bildades och färre förstördes för tidigt. För patienter öppnar detta DNA‑centrerade synsätt på cancerassocierad anemi dörren till behandlingar som samtidigt återställer balansen av röda blodkroppar och undviker att undergräva antitumörimmuniteten.
Citering: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Nyckelord: cancerassocierad anemi, tumor‑deriverat DNA, retikulocyter, röda blodcellers rensning, DNas I‑terapi