Clear Sky Science · ar
الحمض النووي المنبثق من الورم يسبب فقر الدم المرتبط بالسرطان عبر تعزيز إزالة الخلايا الشبكية
لماذا يهم فقر الدم المتصل بالسرطان
فقر الدم مشكلة شائعة ومرهقة لدى الأشخاص المصابين بالسرطان. عندما تكون خلايا الدم الحمراء قليلة جدًا أو ضعيفة، يشعر المرضى بالتعب وقصر النفس وقلة التحمل للعلاج. لطالما عرف الأطباء أن الأورام تُخل بتوازن خلايا الدم الحمراء في الجسم بطريقة ما، لكن الأسباب الدقيقة كانت غامضة. تكشف هذه الدراسة عن مسبب مفاجئ: قطع حرة من الحمض النووي تهرب من الأورام إلى مجرى الدم وتُحدث ضررًا مباشرًا بالخلايا الحمراء الشابة، مما يقدم إطارًا جديدًا لفهم فقر الدم المرتبط بالسرطان وإمكانية علاجه.
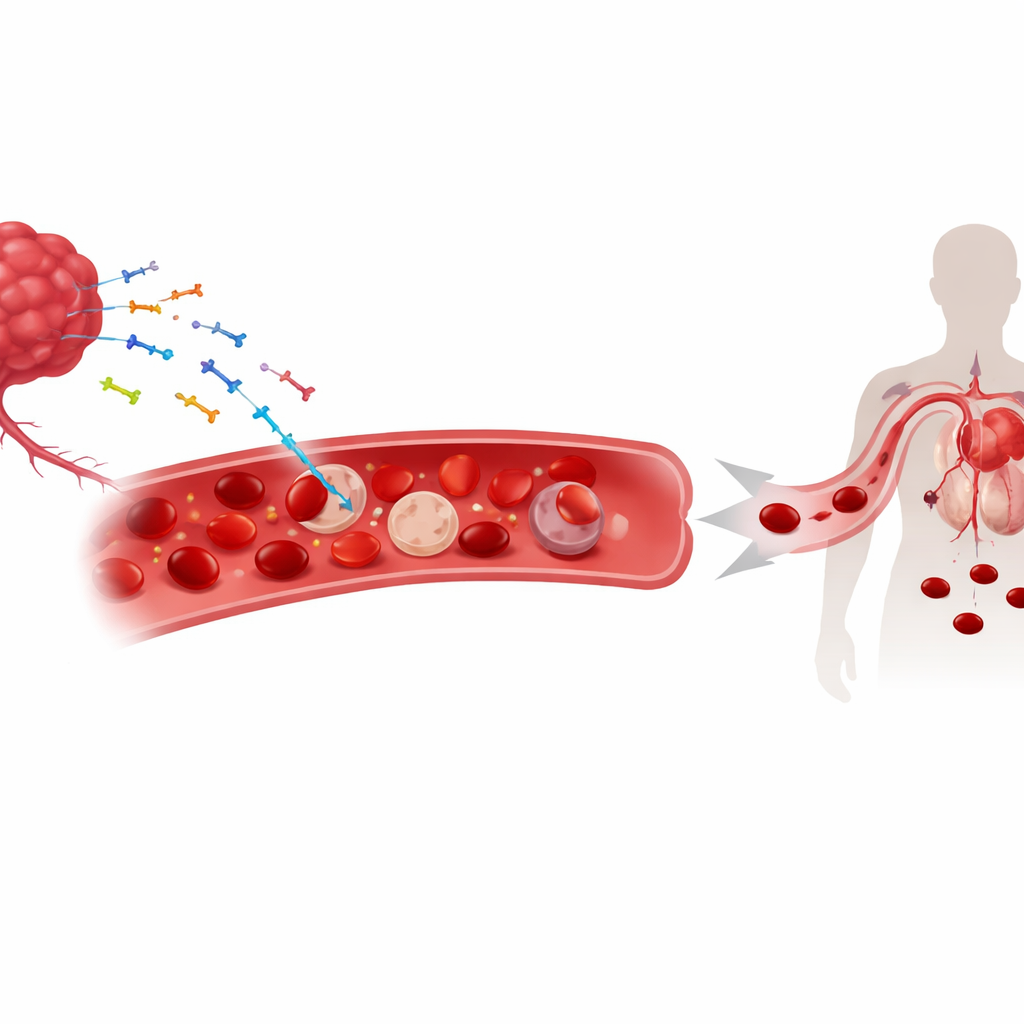
حمض نووي ورمي طافٍ في مجرى الدم
مع نمو الأورام، تتساقط قطع من مادتها الوراثية — سواء النووية أو الميتوكوندرية — إلى الدورة الدموية. تُستخدم هذه القطع من "الحمض النووي الخالي من الخلايا" بالفعل كعلامات حيوية لمتابعة السرطان. وجد الباحثون أن الجزء الكبير من هذا الحمض النووي المنبثق من الورم لا يطفو فحسب في البلازما؛ بل يلتصق بسطح خلايا الدم الحمراء. في نماذج الفئران للسرطان الرئوي والجلدي والقولوني وفي مرضى يعانون عدة أورام صلبة، ارتبطت كميات أعلى من الحمض النووي المرتبط بخلايا الدم الحمراء بانخفاض مستويات الهيموغلوبين وزيادة شدة فقر الدم. ولم تظهر هذه العلاقة في أشكال فقر الدم غير المرتبطة بالسرطان، مما يشير إلى أن ارتباط الحمض النووي سمة مميزة لحالة السرطان بدلاً من نتيجة عامة لانخفاض عدد خلايا الدم الحمراء.
الخلايا الحمراء الشابة تتلقَّى الضربة
تولد خلايا الدم الحمراء بأشكال غير ناضجة تسمى الخلايا الشبكية، التي تدور لفترة وجيزة أثناء إكمال نضجها. اكتشفت الفريق أن الحمض النووي المنبثق من الورم يستهدف هذه الخلايا الشابة بشكل انتقائي. باستخدام أصباغ فلورية والمجهر في الفئران والمرضى، أظهروا أن أكثر من 95 بالمئة من الخلايا الحمراء الحاملة للحمض النووي حملت علامات عدم النضج. كانت هذه الخلايا الشبكية المغطاة بالحمض النووي مشوهة الشكل، ذات أغشية خشنة، ومحتوى منخفض من الهيموغلوبين والهي�م ـ علامات على تعطّل مسار نضجها. عندما أُزيل الحمض النووي المرتبط بواسطة إنزيمات أو جُرِدَ بغسلات خاصة، استعادت الخلايا ملامح أكثر طبيعية وتقدمت في مسار نضجها.
من الضرر السطحي إلى الإزالة المبكرة
لماذا يهم وجود الحمض النووي على سطح الخلية إلى هذا الحد؟ تُظهر الدراسة أنه يحول الخلايا الشبكية الشابة إلى أهداف جاهزة للتدمير. أظهرت الخلايا الشبكية المرتبطة بالحمض النووي علامات على "الإريبتوز"، وهو عملية موت مبرمجة للخلايا الحمراء، بما في ذلك اندفاعات الكالسيوم داخل الخلية وكشف إشارات "اكسرني" على الغشاء. في تجارب مخبرية وحيوانية، ابتلعت الخلايا البلعمية في الطحال والكبد — وهي خلايا مناعية تزيل خلايا الدم القديمة أو التالفة — الخلايا الشبكية المغطاة بالحمض النووي تفضيلاً على الخلايا الطبيعية. معالجة خلايا الدم أو الفئران الحاملة للأورام بإنزيم قطع الحمض النووي DNase I أزالت الحمض النووي المرتبط وخفّضت بشدة هذه الإزالة المتسارعة، مما سمح لبقاء خلايا الدم في الدورة الدموية لفترة أطول.
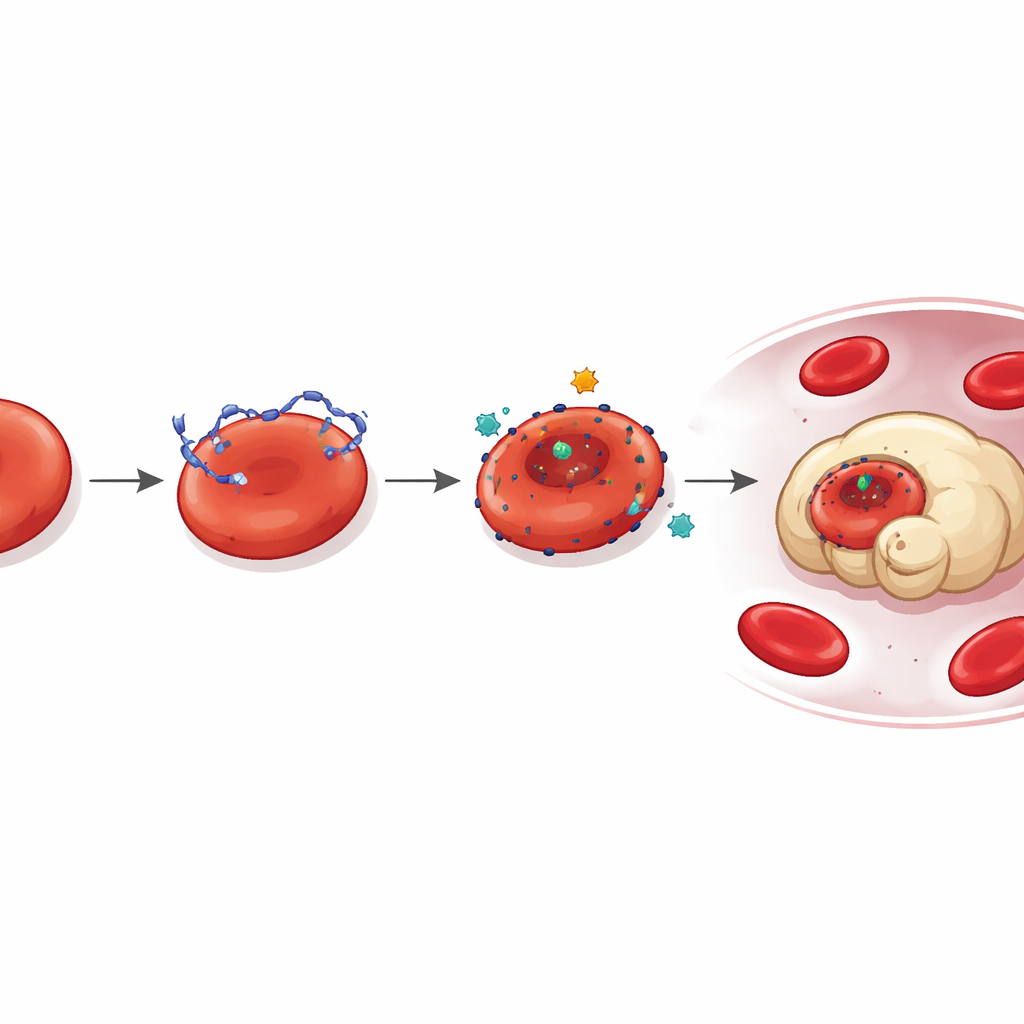
موقع ربط خفي للحمض النووي
بتعمق أكثر، سأل الباحثون كيف يلتصق الحمض النووي بالخلايا الشبكية في المقام الأول. أشارت تحليلات البروتيوم إلى بروتين LONP1، الموجود عادة في الميتوكوندريا، كلاعب أساسي. في الفئران الحاملة للأورام والمرضى، أصبح LONP1 مموضعًا بشكل خاطئ على السطح الخارجي للخلايا الشبكية الدائرة. هناك عمل كموقع تلاصق عالي التقارب للحمض النووي المنبثق من الورم. الخلايا التي تحمل LONP1 سطحيًا ارتبطت بمزيد من الحمض النووي، أظهرت تشوهاً أكبر، وابتلعتها الخلايا البلعمية بسرعة أكبر. حجب نشاط LONP1 أو تقليل مستوياته خفّض ارتباط الحمض النووي والضرر الناتج، كاشفًا مسارًا تُحدثه الأورام حيث يتضافر LONP1 المتموضع بشكل خاطئ والحمض النووي الطافي لتخريب الخلايا الحمراء الشابة.
تحويل إشارة ضارة إلى هدف علاجي
لأن العديد من العلاجات الحالية لفقر الدم المرتبط بالسرطان تركز فقط على زيادة إنتاج خلايا الدم الحمراء، فهي أدوات قد تكون غليظة وتحمل مخاطر مثل جلطات الدم أو تأثيرات غير مرغوبة على الجهاز المناعي. تشير هذه الدراسة إلى نهج أكثر دقة: منع الحمض النووي المنبثق من الورم من تدمير الخلايا الشبكية من البداية. في الفئران، رفع علاج DNase I وحده مستويات الهيموغلوبين دون تسريع نمو الورم عن طريق إزالة الحمض النووي الضار من أسطح خلايا الدم. عندما جمع مع الإريثروبويتين، الهرمون المحفز لإنتاج خلايا الدم الحمراء، أظهر DNase I تحسناً أقوى وتآزريًا: زاد إنتاج الخلايا الحمراء وقُلل تدميرها المبكر. بالنسبة للمرضى، يفتح هذا التصور المركزي للحمض النووي في فقر الدم المرتبط بالسرطان الباب أمام علاجات تستعيد توازن خلايا الدم الحمراء مع تجنب تقويض المناعة المضادة للورم.
الاستشهاد: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
الكلمات المفتاحية: فقر الدم المرتبط بالسرطان, الحمض النووي المنبثق من الورم, الخلايا الشبكية, إزالة خلايا الدم الحمراء, علاج DNase I