Clear Sky Science · pl
DNA pochodzące z guza powoduje anemię związaną z rakiem poprzez przyspieszone usuwanie retikulocytów
Dlaczego anemia związana z rakiem ma znaczenie
Anemia jest częstym i osłabiającym problemem u osób z rakiem. Gdy czerwonych krwinek jest za mało albo są osłabione, pacjenci odczuwają zmęczenie, duszność i mają mniejszą tolerancję leczenia. Lekarze od dawna wiedzieli, że guzy w jakiś sposób zaburzają równowagę czerwonych krwinek, lecz dokładne mechanizmy pozostawały niejasne. To badanie ujawnia zaskakującego sprawcę: luźne fragmenty DNA uwalniane z guzów do krwiobiegu, które bezpośrednio uszkadzają młode czerwone krwinki, oferując nową perspektywę na rozumienie i możliwe leczenie anemii związanej z rakiem.
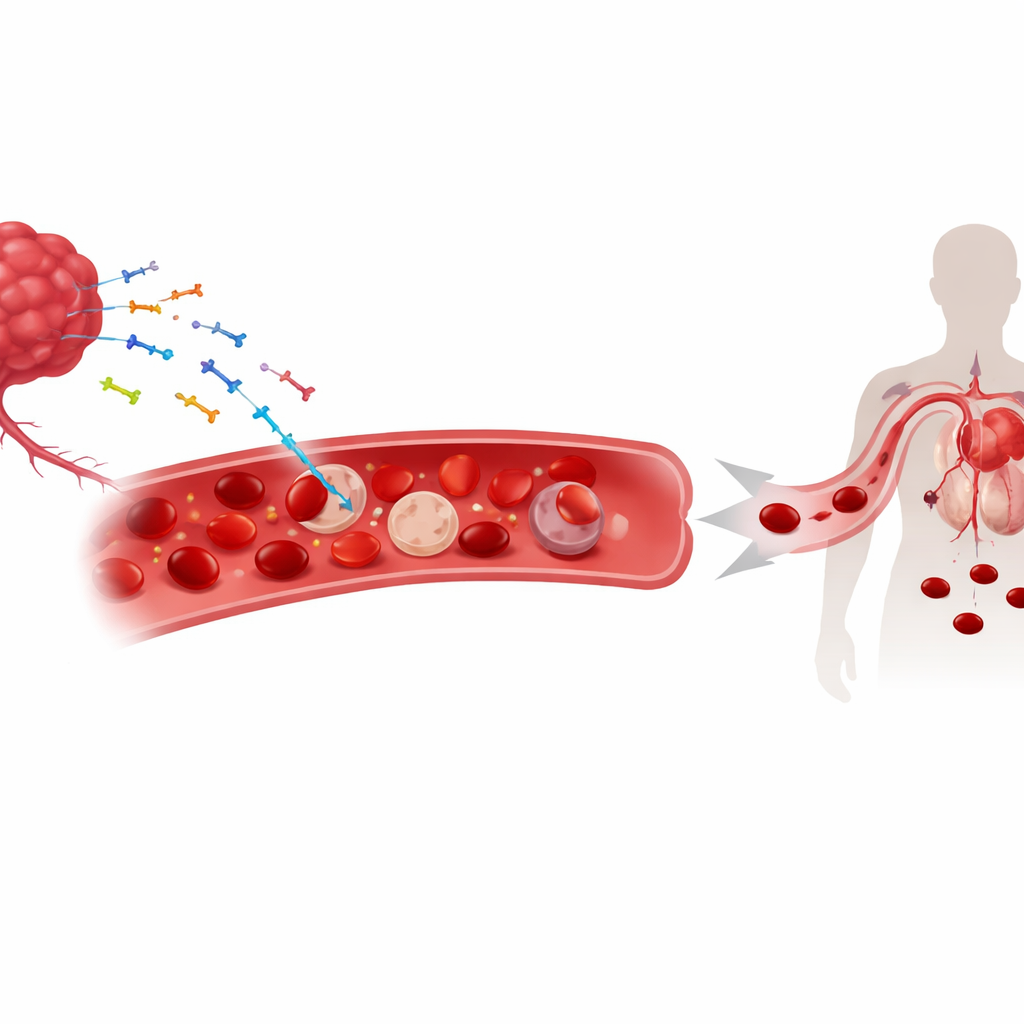
Wędrujące DNA guza we krwi
W miarę wzrostu guzów uwalniane są fragmenty materiału genetycznego — zarówno DNA jądrowe, jak i mitochondrialne — do krążenia. Te kawałki „wolnego” DNA są już wykorzystywane jako markery do monitorowania raka. Badacze stwierdzili, że znaczna część tego DNA pochodzącego z guza nie tylko unosi się w osoczu; zamiast tego przylega do powierzchni czerwonych krwinek. W modelach mysich raka płuca, skóry i jelita grubego oraz u pacjentów z kilkoma nowotworami litymi większe ilości DNA związane z erytrocytami ściśle korelowały z niższym stężeniem hemoglobiny i cięższą anemią. Zależność ta nie występowała w anemii niezwiązanej z rakiem, co sugeruje, że wiązanie DNA jest charakterystyczne dla kontekstu nowotworowego, a nie ogólną konsekwencją niskiej liczby czerwonych krwinek.
Młode czerwone komórki ponoszą konsekwencje
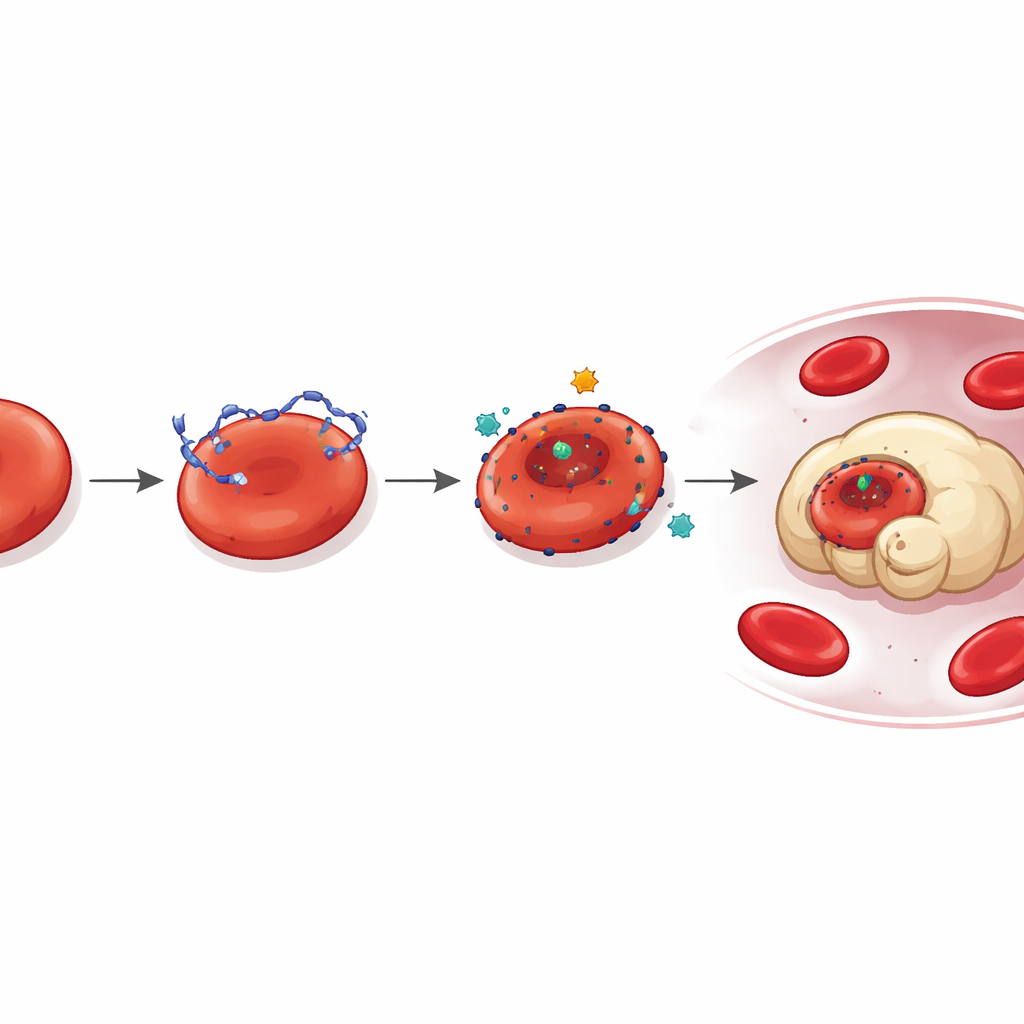
Czerwone krwinki rodzą się jako niedojrzałe formy zwane retikulocytami, które krążą krótko, dopóki nie zakończą dojrzewania. Zespół odkrył, że DNA pochodzące z guza selektywnie atakuje te młode komórki. Przy użyciu barwników fluorescencyjnych i mikroskopii u myszy oraz pacjentów z rakiem wykazano, że ponad 95 procent erytrocytów pozytywnych w kierunku DNA nosiło markery niedojrzałości. Te pokryte DNA retikulocyty miały nieprawidłowy kształt, chropowate błony i zmniejszoną zawartość hemoglobiny i hemu — wszystkie objawy zaburzonego rozwoju. Gdy związane DNA usuwano enzymami lub zmywano specjalnymi roztworami, komórki odzyskiwały bardziej normalne cechy i miały większe szanse dokończyć proces dojrzewania.
Od uszkodzenia powierzchni do przedwczesnego usuwania
Dlaczego DNA na powierzchni komórki ma tak duże znaczenie? Badanie pokazuje, że przemienia to młode czerwone komórki w główne cele do zniszczenia. Retikulocyty pokryte DNA wykazywały cechy „eryptozy” — zaprogramowanej śmierci erytrocytów — w tym wzrost poziomu wapnia w komórce i ekspozycję sygnałów „jedz mnie” na błonie. W eksperymentach laboratoryjnych i na zwierzętach makrofagi śledziony i wątroby — komórki układu odpornościowego odpowiedzialne za usuwanie starych lub uszkodzonych erytrocytów — preferencyjnie pochłaniały retikulocyty pokryte DNA zamiast normalnych. Leczenie czerwonych krwinek lub myszy z guzami enzymem tnącym DNA, DNazą I, usuwało związane DNA i wyraźnie zmniejszało tę przyspieszoną eliminację, pozwalając erytrocytom dłużej przetrwać w krążeniu.
Ukryte miejsce dokowania dla DNA
Idąc dalej, badacze zastanawiali się, jak DNA w ogóle przylega do retikulocytów. Analiza proteomiczna wskazała na LONP1, białko zwykle zlokalizowane w mitochondriach, jako istotnego uczestnika. U myszy z guzami i u pacjentów z rakiem LONP1 został błędnie przemieszczony na zewnętrzną powierzchnię krążących retikulocytów. Tam działał jako miejsce dokowania o wysokim powinowactwie dla DNA pochodzącego z guza. Komórki z LONP1 na powierzchni wiązały więcej DNA, wykazywały większe deformacje i były szybciej pochłaniane przez makrofagi. Hamowanie aktywności LONP1 lub zmniejszanie jego poziomów ograniczało wiązanie DNA i wynikające z tego uszkodzenia, ujawniając indukowaną przez guz ścieżkę, w której błędnie zlokalizowany LONP1 i luźne DNA wspólnie sabotują młode czerwone komórki.
Przekształcenie szkodliwego sygnału w cel terapeutyczny
Ponieważ wiele obecnych metod leczenia anemii związanej z rakiem skupia się jedynie na zwiększeniu produkcji czerwonych krwinek, mogą być to narzędzia nieprecyzyjne niosące ryzyko powikłań, takich jak zakrzepy czy niepożądane efekty dla układu odpornościowego. Ta praca sugeruje bardziej precyzyjne podejście: zapobiec temu, by DNA pochodzące z guza niszczyło retikulocyty na samym początku. U myszy sama terapia DNazą I podniosła poziom hemoglobiny bez przyspieszania wzrostu guza poprzez usuwanie szkodliwego DNA z powierzchni erytrocytów. W połączeniu z erytropoetyną — hormonem stymulującym produkcję czerwonych krwinek — DNaza I dała jeszcze silniejsze, synergistyczne efekty: wytwarzano więcej krwinek, a mniej z nich było przedwcześnie eliminowanych. Dla pacjentów to spojrzenie na anemię związaną z rakiem skoncentrowane na DNA otwiera drzwi do terapii, które równocześnie przywracają równowagę czerwonych krwinek i unikają osłabiania odpowiedzi przeciwnowotworowej.
Cytowanie: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Słowa kluczowe: anemia związana z rakiem, DNA pochodzące z guza, retikulocyty, usuwanie czerwonych krwinek, terapia DNazą I