Clear Sky Science · it
Il DNA derivato dal tumore causa anemia associata al cancro promuovendo l’eliminazione dei reticolociti
Perché l’anemia correlata al cancro conta
L’anemia è un problema comune e debilitante per le persone con cancro. Quando i globuli rossi sono troppo pochi o troppo deboli, i pazienti si sentono stanchi, affaticati e meno in grado di tollerare le terapie. I medici sanno da tempo che i tumori in qualche modo disturbano l’equilibrio dei globuli rossi dell’organismo, ma le ragioni esatte sono rimaste poco chiare. Questo studio individua un colpevole sorprendente: frammenti di DNA sciolto che fuoriescono dai tumori nel flusso sanguigno e danneggiano direttamente i globuli rossi giovani, offrendo un nuovo modo di comprendere e possibilmente trattare l’anemia associata al cancro.
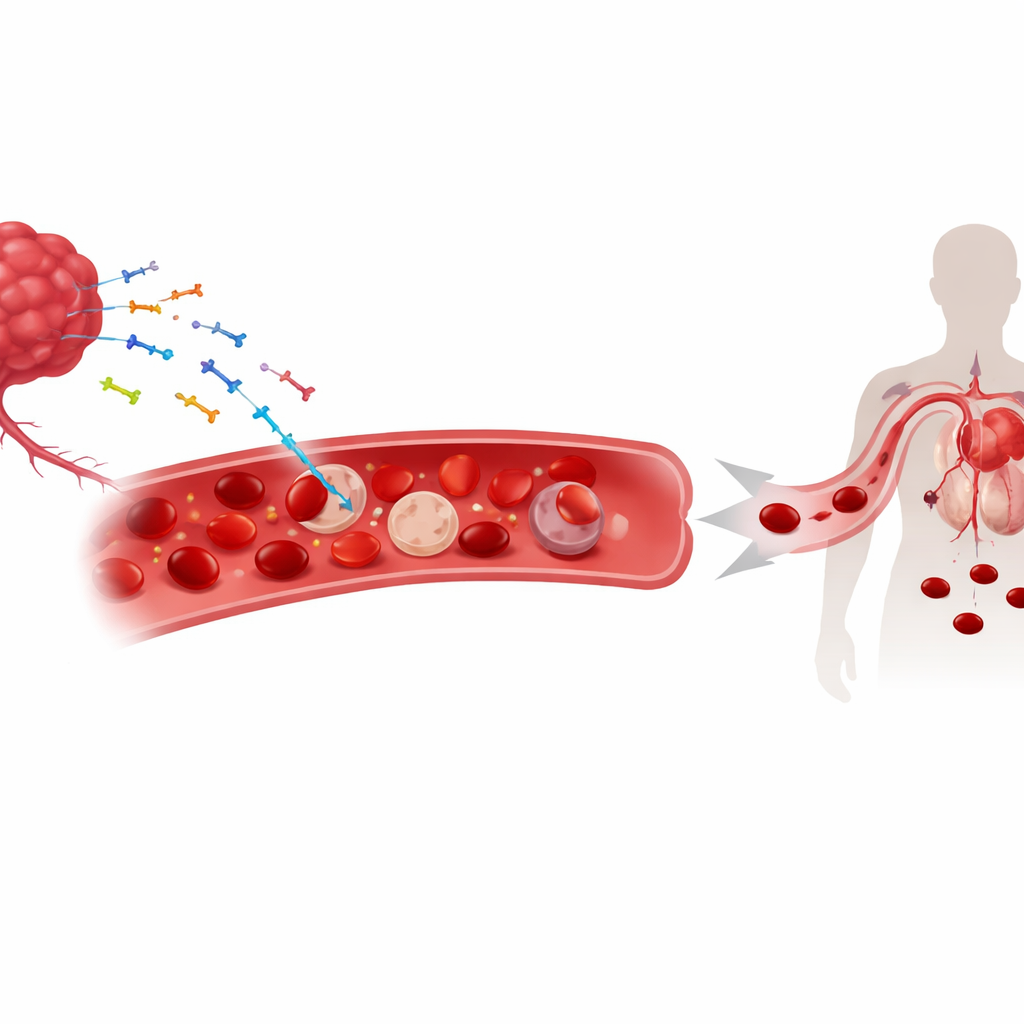
DNA tumorale disperso nel circolo ematico
Man mano che i tumori crescono, rilasciano frammenti del loro materiale genetico—sia DNA nucleare sia mitocondriale—nella circolazione. Questi pezzi di DNA “cell-free” sono già impiegati come biomarcatori per monitorare il cancro. I ricercatori hanno scoperto che una parte sostanziale di questo DNA derivato dal tumore non si limita a galleggiare nel plasma; al contrario, si attacca alla superficie dei globuli rossi. In modelli murini di tumori del polmone, della pelle e del colon e in pazienti con diversi tumori solidi, quantità maggiori di DNA legato ai globuli rossi correla strettamente con livelli più bassi di emoglobina e con anemia più grave. Questo legame non è apparso nelle forme di anemia non correlate al cancro, suggerendo che l’adesione del DNA è una caratteristica distintiva del contesto tumorale piuttosto che una conseguenza generale della riduzione dei globuli rossi.
I globuli rossi giovani sono i più colpiti
I globuli rossi nascono come forme immature chiamate reticolociti, che circolano brevemente mentre completano la maturazione. Il gruppo ha scoperto che il DNA derivato dal tumore prende di mira in modo selettivo queste cellule giovani. Usando coloranti fluorescenți e microscopia in topi e pazienti oncologici, hanno mostrato che oltre il 95 percento delle cellule rosse positive al DNA portava marcatori di immaturità. Questi reticolociti rivestiti di DNA avevano forma anomala, membrane ruvide e contenuto ridotto di emoglobina ed eme, tutti segni che il loro sviluppo era stato compromesso. Quando il DNA legato veniva rimosso con enzimi o lavato via con soluzioni speciali, le cellule recuperavano caratteristiche più normali e progredivano ulteriormente lungo il percorso di maturazione.
Dal danno sulla superficie all’eliminazione precoce
Perché il DNA sulla superficie cellulare è così importante? Lo studio mostra che trasforma i reticolociti in bersagli privilegiati per la distruzione. I reticolociti legati al DNA mostravano i segni dell’“eritposi”, un processo di morte programmata per i globuli rossi, inclusi aumenti di calcio intracellulare ed esposizione di segnali di “mangiami” sulla membrana. In esperimenti in laboratorio e su animali, macrofagi della milza e del fegato—cellule immunitarie che eliminano globuli rossi vecchi o danneggiati—ingerivano preferenzialmente i reticolociti rivestiti di DNA rispetto a quelli normali. Trattare i globuli rossi o i topi portatori di tumore con l’enzima che taglia il DNA, la DNasi I, rimuoveva il DNA legato e riduceva nettamente questa eliminazione accelerata, permettendo ai globuli rossi di persistere più a lungo in circolo.
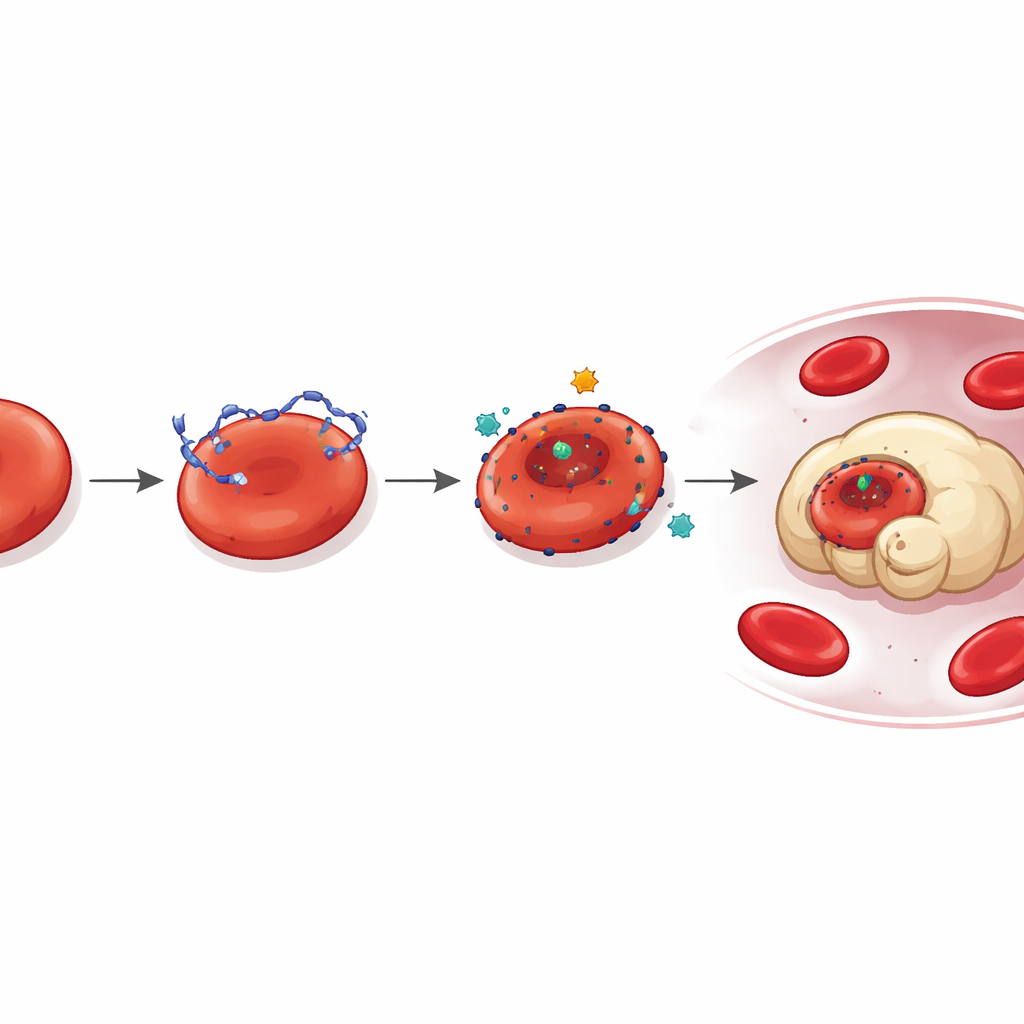
Un sito di ancoraggio nascosto per il DNA
Approfondendo la questione, i ricercatori si sono chiesti come il DNA si agganci ai reticolociti in primo luogo. L’analisi proteomica ha indicato LONP1, una proteina normalmente presente nei mitocondri, come attore chiave. Nei topi portatori di tumore e nei pazienti oncologici, LONP1 risultava mal localizzata sulla superficie esterna dei reticolociti circolanti. Lì agiva come sito di ancoraggio ad alta affinità per il DNA derivato dal tumore. Le cellule con LONP1 superficiale legavano più DNA, mostravano una deformità maggiore ed erano inghiottite più rapidamente dai macrofagi. Bloccare l’attività di LONP1 o ridurne i livelli diminuiva il legame del DNA e i danni risultanti, rivelando una via indotta dal tumore in cui LONP1 mal riposizionato e DNA disperso insieme sabotano i globuli rossi giovani.
Trasformare un segnale dannoso in un bersaglio terapeutico
Poiché molte terapie correnti per l’anemia correlata al cancro si concentrano solo sull’aumentare la produzione di globuli rossi, possono essere strumenti poco precisi che comportano rischi come trombosi o effetti indesiderati sul sistema immunitario. Questo lavoro suggerisce un approccio più mirato: impedire che il DNA derivato dal tumore rovini i reticolociti in primo luogo. Nei topi, la sola terapia con DNasi I aumentava i livelli di emoglobina senza accelerare la crescita tumorale, rimuovendo il DNA dannoso dalla superficie delle cellule rosse. Quando combinata con l’eritropoietina, un ormone che stimola la produzione di globuli rossi, la DNasi I ha prodotto miglioramenti ancora più marcati e sinergici: sono stati prodotti più globuli rossi e ne sono stati distrutti meno prematuramente. Per i pazienti, questa visione centrata sul DNA dell’anemia associata al cancro apre la strada a terapie che ristabiliscono l’equilibrio dei globuli rossi evitando al contempo di compromettere l’immunità anti-tumorale.
Citazione: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Parole chiave: anemia associata al cancro, DNA derivato dal tumore, reticolociti, eliminazione dei globuli rossi, terapia con DNasi I