Clear Sky Science · pt
DNA derivado de tumor provoca anemia associada ao câncer ao promover limpeza de reticulócitos
Por que a anemia relacionada ao câncer é importante
A anemia é um problema comum e exaustivo para pessoas com câncer. Quando os glóbulos vermelhos são poucos ou fracos demais, os pacientes sentem cansaço, falta de ar e menor capacidade de tolerar o tratamento. Os médicos sabem há muito tempo que os tumores de algum modo perturbam o equilíbrio dos glóbulos vermelhos do corpo, mas as causas exatas permaneceram obscuras. Este estudo revela um culpado surpreendente: fragmentos soltos de DNA que escapam dos tumores para a corrente sanguínea e danificam diretamente os glóbulos vermelhos jovens, oferecendo uma nova forma de entender e possivelmente tratar a anemia associada ao câncer.
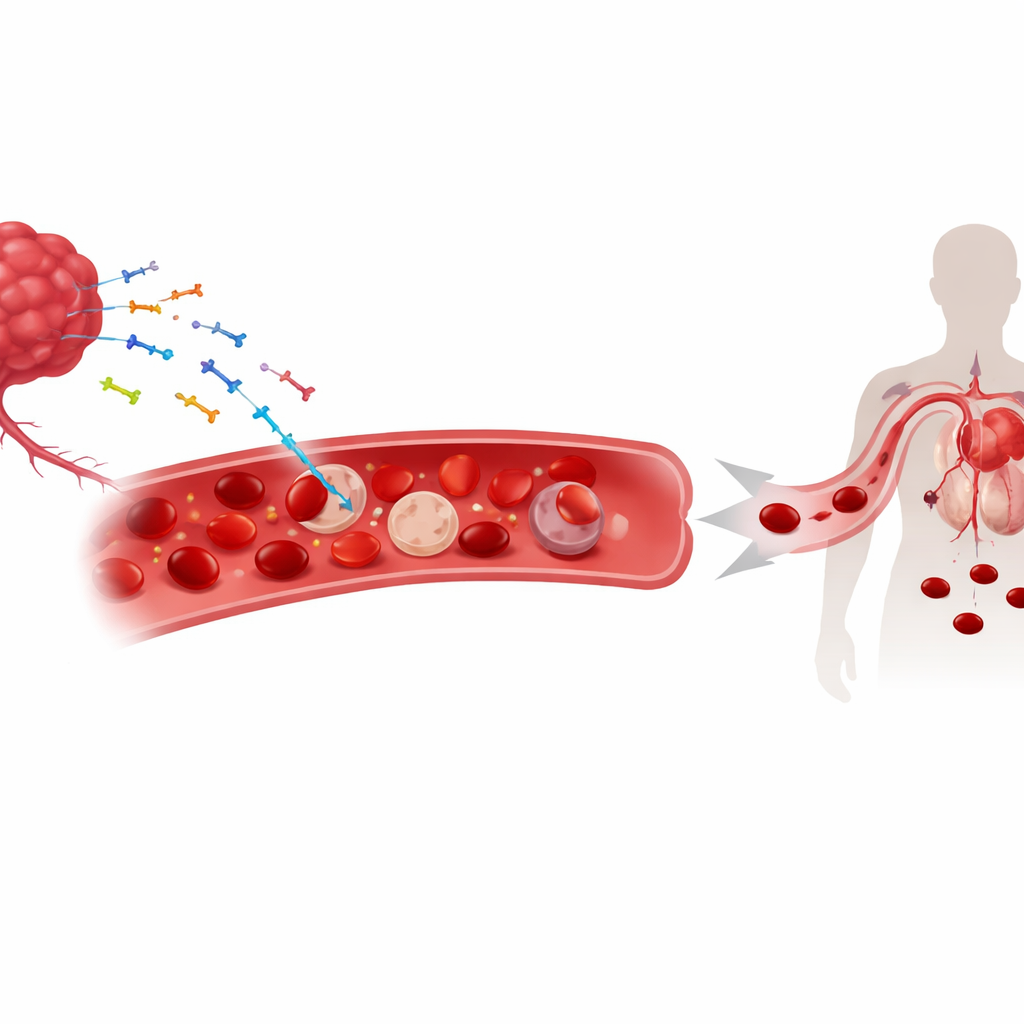
DNA tumoral solto na corrente sanguínea
À medida que os tumores crescem, eles liberam fragmentos de seu material genético — tanto DNA nuclear quanto mitocondrial — na circulação. Esses pedaços de "DNA livre" já são usados como biomarcadores para acompanhar o câncer. Os pesquisadores descobriram que uma parte substancial desse DNA derivado do tumor não apenas flutua no plasma; em vez disso, adere à superfície dos glóbulos vermelhos. Em modelos murinos de câncer de pulmão, pele e cólon e em pacientes com vários tumores sólidos, quantidades maiores de DNA ligado aos glóbulos vermelhos se correlacionaram fortemente com níveis mais baixos de hemoglobina e anemia mais grave. Essa associação não apareceu em formas não cancerígenas de anemia, sugerindo que a ligação do DNA é uma característica distintiva do contexto do câncer, e não uma consequência geral da baixa contagem de glóbulos vermelhos.
As células vermelhas jovens são as mais afetadas
Os glóbulos vermelhos nascem como formas imaturas chamadas reticulócitos, que circulam brevemente enquanto terminam de maturar. A equipe descobriu que o DNA derivado do tumor atinge seletivamente essas células jovens. Usando corantes fluorescentes e microscopia em camundongos e pacientes com câncer, demonstraram que mais de 95% das células vermelhas positivas para DNA carregavam marcadores de imaturidade. Esses reticulócitos revestidos de DNA exibiam formato anormal, membranas ásperas e redução do conteúdo de hemoglobina e heme — todos sinais de que seu desenvolvimento fora desviado. Quando o DNA ligado foi removido com enzimas ou lavado com soluções especiais, as células recuperaram características mais normais e avançaram mais em sua via de maturação.
Do dano superficial à remoção prematura
Por que o DNA na superfície celular importa tanto? O estudo mostra que ele transforma reticulócitos jovens em alvos preferenciais para destruição. Reticulócitos ligados ao DNA apresentaram sinais de "eritoptose", um processo de morte programada para glóbulos vermelhos, incluindo surtos de cálcio dentro da célula e exposição de sinais de "me consuma" na membrana. Em experimentos de laboratório e em animais, macrófagos do baço e do fígado — células imunes que removem glóbulos vermelhos envelhecidos ou danificados — engolfaram preferencialmente reticulócitos revestidos de DNA em relação aos normais. Tratar glóbulos vermelhos ou camundongos portadores de tumor com a enzima que corta DNA, DNase I, removeu o DNA ligado e reduziu drasticamente essa remoção acelerada, permitindo que os glóbulos vermelhos persistissem por mais tempo na circulação.
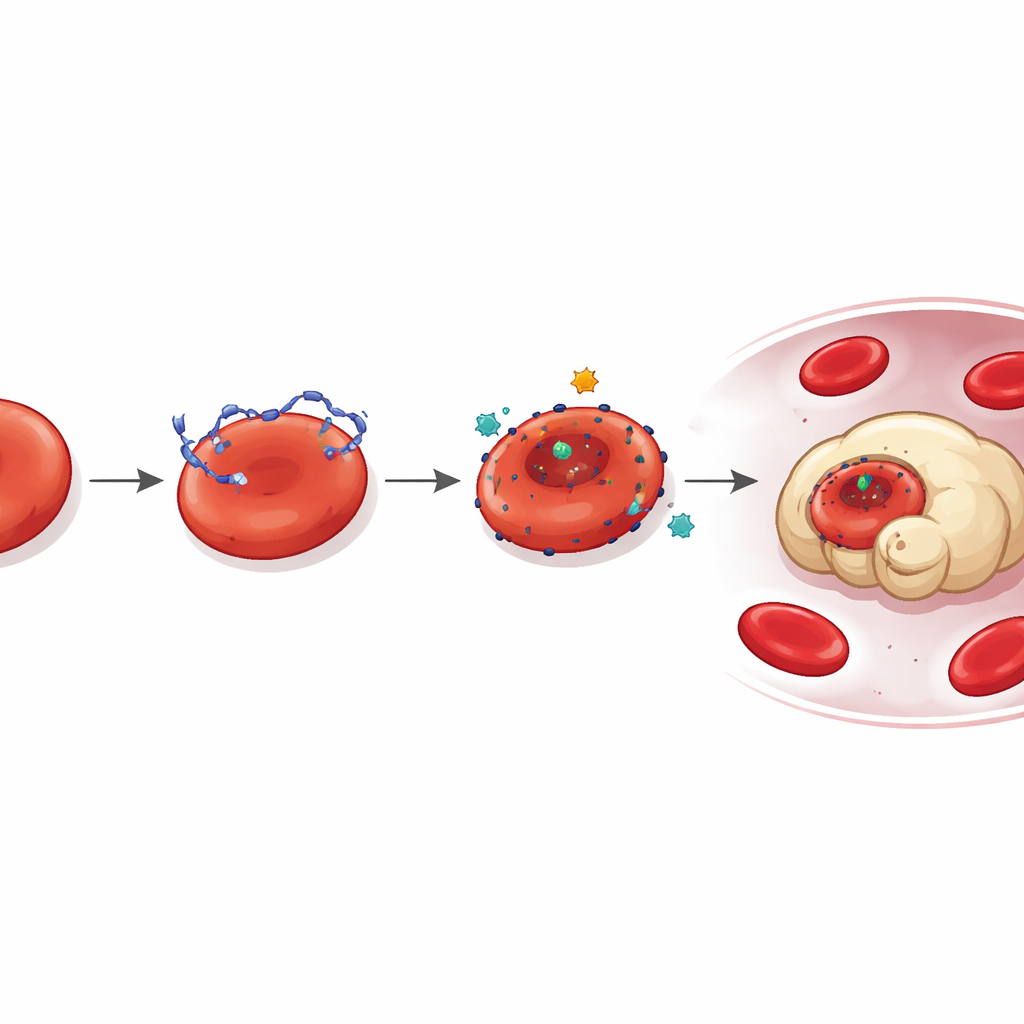
Um ponto de ancoragem oculto para o DNA
Aprofundando a investigação, os pesquisadores perguntaram como o DNA se prende aos reticulócitos em primeiro lugar. A análise proteômica apontou para LONP1, uma proteína normalmente encontrada nas mitocôndrias, como um ator-chave. Em camundongos com tumor e em pacientes com câncer, a LONP1 tornou-se deslocalizada para a superfície externa dos reticulócitos circulantes. Lá, atuou como um sítio de ancoragem de alta afinidade para o DNA derivado do tumor. Células com LONP1 na superfície ligaram mais DNA, apresentaram deformidade maior e foram engolidas mais rapidamente pelos macrófagos. Bloquear a atividade de LONP1 ou reduzir seus níveis diminuiu a ligação de DNA e os danos resultantes, revelando uma via induzida pelo tumor em que LONP1 malposicionado e DNA solto juntos sabotam os glóbulos vermelhos jovens.
Transformando um sinal nocivo em alvo terapêutico
Como muitos tratamentos atuais para a anemia relacionada ao câncer focam apenas em produzir mais glóbulos vermelhos, eles podem ser ferramentas pouco precisas que trazem riscos, como coágulos sanguíneos ou efeitos indesejados sobre o sistema imunológico. Este trabalho sugere uma abordagem mais precisa: impedir que o DNA derivado do tumor destrua os reticulócitos desde o início. Em camundongos, a terapia com DNase I isoladamente elevou os níveis de hemoglobina sem acelerar o crescimento tumoral ao eliminar o DNA prejudicial das superfícies das células vermelhas. Quando combinada com eritropoietina, um hormônio que estimula a produção de glóbulos vermelhos, a DNase I produziu melhorias ainda mais fortes e sinérgicas: mais glóbulos vermelhos foram produzidos e menos foram destruídos prematuramente. Para pacientes, essa visão centrada no DNA da anemia associada ao câncer abre a porta para terapias que simultaneamente restaurem o equilíbrio dos glóbulos vermelhos e evitem minar a imunidade antitumoral.
Citação: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Palavras-chave: anemia associada ao câncer, DNA derivado de tumor, reticulócitos, remoção de glóbulos vermelhos, terapia com DNase I