Clear Sky Science · ru
ДНК, происходящая из опухоли, вызывает анемию, связанную с раком, стимулируя клиренс ретикулоцитов
Почему важна анемия при раке
Анемия — частая и изматывающая проблема у людей с раком. Когда эритроцитов слишком мало или они недостаточно функциональны, пациенты чувствуют усталость, одышку и хуже переносят лечение. Врачи давно замечали, что опухоли как-то нарушают баланс красных кровяных клеток, но точные причины оставались неясными. В этом исследовании выявлен неожиданный виновник: свободные фрагменты ДНК, которые покидают опухоль и попадают в кровь, напрямую повреждая молодые эритроциты — это дает новую перспективу для понимания и возможного лечения анемии, связанной с раком.
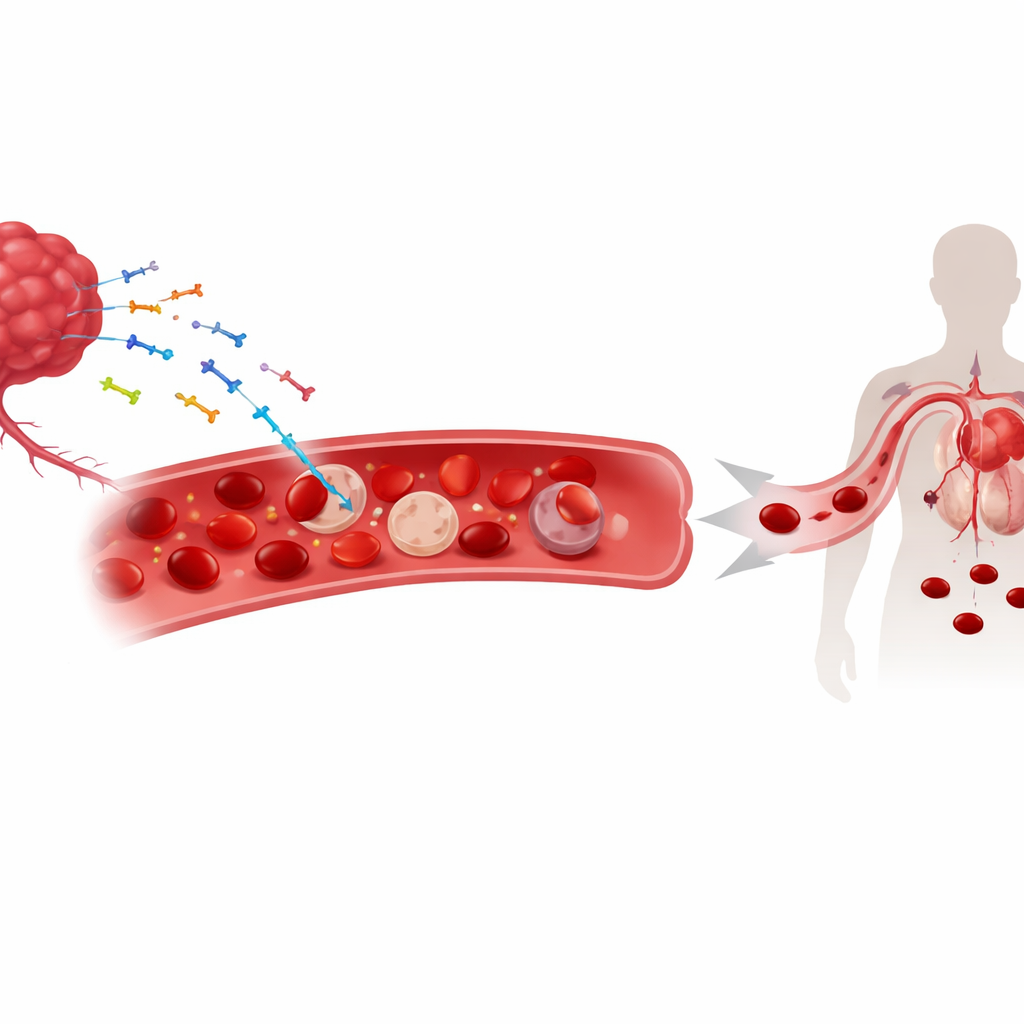
Свободная ДНК опухоли в кровотоке
По мере роста опухоли она сбрасывает фрагменты своего генетического материала — как ядерной, так и митохондриальной ДНК — в циркуляцию. Эти кусочки «свободной» ДНК уже используются как биомаркеры для отслеживания рака. Исследователи обнаружили, что значительная часть этой опухолевой ДНК не просто плавает в плазме; она прикрепляется к поверхности эритроцитов. В модельных экспериментах на мышах с опухолями легких, кожи и толстой кишки, а также у пациентов с несколькими солидными опухолями, более высокие уровни ДНК, связанной с эритроцитами, тесно коррелировали с низким уровнем гемоглобина и более тяжелой анемией. Эта связь не наблюдалась при неонкологической анемии, что указывает на то, что связывание ДНК — отличительная особенность именно ракового состояния, а не общее следствие низкого числа эритроцитов.
Главный удар приходится по молодым клеткам
Эритроциты рождаются в виде незрелых форм — ретикулоцитов, которые циркулируют недолго, пока завершают созревание. Команда обнаружила, что опухолевая ДНК избирательно поражает эти молодые клетки. С помощью флуоресцентных красителей и микроскопии у мышей и пациентов с раком показано, что более 95 процентов ДНК-позитивных эритроцитов несли маркеры незрелости. Эти покрытые ДНК ретикулоциты имели аномальную форму, шероховатые мембраны и сниженное содержание гемоглобина и гема — все признаки сбоев в их развитии. Когда связанная ДНК удалялась ферментами или смывами специальными растворами, клетки восстанавливали более нормальные характеристики и продвигались дальше по пути созревания.
От повреждения поверхности к преждевременному удалению
Почему ДНК на поверхности клетки так вредна? Исследование показывает, что она превращает молодые эритроциты в легкую мишень для уничтожения. Ретикулоциты с прикрепленной ДНК демонстрировали признаки «эриптоза» — запрограммированной гибели эритроцитов, включая всплески кальция внутри клетки и выведение на мембрану сигналов «съешь меня». В лабораторных и животных экспериментах макрофаги селезенки и печени — иммунные клетки, очищающие старые или поврежденные эритроциты — преимущественно поглощали ретикулоциты, покрытые ДНК, по сравнению с нормальными. Лечение эритроцитов или опухолевых мышей рестриктазой DNase I срезало связанную ДНК и резко уменьшало ускоренный клиренс, позволяя эритроцитам дольше сохраняться в кровообращении.
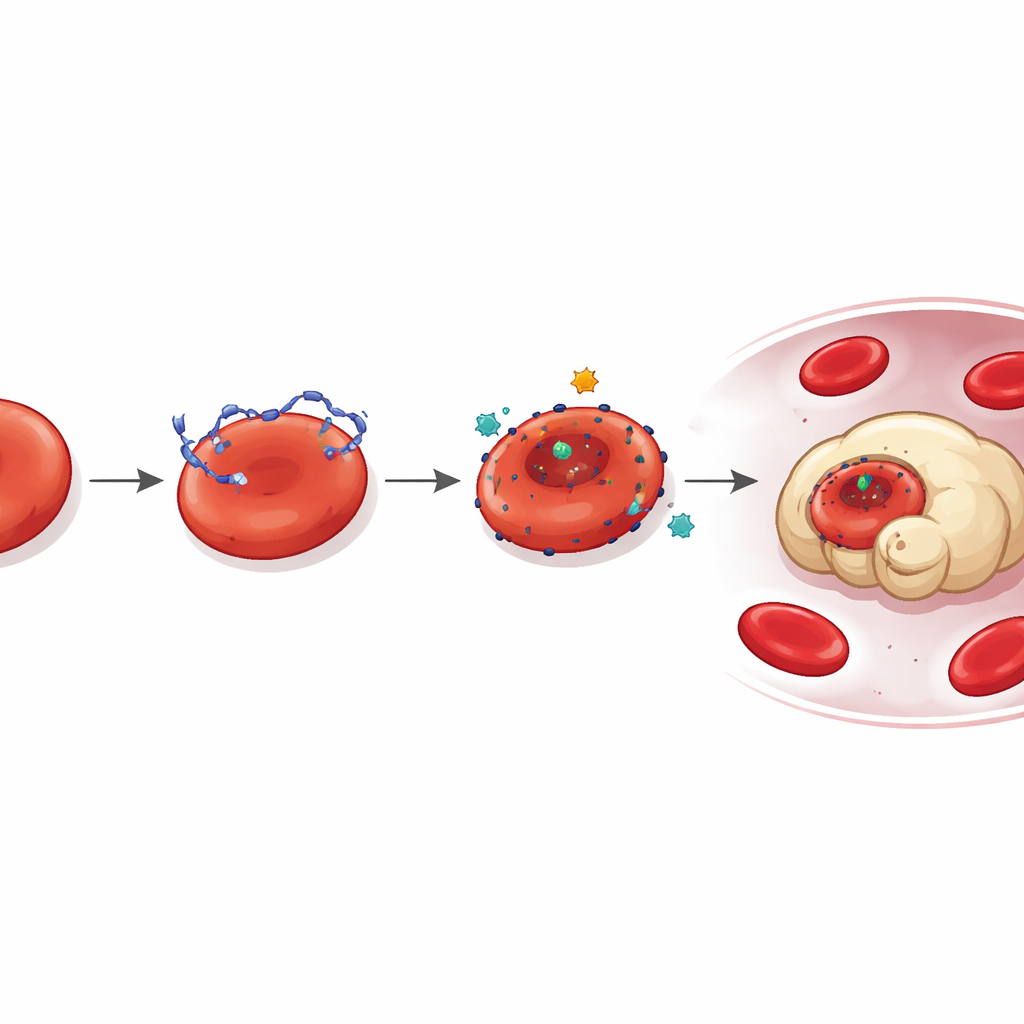
Скрытая точка прикрепления ДНК
Углубляясь, исследователи задали вопрос, как ДНК вообще закрепляется на ретикулоцитах. Протеомный анализ указал на LONP1 — белок, обычно локализующийся в митохондриях, — как на ключевой фактор. У мышей с опухолями и у пациентов с раком LONP1 оказался смещен на наружную поверхность циркулирующих ретикулоцитов. Там он служил высокоаффинным сайтом прикрепления для опухолевой ДНК. Клетки с наружным LONP1 связывали больше ДНК, были более деформированы и быстрее поглощались макрофагами. Блокирование активности LONP1 или снижение его уровня сокращало связывание ДНК и сопряженное повреждение, выявляя индуцированный опухолью путь, в котором неправильно локализованный LONP1 и свободная ДНК вместе саботируют молодые эритроциты.
Преобразование вредного сигнала в лечебную мишень
Поскольку многие современные подходы к лечению анемии при раке направлены лишь на увеличение производства эритроцитов, они могут быть грубыми инструментами с риском тромбозов или побочных эффектов на иммунную систему. Эта работа предлагает более точную стратегию: предотвратить разрушительное воздействие опухолевой ДНК на ретикулоциты изначально. У мышей монотерапия DNase I повышала уровни гемоглобина без ускорения роста опухоли, удаляя вредную ДНК с поверхности эритроцитов. В сочетании с эритропоэтином, гормоном, стимулирующим производство красных кровяных клеток, DNase I давала еще более выраженный синергетический эффект: образовывалось больше эритроцитов, и меньше из них уничтожалось преждевременно. Для пациентов этот ориентир на ДНК в патогенезе анемии при раке открывает путь к терапии, которая одновременно восстанавливает баланс красных кровяных клеток и избегает подрыва антиопухолевого иммунитета.
Цитирование: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Ключевые слова: анемия, связанная с раком, ДНК, происходящая из опухоли, ретикулоциты, удаление эритроцитов, терапия DNase I