Clear Sky Science · es
El ADN derivado del tumor provoca anemia asociada al cáncer al favorecer la eliminación de reticulocitos
Por qué importa la anemia relacionada con el cáncer
La anemia es un problema común y agotador en personas con cáncer. Cuando los glóbulos rojos son demasiado pocos o están debilitados, los pacientes sienten cansancio, falta de aliento y menor tolerancia a los tratamientos. Los médicos sabían desde hace tiempo que los tumores alteran de algún modo el equilibrio de los glóbulos rojos, pero las causas exactas eran poco claras. Este estudio descubre a un culpable sorprendente: fragmentos sueltos de ADN que se escapan de los tumores hacia el torrente sanguíneo y dañan directamente a los glóbulos rojos jóvenes, ofreciendo una nueva manera de entender y posiblemente tratar la anemia asociada al cáncer.
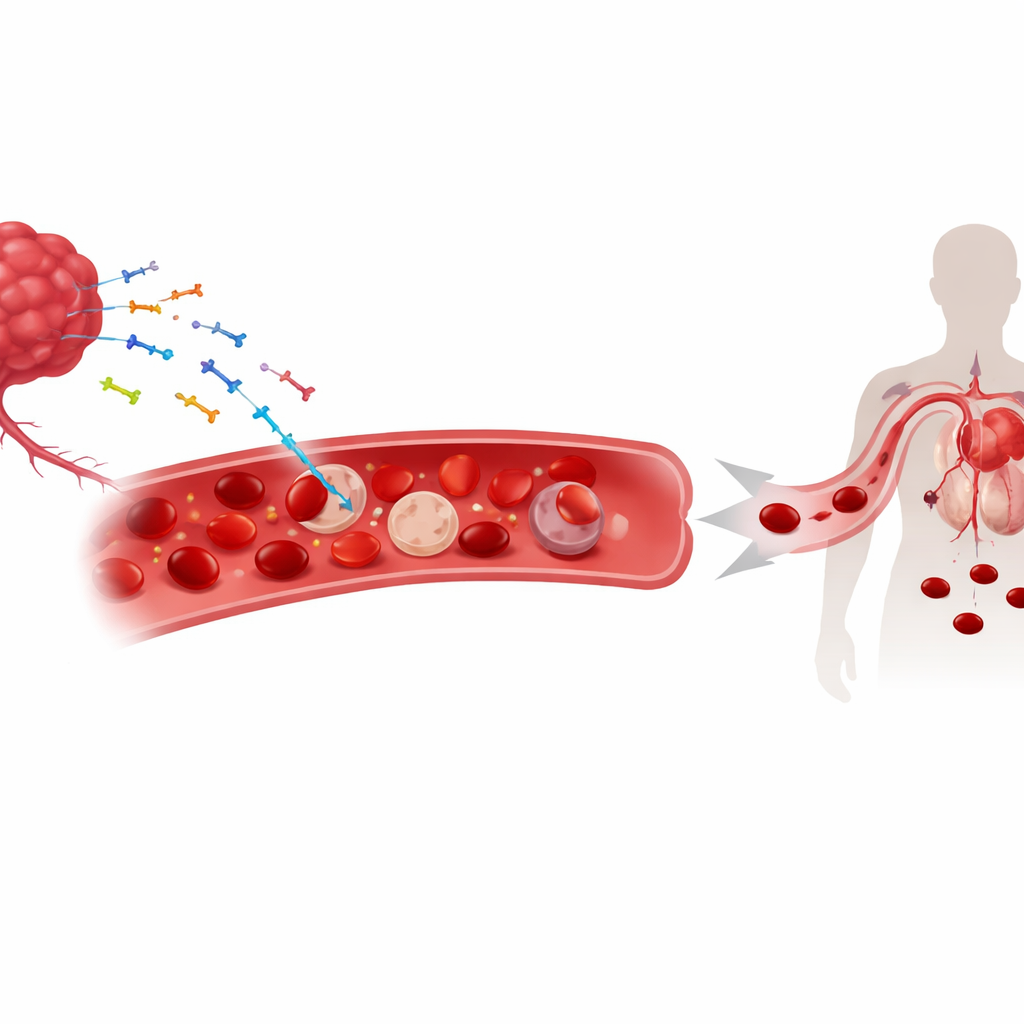
ADN tumoral errante en el torrente sanguíneo
A medida que los tumores crecen, desprenden fragmentos de su material genético—tanto ADN nuclear como mitocondrial—hacia la circulación. Estos fragmentos de “ADN libre” ya se utilizan como biomarcadores para monitorizar el cáncer. Los investigadores hallaron que una porción sustancial de este ADN derivado del tumor no se limita a flotar en el plasma; en lugar de eso, se adhiere a la superficie de los glóbulos rojos. En modelos murinos de cáncer de pulmón, piel y colon, y en pacientes con varios tumores sólidos, mayores cantidades de ADN unido a glóbulos rojos se correlacionaron estrechamente con niveles más bajos de hemoglobina y anemia más severa. Este vínculo no apareció en formas no tumorales de anemia, lo que sugiere que la unión de ADN es una característica distintiva del contexto canceroso y no una consecuencia general de la disminución del recuento de glóbulos rojos.
Las células rojas jóvenes son las más afectadas
Los glóbulos rojos nacen como formas inmaduras llamadas reticulocitos, que circulan brevemente mientras terminan de madurar. El equipo descubrió que el ADN derivado del tumor selecciona de forma preferente a estas células jóvenes. Mediante tintes fluorescentes y microscopía en ratones y pacientes con cáncer, mostraron que más del 95 por ciento de las células rojas positivas para ADN portaban marcadores de inmadurez. Estos reticulocitos recubiertos de ADN tenían forma anormal, membranas rugosas y contenido reducido de hemoglobina y hemo, todos signos de que su desarrollo había sido trastornado. Cuando el ADN adherido se eliminó con enzimas o se lavó con soluciones especiales, las células recuperaron características más normales y avanzaron en su vía de maduración.
Del daño superficial a la eliminación prematura
¿Por qué importa tanto el ADN en la superficie celular? El estudio muestra que convierte a los reticulocitos jóvenes en objetivos preferentes de destrucción. Los reticulocitos unidos al ADN exhibieron señales de “eritoptosis”, un proceso programado de muerte para los glóbulos rojos, incluyendo oleadas de calcio intracelular y exposición de señales de “cómeme” en la membrana. En experimentos de laboratorio y animales, los macrófagos del bazo y del hígado—células inmunitarias que eliminan glóbulos rojos envejecidos o dañados—engloberon preferentemente a los reticulocitos recubiertos de ADN frente a los normales. Tratar los glóbulos rojos o a ratones portadores de tumores con la enzima que corta ADN, DNasa I, eliminó el ADN adherido y redujo drásticamente esta eliminación acelerada, permitiendo que los glóbulos rojos permanecieran más tiempo en circulación.
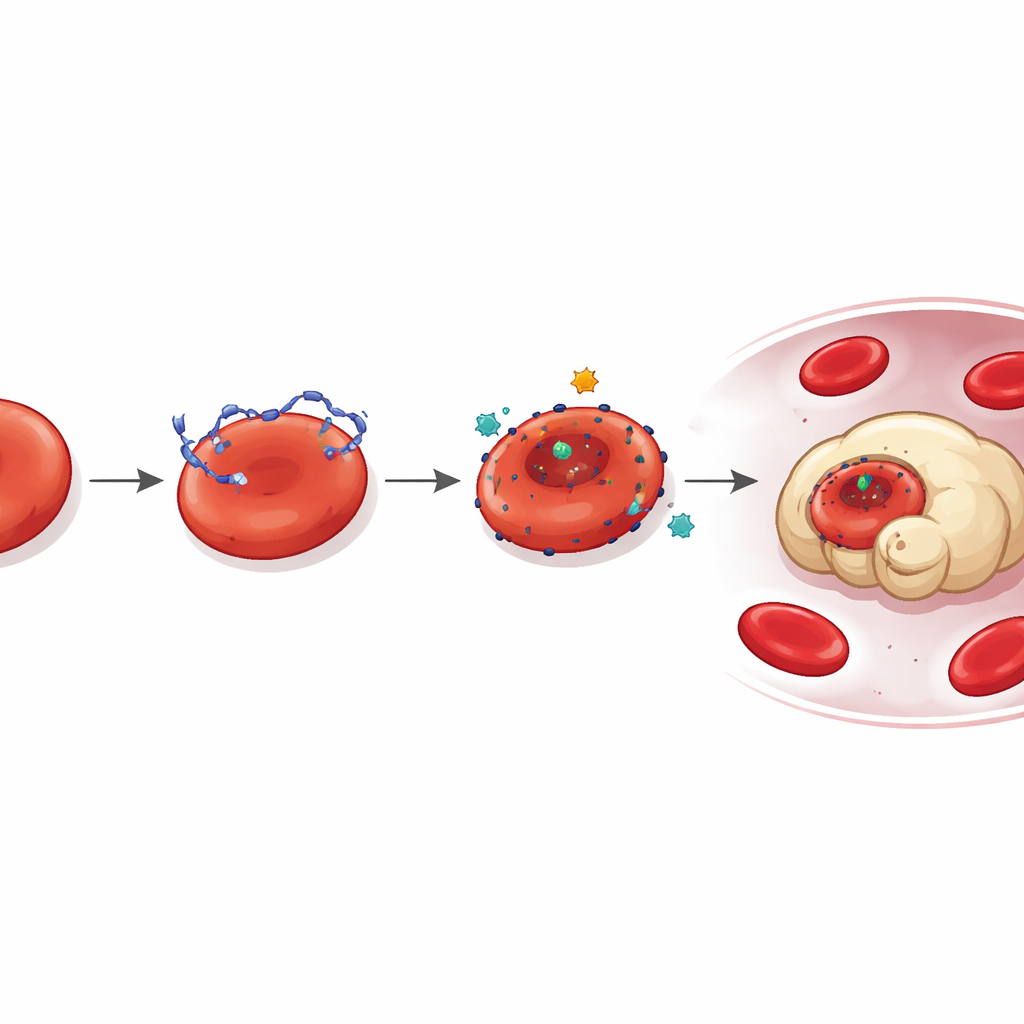
Un sitio oculto de anclaje para el ADN
Investigando más a fondo, los autores preguntaron cómo se fija el ADN a los reticulocitos en primer lugar. El análisis proteómico señaló a LONP1, una proteína normalmente localizada en mitocondrias, como un actor clave. En ratones con tumores y en pacientes con cáncer, LONP1 se deslocalizó hacia la superficie externa de los reticulocitos circulantes. Allí actuó como un sitio de anclaje de alta afinidad para el ADN derivado del tumor. Las células con LONP1 en la superficie unieron más ADN, mostraron mayor deformidad y fueron fagocitadas más rápidamente por los macrófagos. Bloquear la actividad de LONP1 o reducir sus niveles disminuyó la unión de ADN y el daño resultante, revelando una vía inducida por el tumor en la que LONP1 mal ubicado y el ADN errante colaboran para sabotear a los glóbulos rojos jóvenes.
Convertir una señal dañina en un objetivo terapéutico
Puesto que muchos tratamientos actuales para la anemia relacionada con el cáncer se centran únicamente en producir más glóbulos rojos, pueden ser herramientas toscas que conllevan riesgos como coágulos sanguíneos o efectos indeseados sobre el sistema inmune. Este trabajo sugiere un enfoque más preciso: impedir que el ADN derivado del tumor destruya a los reticulocitos desde el principio. En ratones, la terapia con DNasa I por sí sola elevó los niveles de hemoglobina sin acelerar el crecimiento tumoral al eliminar el ADN perjudicial de las superficies celulares. Cuando se combinó con eritropoyetina, una hormona que estimula la producción de glóbulos rojos, la DNasa I produjo mejoras sinérgicas aún mayores: se generaron más glóbulos rojos y se destruyeron menos prematuramente. Para los pacientes, esta visión centrada en el ADN de la anemia asociada al cáncer abre la puerta a terapias que restauren simultáneamente el equilibrio de los glóbulos rojos y eviten socavar la inmunidad antitumoral.
Cita: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Palabras clave: anemia asociada al cáncer, ADN derivado del tumor, reticulocitos, eliminación de glóbulos rojos, terapia con DNasa I