Clear Sky Science · de
Vom Tumor stammende DNA treibt krebsassoziierte Anämie voran, indem sie Retikulozytenabbau fördert
Warum krebsbedingte Anämie wichtig ist
Anämie ist ein häufiges und zermürbendes Problem bei Menschen mit Krebs. Wenn die roten Blutkörperchen zu wenige oder zu schwach sind, fühlen sich Patientinnen und Patienten müde, kurzatmig und weniger in der Lage, eine Behandlung zu tolerieren. Ärztinnen und Ärzte wissen schon lange, dass Tumoren auf irgendeine Weise das Gleichgewicht der roten Blutkörperchen stören, doch die genauen Gründe waren unklar. Diese Studie legt einen überraschenden Täter offen: lose DNA‑Fragmente, die aus Tumoren in den Blutkreislauf entweichen und junge rote Blutkörperchen direkt schädigen — ein neuer Ansatz, um krebsassoziierte Anämie zu verstehen und möglicherweise zu behandeln.
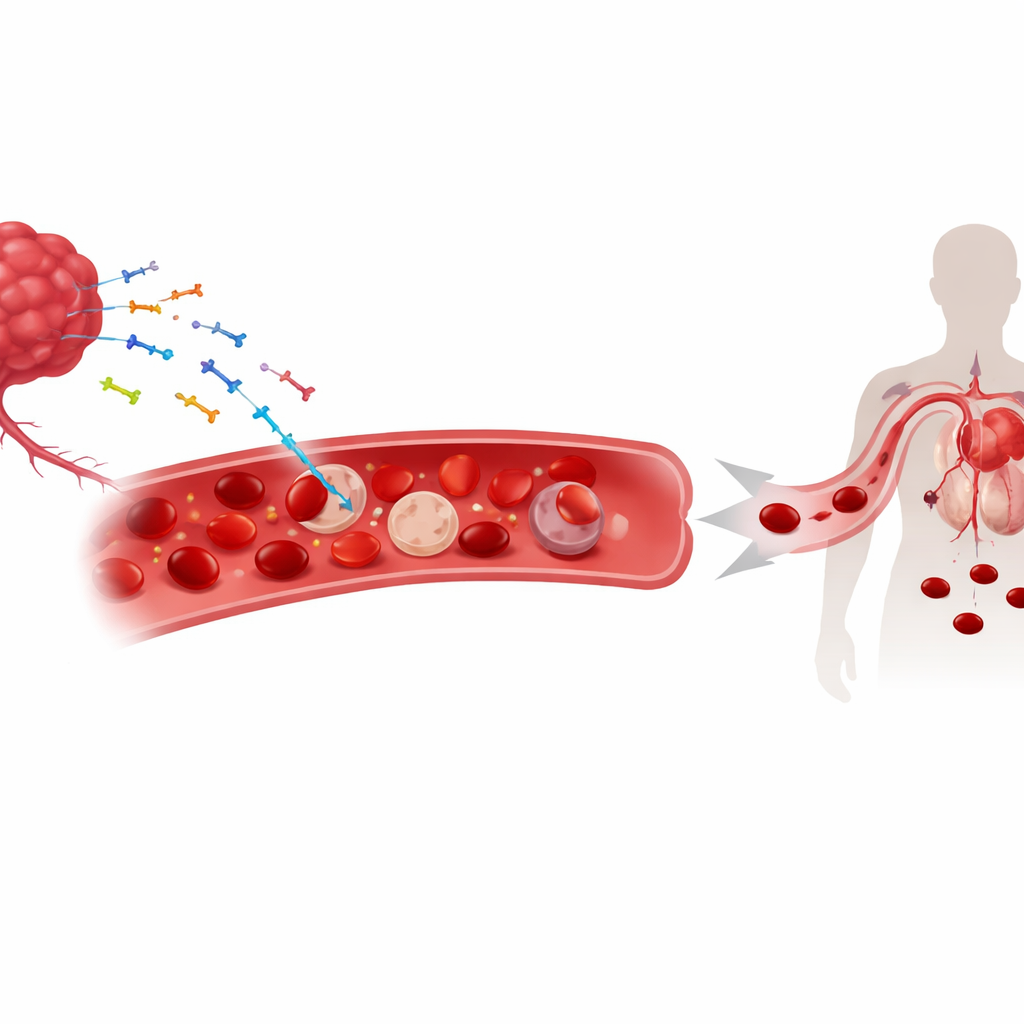
Umherirrende Tumor‑DNA im Blutkreislauf
Wenn Tumoren wachsen, schleudern sie Fragmente ihres genetischen Materials – sowohl nukleäre als auch mitochondriale DNA – in die Zirkulation. Diese Stücke „zellfreier“ DNA werden bereits als Biomarker zur Überwachung von Krebs verwendet. Die Forschenden fanden heraus, dass ein erheblicher Teil dieser tumorausgehenden DNA nicht einfach im Plasma treibt; stattdessen haftet sie an der Oberfläche roter Blutkörperchen. In Mausmodellen von Lungen‑, Haut‑ und Darmtumoren und bei Patientinnen und Patienten mit mehreren soliden Tumoren korrelierten höhere Mengen an an Erythrozyten gebundener DNA eng mit niedrigeren Hämoglobinwerten und schwererer Anämie. Dieser Zusammenhang trat bei nicht‑tumorbedingten Anämien nicht auf, was nahelegt, dass DNA‑Bindung ein charakteristisches Merkmal des Krebsfalls und keine allgemeine Folge niedriger Erythrozytenzahlen ist.
Junge rote Zellen sind besonders betroffen
Rote Blutkörperchen entstehen als unreife Formen, die Retikulozyten genannt werden und kurz im Blut kreisen, während sie weiter ausreifen. Das Team entdeckte, dass tumorausgehende DNA gezielt diese jungen Zellen angreift. Mit fluoreszierenden Farbstoffen und Mikroskopie in Mäusen und Krebspatienten zeigten sie, dass über 95 Prozent der DNA‑positiven Erythrozyten Marker der Unreife trugen. Diese DNA‑beschichteten Retikulozyten zeigten abnorme Form, aufgerautete Membranen sowie verringertes Hämoglobin‑ und Häm‑Gehalt — alles Zeichen einer gestörten Entwicklung. Wurde die gebundene DNA enzymatisch entfernt oder mit speziellen Lösungen abgespült, gewannen die Zellen wieder normalere Eigenschaften und schritten in ihrer Reifung weiter voran.
Von Oberflächenschaden zur vorzeitigen Eliminierung
Warum ist DNA an der Zelloberfläche so schädlich? Die Studie zeigt, dass sie junge rote Zellen zu bevorzugten Zielen der Vernichtung macht. An DNA gebundene Retikulozyten zeigten Kennzeichen der „Eryptose“, eines programmierten Todesprozesses für Erythrozyten, einschließlich intrazellulärer Kalziumanstiege und der Exposition von „Fress mich“‑Signalen auf der Membran. In Labor‑ und Tierversuchen verschlangen Milz‑ und Lebermakrophagen — Immunzellen, die gealterte oder beschädigte rote Zellen entfernen — bevorzugt DNA‑beschichtete Retikulozyten gegenüber normalen. Die Behandlung von Erythrozyten oder tumorbefallenen Mäusen mit dem DNA‑schneidenden Enzym DNase I entfernte die gebundene DNA und verringerte diese beschleunigte Eliminierung deutlich, wodurch die Lebensdauer der roten Zellen im Kreislauf erhöht wurde.
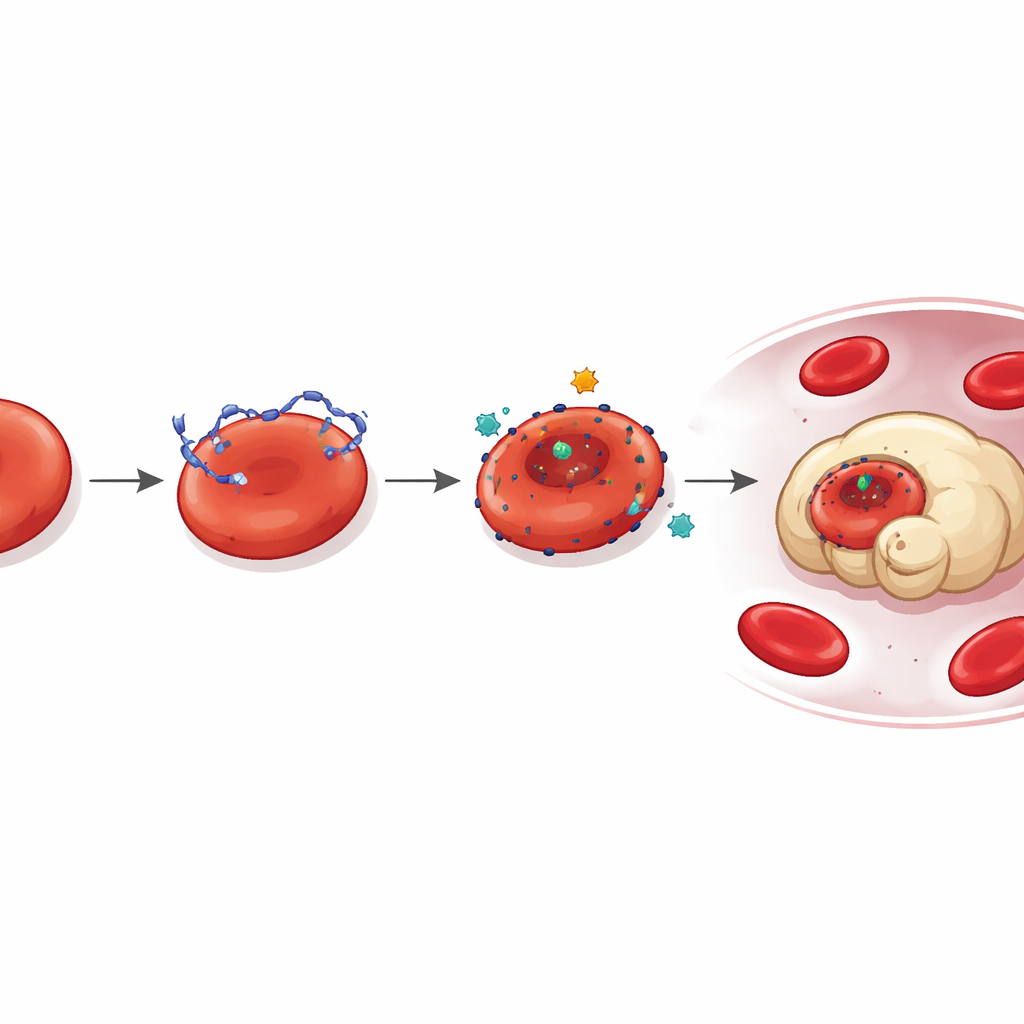
Eine verborgene Andockstelle für DNA
Bei tieferer Untersuchung fragten die Forschenden, wie DNA überhaupt an Retikulozyten haftet. Proteomische Analysen wiesen auf LONP1 hin, ein Protein, das normalerweise in Mitochondrien vorkommt, als Schlüsselakteur. Bei tumorbefallenen Mäusen und Krebspatienten wurde LONP1 fehllokalisiert und tauchte auf der Außenseite zirkulierender Retikulozyten auf. Dort fungierte es als hochaffine Andockstelle für tumorausgehende DNA. Zellen mit Oberflächen‑LONP1 banden mehr DNA, zeigten stärkere Deformität und wurden rascher von Makrophagen aufgenommen. Das Blockieren der LONP1‑Aktivität oder das Reduzieren seiner Menge verringerte die DNA‑Bindung und die daraus resultierende Schädigung und zeigte so einen tumorausgelösten Mechanismus, bei dem fehl positioniertes LONP1 und umherschweifende DNA zusammen junge rote Zellen sabotieren.
Ein schädliches Signal als therapeutisches Ziel
Da viele aktuelle Behandlungen der krebsbedingten Anämie allein darauf abzielen, mehr rote Blutkörperchen zu produzieren, sind sie oft grobe Werkzeuge, die Risiken wie Blutgerinnsel oder unerwünschte Effekte auf das Immunsystem bergen. Diese Arbeit legt einen präziseren Ansatz nahe: verhindern, dass tumorausgehende DNA Retikulozyten überhaupt zerstört. Bei Mäusen erhöhte allein die DNase‑I‑Therapie die Hämoglobinwerte ohne das Tumorwachstum zu beschleunigen, indem schädliche DNA von den Zelloberflächen entfernt wurde. In Kombination mit Erythropoetin, einem Hormon, das die Bildung roter Blutkörperchen fördert, erzielte DNase I noch stärkere, synergistische Effekte: Es wurden mehr rote Zellen gebildet und weniger vorzeitig zerstört. Für Patientinnen und Patienten eröffnet diese DNA‑zentrierte Sichtweise der krebsassoziierten Anämie Wege zu Therapien, die gleichzeitig das Gleichgewicht der roten Blutkörperchen wiederherstellen und die antitumorale Immunität nicht untergraben.
Zitation: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Schlüsselwörter: krebsassoziierte Anämie, vom Tumor stammende DNA, Retikulozyten, Abbau roter Blutkörperchen, DNase‑I‑Therapie