Clear Sky Science · fr
L’ADN d’origine tumorale provoque l’anémie associée au cancer en favorisant l’élimination des réticulocytes
Pourquoi l’anémie liée au cancer importe
L’anémie est un problème fréquent et épuisant chez les personnes atteintes de cancer. Quand les globules rouges sont trop peu nombreux ou trop fragiles, les patients se sentent fatigués, essoufflés et moins capables de tolérer les traitements. Les médecins savent depuis longtemps que les tumeurs perturbent d’une manière ou d’une autre l’équilibre des globules rouges, mais les mécanismes exacts sont restés flous. Cette étude met en lumière un coupable surprenant : des fragments d’ADN qui s’échappent des tumeurs dans la circulation sanguine et endommagent directement les jeunes globules rouges, offrant une nouvelle façon de comprendre et éventuellement de traiter l’anémie associée au cancer.
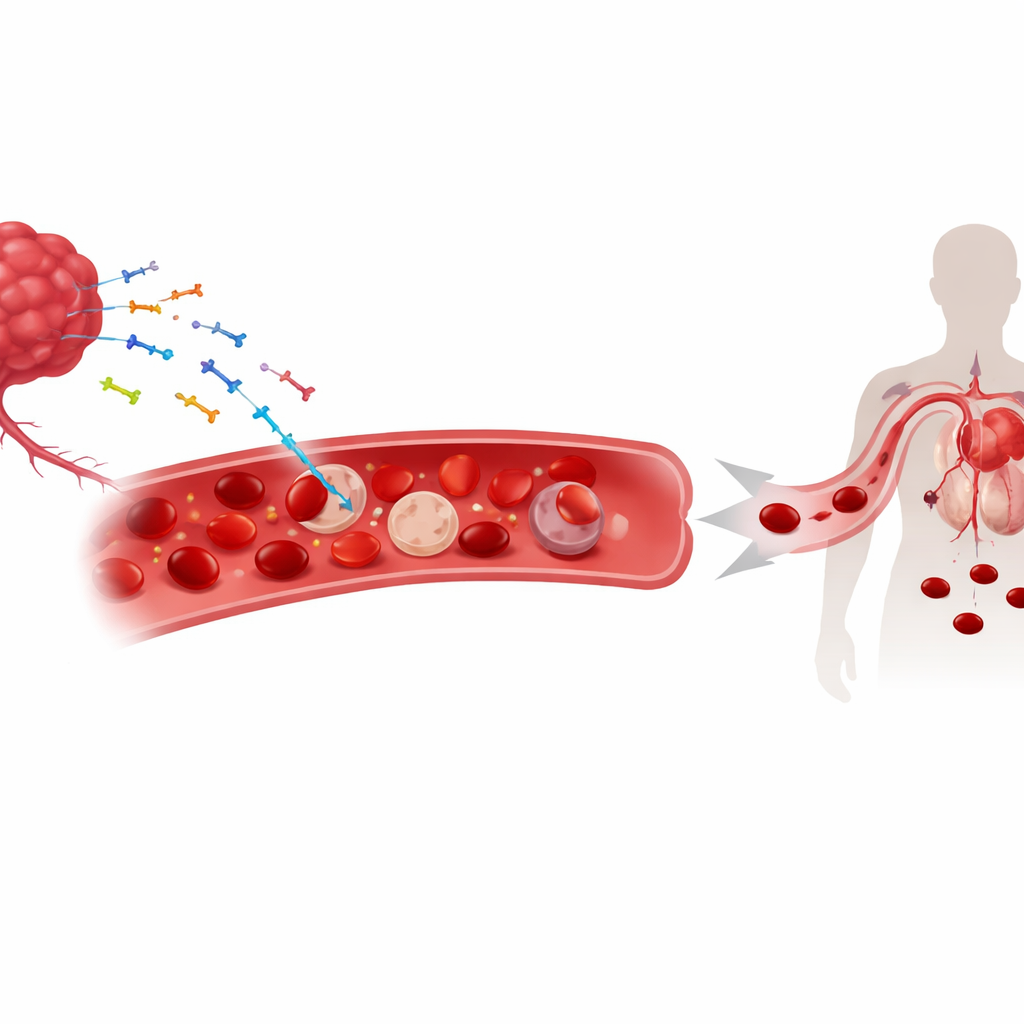
ADN tumoral errant dans la circulation
À mesure que les tumeurs croissent, elles libèrent des fragments de leur matériel génétique — ADN nucléaire et mitochondrial — dans la circulation. Ces fragments d’« ADN libre » sont déjà utilisés comme biomarqueurs pour suivre le cancer. Les chercheurs ont découvert qu’une part importante de cet ADN d’origine tumorale ne flotte pas seulement dans le plasma ; elle se fixe à la surface des globules rouges. Chez des modèles murins de cancers du poumon, de la peau et du côlon et chez des patients atteints de plusieurs tumeurs solides, des quantités plus élevées d’ADN lié aux globules rouges étaient étroitement corrélées à des taux d’hémoglobine plus bas et à une anémie plus sévère. Ce lien n’apparaissait pas dans des formes d’anémie non liées au cancer, ce qui suggère que la fixation de l’ADN est une caractéristique spécifique du contexte tumoral plutôt qu’une conséquence générale d’une baisse du nombre de globules rouges.
Les jeunes globules rouges prennent le coup
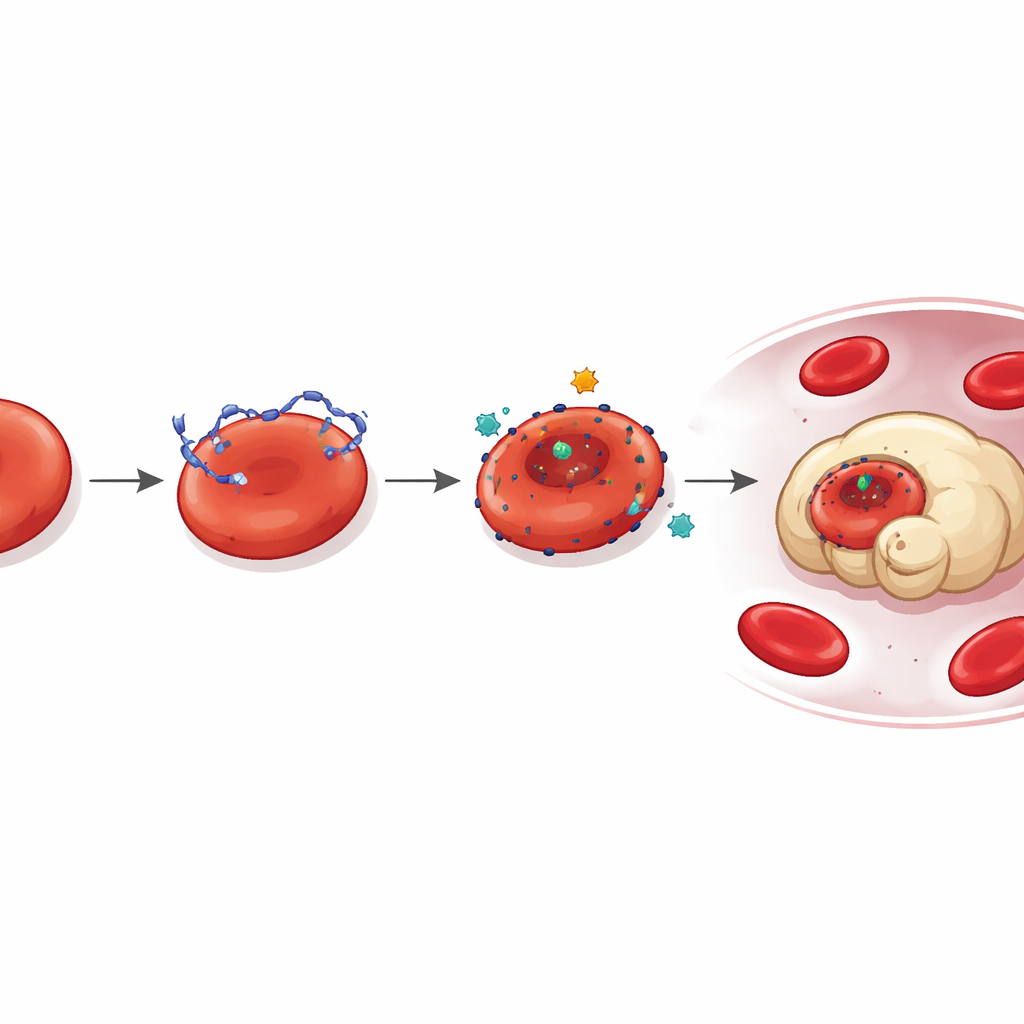
Les globules rouges naissent sous une forme immature appelée réticulocytes, qui circulent brièvement le temps de terminer leur maturation. L’équipe a découvert que l’ADN d’origine tumorale cible de manière sélective ces cellules jeunes. À l’aide de colorants fluorescents et de la microscopie chez la souris et chez des patients atteints de cancer, ils ont montré que plus de 95 % des globules rouges positifs pour l’ADN portaient des marqueurs d’immaturité. Ces réticulocytes enrobés d’ADN présentaient une morphologie anormale, des membranes rugueuses et un contenu réduit en hémoglobine et en hème, autant de signes que leur développement avait été perturbé. Quand l’ADN lié était éliminé par des enzymes ou éliminé par des lavages spéciaux, les cellules retrouvaient des caractéristiques plus normales et progressaient davantage le long de leur voie de maturation.
Des dommages de surface à l’élimination prématurée
Pourquoi l’ADN à la surface des cellules a-t-il autant d’importance ? L’étude montre qu’il transforme les jeunes globules rouges en cibles privilégiées pour la destruction. Les réticulocytes liés à l’ADN présentaient des signes d’« éryptose », un processus de mort programmée des globules rouges, incluant des pics de calcium intracellulaire et l’exposition de signaux « mange-moi » à la surface membranaire. Dans des expériences in vitro et chez l’animal, les macrophages de la rate et du foie — cellules immunitaires qui éliminent les globules rouges âgés ou endommagés — phagocytaient préférentiellement les réticulocytes enrobés d’ADN plutôt que les cellules normales. Le traitement des globules rouges ou des souris porteuses de tumeurs par l’enzyme coupant l’ADN DNase I a détaché l’ADN lié et réduit fortement cette élimination accélérée, permettant aux globules rouges de persister plus longtemps en circulation.
Un site d’ancrage caché pour l’ADN
En creusant plus avant, les chercheurs se sont demandé comment l’ADN s’accrochait aux réticulocytes. L’analyse protéomique a pointé LONP1, une protéine normalement localisée dans les mitochondries, comme un acteur clé. Chez les souris porteuses de tumeurs et chez les patients, LONP1 se retrouvait mal localisée à la surface externe des réticulocytes circulants. Là, elle agissait comme un site d’ancrage à haute affinité pour l’ADN d’origine tumorale. Les cellules avec LONP1 à la surface fixaient plus d’ADN, montraient une plus grande déformation et étaient ingérées plus rapidement par les macrophages. Bloquer l’activité de LONP1 ou réduire son niveau diminuait la fixation de l’ADN et les dommages qui en résultent, révélant une voie induite par la tumeur dans laquelle LONP1 mal positionnée et ADN errant sabotent ensemble les jeunes globules rouges.
Transformer un signal nuisible en une cible thérapeutique
Parce que de nombreux traitements actuels de l’anémie liée au cancer se concentrent uniquement sur la production de davantage de globules rouges, ils peuvent être des outils lourds comportant des risques tels que des caillots sanguins ou des effets indésirables sur le système immunitaire. Ce travail suggère une approche plus précise : empêcher l’ADN d’origine tumorale de détruire les réticulocytes dès le départ. Chez la souris, la thérapie par DNase I à elle seule a augmenté les taux d’hémoglobine sans accélérer la croissance tumorale en éliminant l’ADN nocif à la surface des globules rouges. Associée à l’érythropoïétine, une hormone qui stimule la production de globules rouges, la DNase I a produit des améliorations encore plus fortes et synergiques : davantage de globules rouges étaient produits et moins étaient détruits prématurément. Pour les patients, cette vision centrée sur l’ADN de l’anémie associée au cancer ouvre la porte à des thérapies qui rétablissent l’équilibre des globules rouges tout en évitant d’affaiblir l’immunité anti-tumorale.
Citation: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Mots-clés: anémie associée au cancer, ADN d’origine tumorale, réticulocytes, élimination des globules rouges, thérapie par DNase I