Clear Sky Science · nl
Tumorafgeleide DNA veroorzaakt anemie geassocieerd met kanker door reticulocyten te bevorderen clearance
Waarom anemie bij kanker ertoe doet
Anemie is een veelvoorkomend en uitputtend probleem bij mensen met kanker. Wanneer er te weinig of te zwakke rode bloedcellen zijn, voelen patiënten zich moe, kortademig en minder in staat om behandelingen te verdragen. Artsen wisten al langer dat tumoren het evenwicht van rode bloedcellen in het lichaam op de een of andere manier verstoren, maar de precieze oorzaken waren onduidelijk. Deze studie onthult een verrassende schuldige: losse stukjes DNA die uit tumoren ontsnappen naar de bloedbaan en rechtstreeks jonge rode bloedcellen beschadigen, wat een nieuw inzicht biedt en mogelijk nieuwe behandelrichtingen voor anemie geassocieerd met kanker opent.
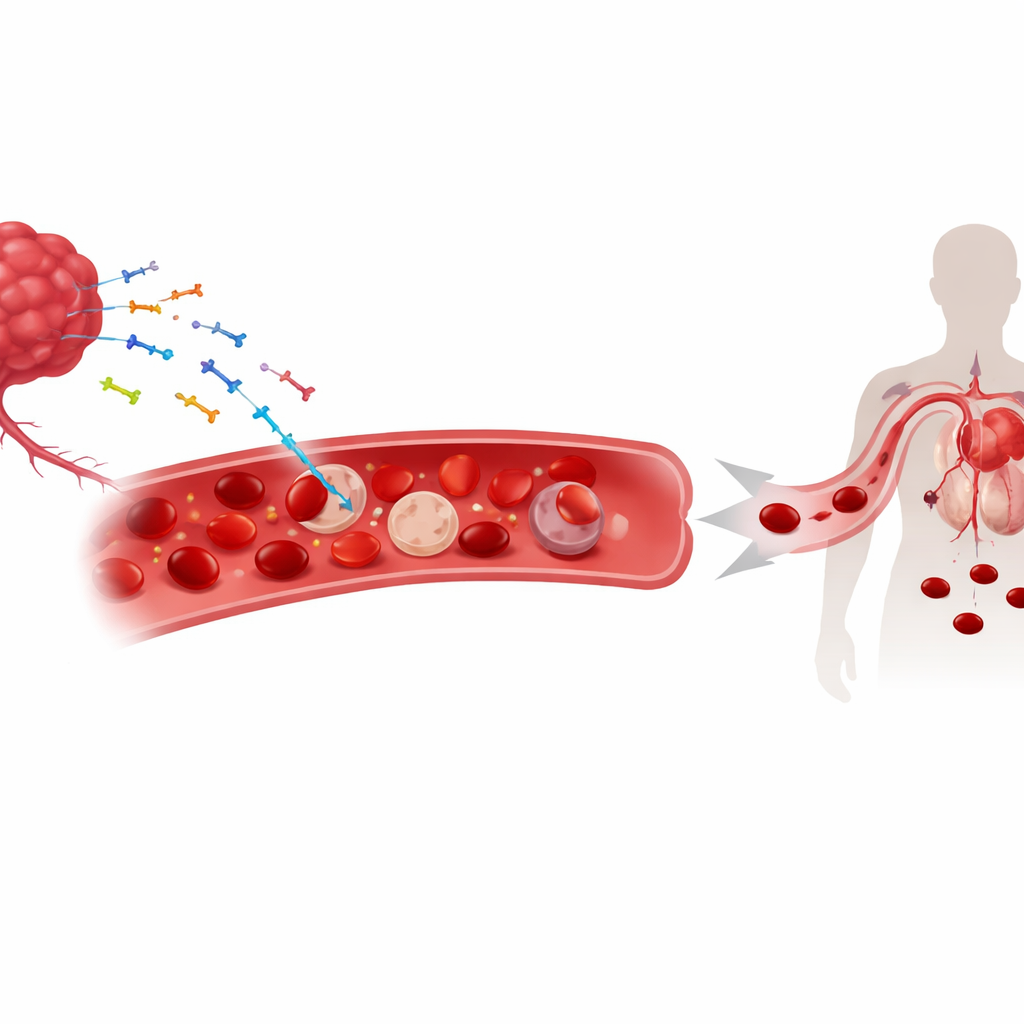
Loslopend tumor-DNA in de bloedbaan
Terwijl tumoren groeien, laten ze fragmenten van hun genetisch materiaal—zowel nucleair als mitochondriaal DNA—los in de circulatie. Deze stukjes “celvrij” DNA worden al gebruikt als biomarkers om kanker te volgen. De onderzoekers vonden dat een substantieel deel van dit tumorafgeleide DNA niet alleen in het plasma zweeft; het hecht zich in plaats daarvan aan het oppervlak van rode bloedcellen. In muismodellen van long-, huid- en darmkankers en bij patiënten met verschillende solide tumoren correleerden hogere hoeveelheden aan rode bloedcellen gebonden DNA sterk met lagere hemoglobinewaarden en ernstigere anemie. Deze koppeling leek niet aanwezig te zijn bij niet-kankergerelateerde vormen van anemie, wat suggereert dat DNA-binding een onderscheidend kenmerk is van de kankersituatie en niet louter een algemeen gevolg van lage aantallen rode bloedcellen.
Jonge rode cellen krijgen de klap
Rode bloedcellen ontstaan als onrijpe vormen die reticulocyten worden genoemd; zij circuleren kort terwijl ze hun rijping voltooien. Het team ontdekte dat tumorafgeleide DNA selectief deze jonge cellen aantast. Met behulp van fluorescente kleurstoffen en microscopie in muizen en kankerpatiënten toonden ze aan dat meer dan 95 procent van de DNA-positieve rode cellen merkers van onrijpheid droeg. Deze met DNA gecoate reticulocyten vertoonden een abnormale vorm, ruwere membranen en verminderde hemoglobine- en heeminhoud, allemaal tekenen dat hun ontwikkeling was verstoord. Wanneer het gebonden DNA werd verwijderd met enzymen of afgespoeld met speciale oplossingen, kregen de cellen meer normale eigenschappen terug en zetten ze hun rijpingspad verder voort.
Van oppervlaktebeschadiging naar voortijdige verwijdering
Waarom is DNA op het celoppervlak zo belangrijk? De studie laat zien dat het jonge rode cellen verandert in aantrekkelijke doelwitten voor vernietiging. Aan DNA gebonden reticulocyten vertoonden kenmerken van “eryptose”, een geprogrammeerd doodproces voor rode cellen, inclusief calciumpiekjes binnenin de cel en blootlegging van “eet mij”-signalen op het membraan. In laboratorium- en proefdierexperimenten aten milt- en levermacrofagen—immuuncellen die oude of beschadigde rode cellen opruimen—voorkeurig aan DNA-gecoate reticulocyten in plaats van normale cellen. Behandeling van rode cellen of van muizen met tumoren met het DNA-snijvende enzym DNase I verwijderde het gebonden DNA en verminderde deze versnelde verwijdering sterk, waardoor rode cellen langer in de circulatie bleven.
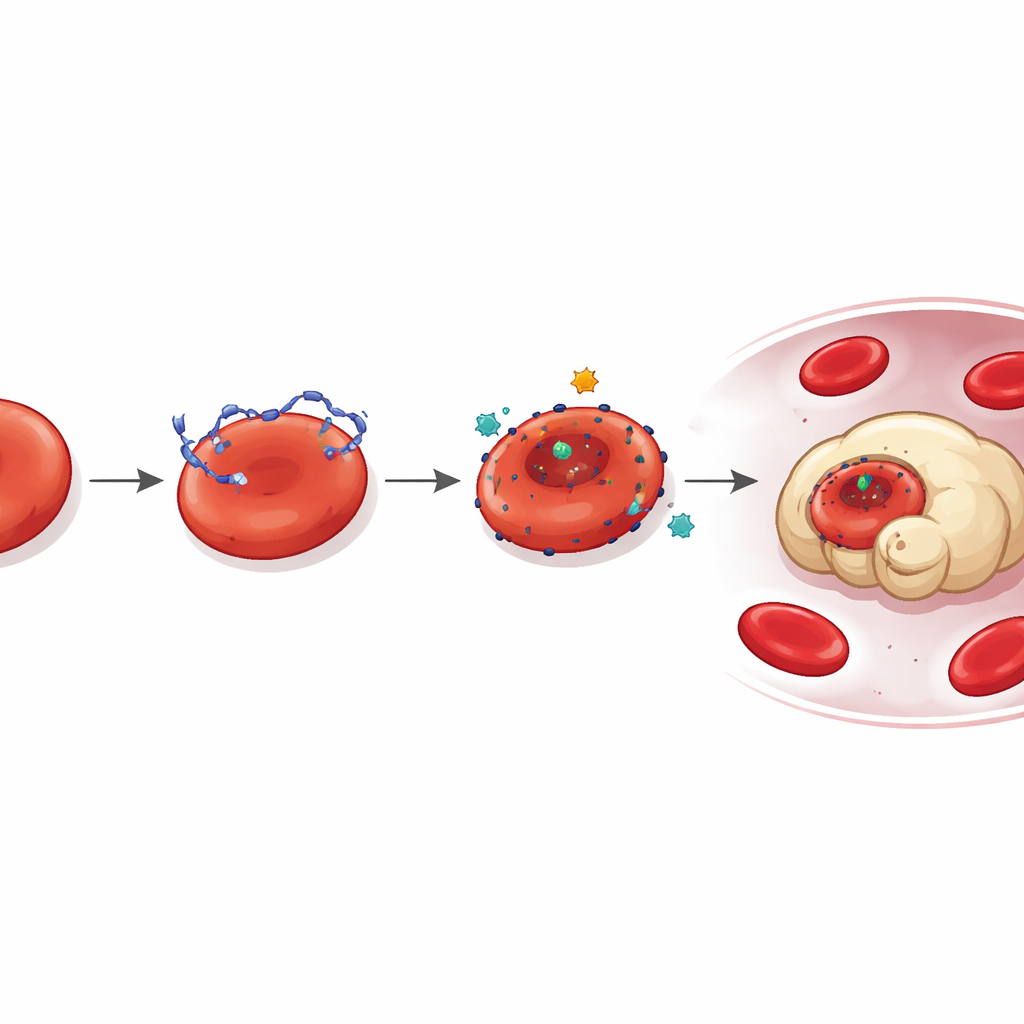
Een verborgen aanlegplaats voor DNA
Dieper gravend vroegen de onderzoekers zich af hoe DNA zich in de eerste plaats aan reticulocyten vastklampt. Proteomische analyse wees op LONP1, een eiwit dat normaal gesproken in de mitochondriën voorkomt, als een belangrijke speler. Bij muizen met tumoren en bij kankerpatiënten werd LONP1 verkeerd gelokaliseerd aan de buitenkant van circulerende reticulocyten. Daar fungeerde het als een hoge-affiniteitsaangrijpingsplaats voor tumorafgeleide DNA. Cellen met oppervlakte-LONP1 binden meer DNA, vertonen grotere vervorming en werden sneller opgegeten door macrofagen. Het blokkeren van LONP1-activiteit of het verminderen van de hoeveelheid van dit eiwit verminderde DNA-binding en de daaruit voortvloeiende schade, wat een tumorgemedieerde route blootlegt waarbij verkeerd gepositioneerde LONP1 en loslopend DNA samen jonge rode cellen saboteren.
Van schadelijk signaal naar behandelbaar doel
Aangezien veel huidige behandelingen voor anemie bij kanker zich alleen richten op het produceren van meer rode bloedcellen, kunnen ze grove instrumenten zijn met risico’s zoals bloedstolsels of ongewenste effecten op het immuunsysteem. Dit werk suggereert een preciezere benadering: voorkom dat tumorafgeleide DNA reticulocyten in de eerste plaats beschadigt. Bij muizen verhoogde DNase I-therapie alleen al de hemoglobinewaarden zonder de tumorgroei te versnellen door schadelijk DNA van rode celoppervlakken te verwijderen. In combinatie met erytropoëtine, een hormoon dat de aanmaak van rode bloedcellen stimuleert, produceerde DNase I nog sterkere, synergistische verbeteringen: er werden meer rode cellen aangemaakt en er werden minder voortijdig vernietigd. Voor patiënten opent deze op DNA gerichte kijk op anemie geassocieerd met kanker de deur naar therapieën die tegelijk het evenwicht van rode bloedcellen herstellen en het antitumorimmuniteit niet ondermijnen.
Bronvermelding: Yuan, T., Liu, X., Wu, Y. et al. Tumor-derived DNA drives cancer-associated anemia by promoting reticulocyte clearance. Sig Transduct Target Ther 11, 152 (2026). https://doi.org/10.1038/s41392-026-02674-9
Trefwoorden: anemie geassocieerd met kanker, tumorafgeleide DNA, reticulocyten, vernietiging van rode bloedcellen, DNase I-therapie