Clear Sky Science · zh
通过提高血管紧张素转换酶(ACE)表达的生物工程iPSC来源人巨噬细胞可抑制实体瘤生长
将我们自身的防御者转向抗癌
癌症免疫治疗已改善了部分患者的预后,但许多肿瘤仍能找到隐匿或耗损免疫系统的方法。本研究探索了一种在实验室中改造巨噬细胞的新途径,使其对实体瘤更具攻击性。研究表明,未来医生或可向患者输注定制免疫细胞,这些细胞无需识别某一特定肿瘤标志物便能对多种癌症发起攻击。
巨噬细胞在癌症中的重要性
巨噬细胞是既清道夫又前线战士的白细胞。在许多实体瘤内,它们数量充足——但常常处于错误的状态。它们并非攻击者,而是陷入一种“修复者”状态,反而助长肿瘤生长、转移并逃避免疫监视。作者认为,如果能可靠地将巨噬细胞推向一种强烈的炎性状态并在肿瘤内维持这种状态,这些细胞既可直接杀伤癌细胞,也能动员其他免疫战士,如T细胞和自然杀伤(NK)细胞。
借用一种调血压的酶来增强免疫力
研究团队聚焦于血管紧张素转换酶(ACE),该酶以调节血压和作为常用心脏药物靶点而闻名。此前小鼠研究提示,髓系细胞(包括巨噬细胞)中ACE水平提高会增强其抗感染和抗肿瘤能力。这项研究将该想法移植到人体体系。研究者使用诱导多能干细胞——将成年细胞重编程回干细胞样状态——并插入一个基因开关,可通过常用抗生素多西环素上调或下调ACE表达。由这些工程化干细胞生成了大量按需供应的巨噬细胞,他们称之为ACE‑iMac,这是一个可扩展的平台。
在实验室构建超充能巨噬细胞
当ACE开关被打开时,产生的ACE‑iMac细胞在形态和功能上与常规实验室培养的巨噬细胞显著不同。它们分泌了更多炎性信号,产生大量活性氧和一氧化氮——这些化学武器会损伤肿瘤细胞——并显示出与高度活化“类似M1”状态相关的基因活动模式。同时,它们降低了与抑制性、助瘤状态相关的分子产生。在培养皿中,ACE‑iMac细胞比对照巨噬细胞更有效地抑制黑色素瘤、三阴性乳腺癌和耐药头颈癌细胞的生长。
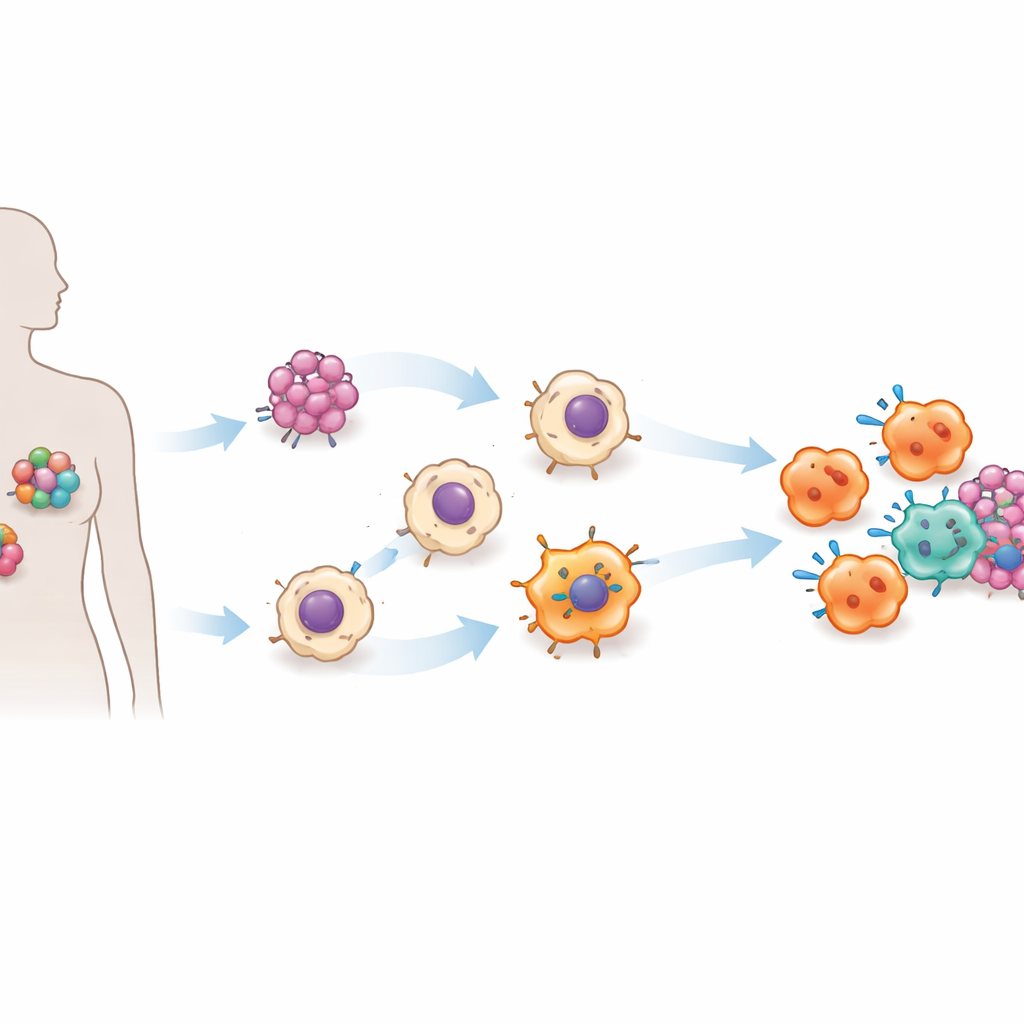
抑制肿瘤并激活其他免疫细胞
关键测试在带有人人源肿瘤的小鼠模型中进行。当ACE‑iMac细胞直接注入实体瘤时,这些肿瘤显著缩小——与接受普通巨噬细胞的肿瘤相比,体积大约缩小四分之三或更多。该结果在黑色素瘤、乳腺癌和头颈癌模型中均成立。肿瘤内部,ACE‑iMac细胞表现出强烈的炎性特征,并伴随更活跃的NK细胞;在具有人体免疫系统功能的特殊人源化小鼠中,还观察到更强效的人类细胞毒性T细胞。有趣的是,其他免疫细胞的总数并未发生显著变化;相反,它们变得更为活化,这表明ACE‑iMac细胞更像是现场教练,激发更广泛的免疫反应,而不仅仅是增加作战人数。
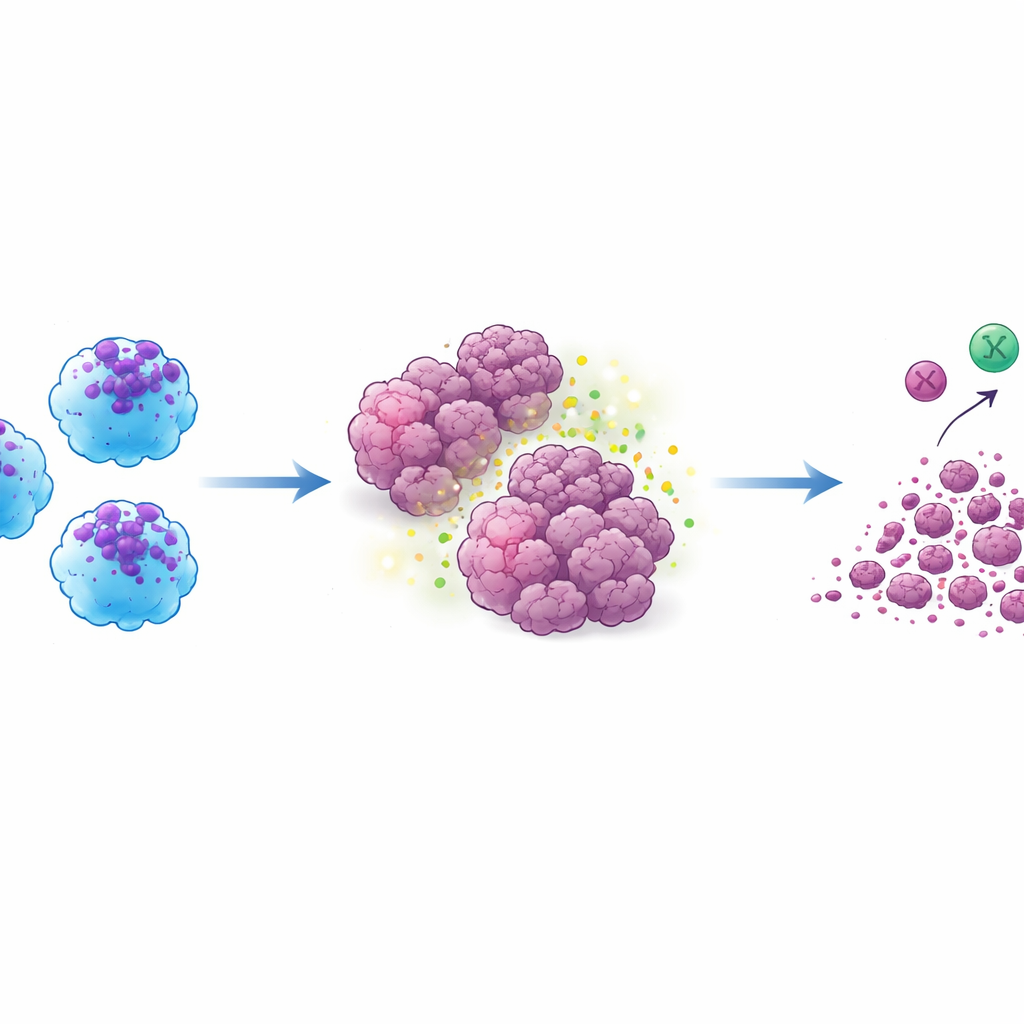
解码内在机制
为理解这种行为的驱动机制,研究者检查了ACE‑iMac细胞的全局基因活性。打开ACE后,增强了与经典巨噬细胞活化、细胞因子产生、抗原加工以及消化靶标的细胞“胃”(吞噬体)组装相关的网络。它还调节了有助于巨噬细胞向T细胞呈递肿瘤蛋白片段的通路,这可能解释了在人源化小鼠中更强的T细胞反应。在肿瘤样刺激下,ACE‑iMac细胞在代谢和分化相关基因上进一步获益,这些变化可能帮助它们在恶劣的肿瘤环境中保持活性,而不会耗竭或倒戈。
这对未来癌症护理意味着什么
对非专业读者而言,结论是作者构建了一种可控的、可再生来源的人巨噬细胞,这些细胞表现为高度聚焦的肿瘤猎手和免疫增强剂。通过仅在需要时使用外源药物提高ACE水平,他们可在原理上调整反应的强度和时机,从而可能提高安全性。尽管在用于患者之前仍需完成许多步骤——包括静脉给药测试、长期安全性评估以及与现有疗法的联合研究——这项工作指出了一类新的细胞治疗途径。ACE‑iMac细胞并非逐一针对单一肿瘤标志物,而是旨在广泛重置实体瘤内的免疫景观,可能使癌症对人体自身防御更可见且更脆弱。
引用: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
关键词: 癌症免疫治疗, 巨噬细胞, 诱导多能干细胞, 血管紧张素转换酶, 实体瘤