Clear Sky Science · pl
Bioinżynierowane ludzkie makrofagi pochodzące z iPSC z zwiększoną ekspresją enzymu konwertującego angiotensynę (ACE) hamują wzrost nowotworów litych
Skierowanie naszych własnych obrońców przeciwko rakowi
Immunoterapia nowotworów zmieniła perspektywy dla niektórych pacjentów, ale wiele guzów wciąż potrafi ukryć się przed układem odpornościowym lub go osłabić. Badanie to przedstawia nowy sposób „wzmocnienia” jednej z naturalnych linii obrony organizmu — makrofagów — przez przereprogramowanie ich w laboratorium tak, aby stały się znacznie bardziej agresywne wobec guzów litych. Praca sugeruje przyszłość, w której lekarze mogliby podawać pacjentom na zamówienie komórki odpornościowe atakujące szerokie spektrum nowotworów, bez konieczności rozpoznawania pojedynczego specyficznego markera guza.
Dlaczego makrofagi mają znaczenie w onkologii
Makrofagi to białe krwinki pełniące rolę zarówno sprzątaczy, jak i żołnierzy pierwszej linii. W wielu guzach litych są liczne — ale często działają w niewłaściwym trybie. Zamiast atakować, przechodzą w stan „leczący”, który faktycznie pomaga guzom rosnąć, przerzutować i unikać innych komórek odpornościowych. Autorzy wysnuli hipotezę, że jeśli uda się niezawodnie przesunąć makrofagi w kierunku silnie prozapalnego, „uderzeniowego” stanu i utrzymać je w nim wewnątrz guza, komórki te mogłyby bezpośrednio zabijać komórki nowotworowe i mobilizować innych bojowników odpornościowych, takich jak limfocyty T i komórki NK.
Wykorzystanie enzymu regulującego ciśnienie krwi do wzmocnienia odporności
Zespół skupił się na enzymie konwertującym angiotensynę (ACE), znanym głównie z roli w kontroli ciśnienia krwi i jako cel powszechnie stosowanych leków kardiologicznych. Wcześniejsze badania na myszach sugerowały, że wyższy poziom ACE w komórkach mieloidalnych, w tym w makrofagach, poprawia ich zdolność do zwalczania infekcji i guzów. W niniejszym badaniu autorzy przenieśli ten pomysł na system ludzki. Wykorzystali indukowane komórki pluripotentne (iPSC) — komórki dorosłe przereprogramowane do stanu podobnego do macierzystego — i wprowadzili genetyczny przełącznik pozwalający regulować poziomy ACE przy pomocy powszechnego antybiotyku doksycykliny. Z tych zmodyfikowanych komórek macierzystych wytwarzali na żądanie duże ilości makrofagów — skalowalną platformę nazwaną ACE-iMac.
Budowanie „przeładowanych” makrofagów w laboratorium
Po włączeniu przełącznika ACE komórki ACE-iMac wyglądały i zachowywały się zupełnie inaczej niż zwykłe hodowane w laboratorium makrofagi. Wydzielały znacznie większe ilości sygnałów prozapalnych, generowały duże wyrzuty reaktywnych form tlenu i tlenku azotu — chemicznych „broni” niszczących komórki nowotworowe — oraz wykazywały wzorce aktywności genów powiązane z silnie aktywowanym stanem podobnym do M1. Jednocześnie zmniejszyła się produkcja cząsteczek związanych z bardziej supresyjnym, sprzyjającym guzom trybem działania. W hodowlach ACE-iMac znacznie skuteczniej niż kontrolne makrofagi hamowały wzrost komórek czerniaka, potrójnie ujemnego raka piersi oraz opornych na leki nowotworów głowy i szyi.
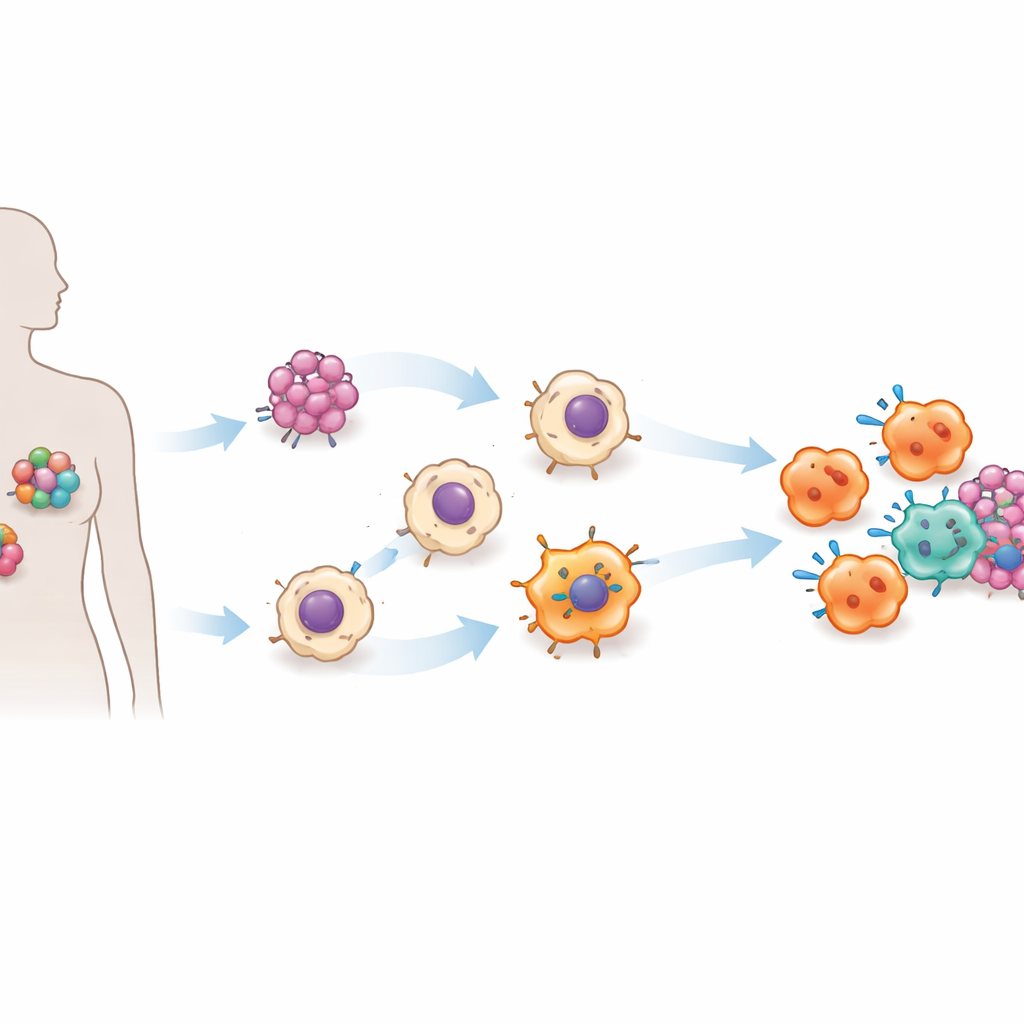
Powstrzymywanie guzów i pobudzanie innych komórek odpornościowych
Decydujący test przeprowadzono w modelach mysich z ludzkimi guzami. Gdy ACE-iMac wstrzyknięto bezpośrednio do guzów litych, guzy te skurczyły się dramatycznie — o około trzy czwarte lub więcej w porównaniu z guzami otrzymującymi zwykłe makrofagi. Efekt obserwowano w modelach czerniaka, raka piersi i raka głowy i szyi. W obrębie guzów ACE-iMac wykazywały silne sygnatury zapalne i towarzyszyły im bardziej aktywne komórki NK oraz, w specjalnie humanizowanych myszach z funkcjonalnym ludzkim układem odpornościowym, silniejsze ludzkie limfocyty zabójcze T. Co ciekawe, ogólna liczba tych innych komórek odpornościowych niewiele się zmieniała; zamiast tego stały się one bardziej aktywne, co sugeruje, że ACE-iMac działają jak trenerzy na miejscu, pobudzając szerszą odpowiedź immunologiczną, zamiast jedynie zwiększać liczebność bojowników.
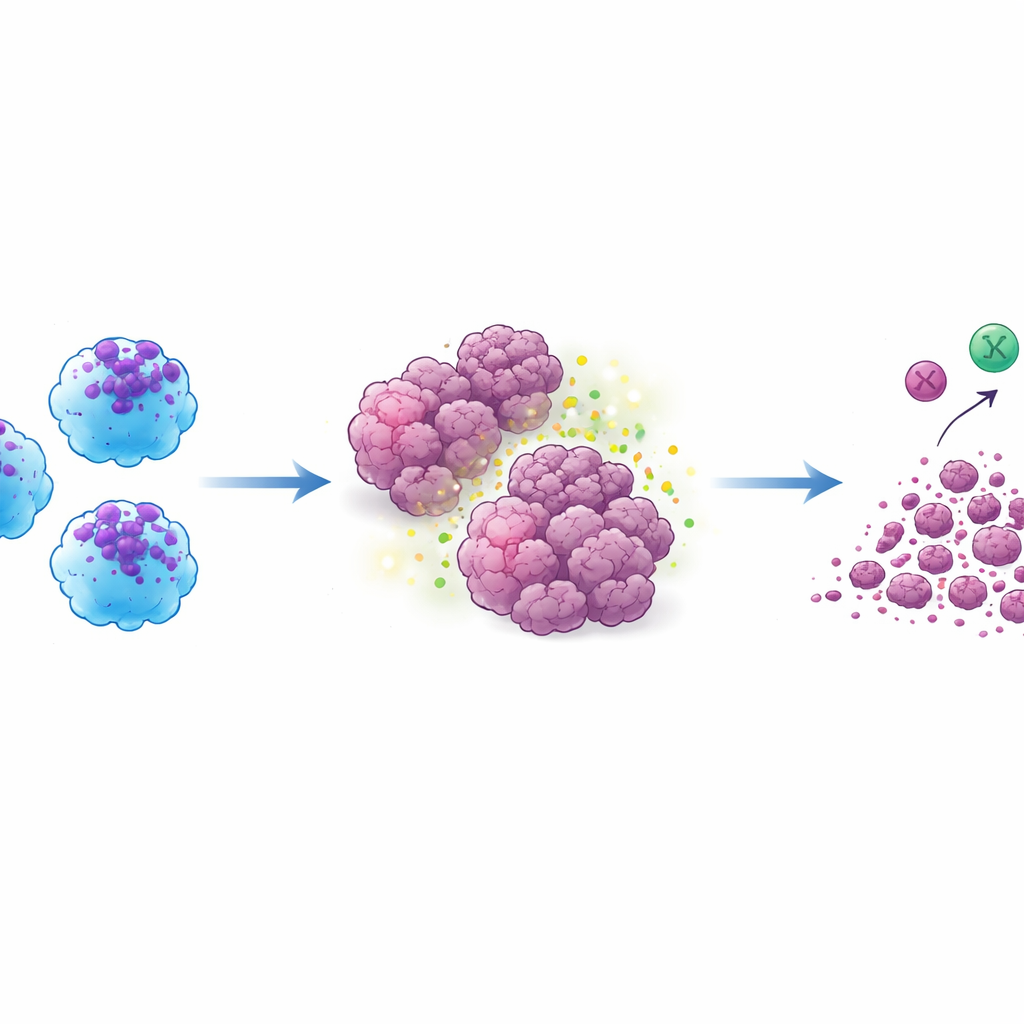
Odkodowanie mechanizmów wewnętrznych
Aby zrozumieć, co napędza takie zachowanie, badacze przeanalizowali globalną aktywność genów w komórkach ACE-iMac. Włączenie ACE wzmocniło sieci powiązane z klasyczną aktywacją makrofagów, produkcją cytokin, przetwarzaniem antygenów oraz skompletowaniem komórkowych „żołądków” zwanych fagosomami, które trawią cele. Dodatkowo nasiliło szlaki pomagające makrofagom prezentować fragmenty białek nowotworowych limfocytom T, co może wyjaśniać silniejszą odpowiedź T w humanizowanych myszach. Pod wpływem stymulacji przypominającej środowisko guza ACE-iMac wykazywały dalsze wzrosty ekspresji genów zaangażowanych w metabolizm i różnicowanie — zmiany, które prawdopodobnie pomagają im pozostać aktywnymi w surowych warunkach guza, zamiast ulegać wyczerpaniu lub zmieniać stronę.
Co to może znaczyć dla przyszłej opieki onkologicznej
Dla nietechnicznego czytelnika kluczowa konkluzja jest taka, że autorzy stworzyli kontrolowalne, odnawialne źródło ludzkich makrofagów, które zachowują się jak wysoko wyspecjalizowani łowcy guzów i wzmacniacze odporności. Podnosząc poziom ACE tylko wtedy, gdy jest to potrzebne, przy użyciu zewnętrznego leku, można w zasadzie regulować siłę i czas trwania tej odpowiedzi, co może poprawić bezpieczeństwo. Przed zastosowaniem u pacjentów stoi jeszcze wiele etapów — w tym testy podawania dożylnie, długoterminowe bezpieczeństwo oraz połączenia z istniejącymi terapiami — lecz praca ta wskazuje na nową klasę terapii komórkowej. Zamiast celować w pojedynczy marker guza, komórki ACE-iMac dążą do szerokiego przeprogramowania środowiska odpornościowego wewnątrz guzów litych, potencjalnie czyniąc nowotwory bardziej widocznymi i bardziej podatnymi na własne mechanizmy obronne organizmu.
Cytowanie: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Słowa kluczowe: immunoterapia nowotworów, makrofagi, komórki macierzyste pluripotentne indukowane, enzym konwertujący angiotensynę, nowotwory lite