Clear Sky Science · es
Macrófagos humanos derivados de iPSC bioingenierizados con mayor expresión de la enzima convertidora de angiotensina (ECA) suprimen el crecimiento de tumores sólidos
Volver nuestras propias defensas contra el cáncer
La inmunoterapia contra el cáncer ha cambiado el pronóstico de algunos pacientes, pero muchos tumores aún encuentran formas de ocultarse del sistema inmunitario o agotarlo. Este estudio explora una nueva manera de potenciar a uno de los defensores naturales del organismo —los macrófagos— reprogramándolos en el laboratorio para que se vuelvan mucho más agresivos frente a los tumores sólidos. El trabajo sugiere un futuro en el que los médicos podrían infundir a los pacientes células inmunitarias hechas a medida que ataquen una amplia gama de cánceres sin necesitar reconocer un único marcador tumoral específico.
Por qué importan los macrófagos en el cáncer
Los macrófagos son glóbulos blancos que actúan tanto como recolectores de desechos como soldados de primera línea. En muchos tumores sólidos son abundantes, pero a menudo en el modo equivocado. En lugar de atacar, derivan a un estado “sanador” que en realidad ayuda a los tumores a crecer, diseminarse y evadir a otras células inmunitarias. Los autores razonaron que si podían empujar de forma fiable a los macrófagos hacia un estado inflamatorio y contundente y mantenerlos así dentro del tumor, estas células podrían tanto matar directamente a las células cancerosas como movilizar a otros combatientes inmunitarios como los linfocitos T y las células NK (natural killer).
Tomando prestada una enzima de la presión arterial para potenciar la inmunidad
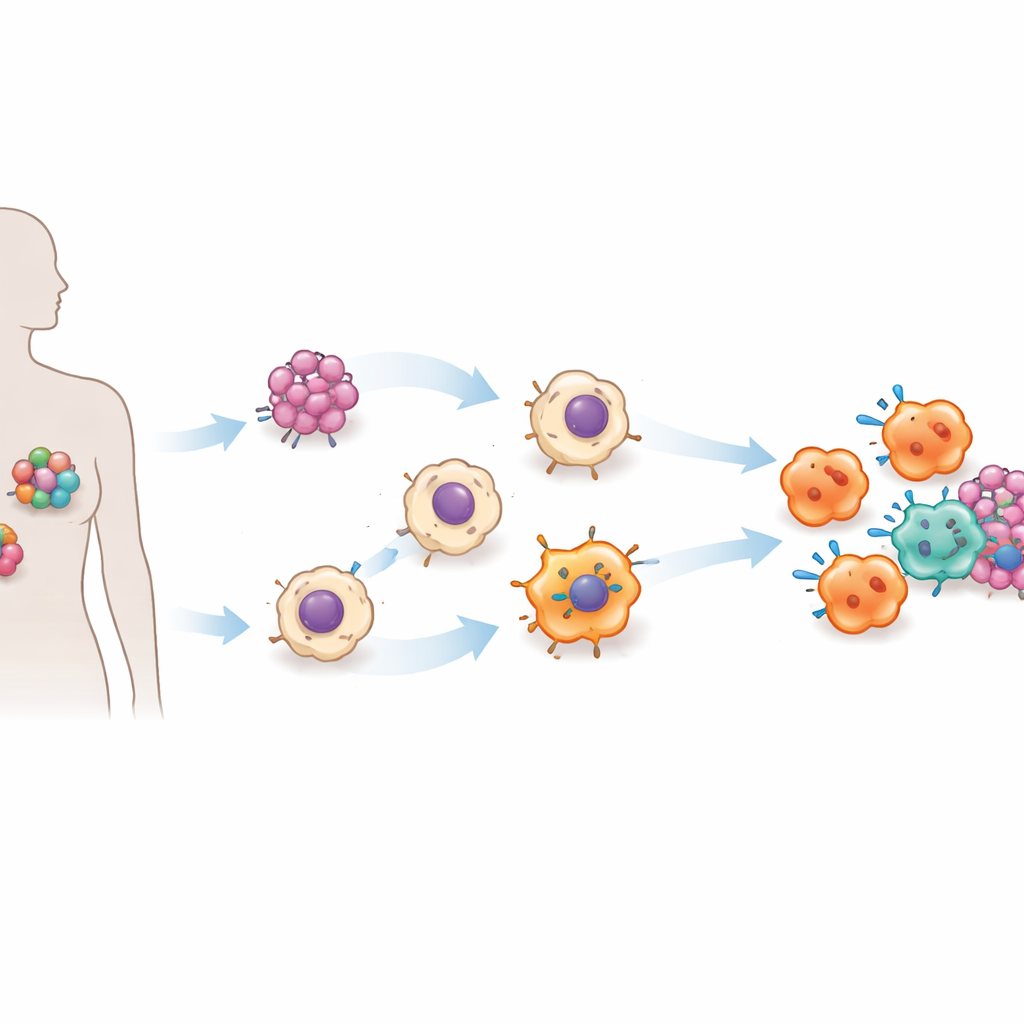
El equipo se centró en la enzima convertidora de angiotensina (ECA), conocida por su papel en el control de la presión arterial y como diana de fármacos cardiacos comunes. Trabajos previos en ratones insinuaron que niveles más altos de ECA en células mieloides, incluidos los macrófagos, mejoran la capacidad de estas células para combatir infecciones y tumores. En este estudio, los investigadores llevaron esa idea a un sistema humano. Usaron células pluripotentes inducidas —células adultas reprogramadas a un estado similar al de las células madre— e insertaron un interruptor genético que permite aumentar o disminuir los niveles de ECA con el antibiótico habitual doxiciclina. A partir de estas células madre modificadas, produjeron grandes cantidades de macrófagos a la demanda, una plataforma escalable que llaman ACE‑iMac.
Construyendo macrófagos supercargados en el laboratorio
Cuando se activó el interruptor de la ECA, las células ACE‑iMac resultantes se parecían y se comportaban de forma muy distinta a los macrófagos cultivados de forma habitual. Liberaron cantidades mucho mayores de señales inflamatorias, generaron grandes estallidos de especies reactivas de oxígeno y óxido nítrico —armas químicas que dañan células tumorales— y mostraron patrones de actividad génica asociados con un estado altamente activado, similar a M1. Al mismo tiempo, redujeron la producción de moléculas vinculadas a un modo más supresor que favorece al tumor. En placas de cultivo, las células ACE‑iMac ralentizaron el crecimiento de células de melanoma, cáncer de mama triple negativo y cáncer de cabeza y cuello resistente a fármacos con mucha más efectividad que macrófagos de control.
Detener tumores y activar a otras células inmunitarias
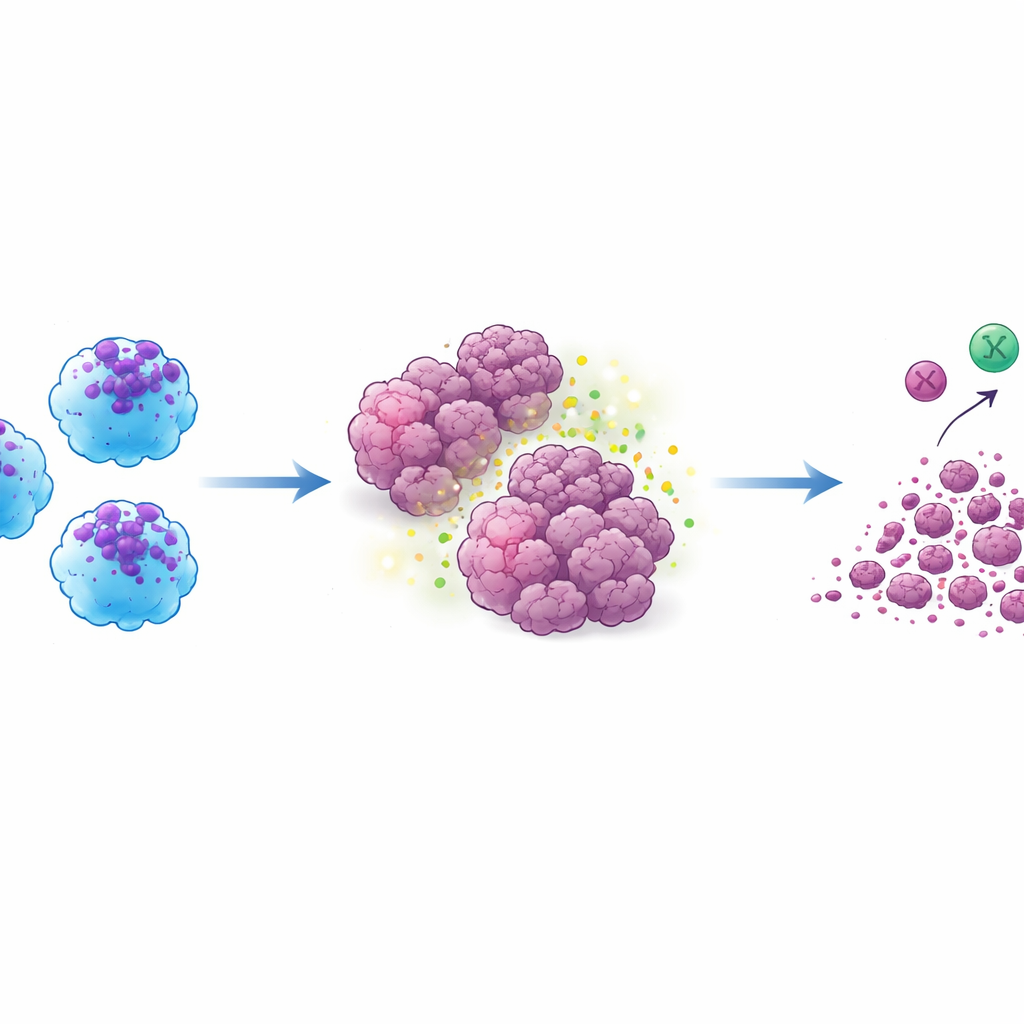
La prueba crucial se realizó en modelos murinos con tumores humanos. Cuando las células ACE‑iMac se inyectaron directamente en tumores sólidos, esos tumores se redujeron drásticamente —aproximadamente en tres cuartas partes o más en comparación con tumores que recibieron macrófagos ordinarios. Esto se mantuvo en modelos de melanoma, mama y cabeza y cuello. Dentro de los tumores, las ACE‑iMac mostraron fuertes firmas inflamatorias y estuvieron acompañadas por células NK más activas y, en ratones especialmente humanizados con un sistema inmunitario humano funcional, por linfocitos T citotóxicos humanos más potentes. Curiosamente, el número total de estas otras células inmunitarias no cambió mucho; en lugar de ello, se activaron más, lo que sugiere que las ACE‑iMac actúan como entrenadores in situ que energizan la respuesta inmune más amplia en lugar de simplemente aportar más combatientes.
Descifrando el funcionamiento interno
Para entender qué impulsa este comportamiento, los investigadores examinaron la actividad génica global en las células ACE‑iMac. Activar la ECA potenció redes vinculadas a la activación clásica de macrófagos, la producción de citocinas, el procesamiento de antígenos y el ensamblaje de “estómagos” celulares llamados fagosomas que digieren objetivos. También afinó rutas que ayudan a los macrófagos a presentar fragmentos de proteínas tumorales a los linfocitos T, lo que puede explicar la respuesta T más fuerte en los ratones humanizados. Bajo una estimulación similar a la tumoral, las ACE‑iMac mostraron ganancias adicionales en genes implicados en el metabolismo y la diferenciación, cambios que probablemente les ayudan a mantenerse activas en el ambiente hostil del tumor en lugar de agotarse o cambiar de bando.
Qué podría significar esto para la atención del cáncer en el futuro
Para un no especialista, la conclusión es que los autores han construido una fuente controlable y renovable de macrófagos humanos que se comportan como cazadores tumorales muy focalizados y potenciadores inmunitarios. Al elevar los niveles de ECA sólo cuando es necesario mediante un fármaco externo, pueden, en principio, ajustar la intensidad y el momento de esta respuesta, lo que puede mejorar la seguridad. Aunque quedan muchos pasos antes del uso en pacientes —incluidas pruebas de administración intravenosa, seguridad a largo plazo y combinaciones con terapias existentes—, este trabajo apunta a una nueva clase de terapia celular. En vez de dirigirse a un marcador tumoral a la vez, las células ACE‑iMac pretenden reconfigurar de forma amplia el paisaje inmunitario dentro de los tumores sólidos, haciendo potencialmente al cáncer más visible y más vulnerable a las propias defensas del organismo.
Cita: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Palabras clave: inmunoterapia contra el cáncer, macrófagos, células madre pluripotentes inducidas, enzima convertidora de angiotensina, tumores sólidos