Clear Sky Science · pt
Macrófagos humanos derivados de iPSC bioengenheirados com aumento da expressão da enzima conversora de angiotensina (ECA) suprimem o crescimento de tumores sólidos
Transformando Nossos Próprios Defensores Contra o Câncer
A imunoterapia contra o câncer mudou o prognóstico para alguns pacientes, mas muitos tumores ainda encontram maneiras de se esconder do sistema imunológico ou de desgastá‑lo. Este estudo explora uma nova forma de potencializar um dos defensores naturais do corpo — os macrófagos — reprogramando‑os em laboratório para que se tornem muito mais agressivos contra tumores sólidos. O trabalho sugere um futuro em que médicos possam infundir pacientes com células imunes sob medida que ataquem uma ampla gama de cânceres sem precisar reconhecer um único marcador tumoral específico.
Por Que os Macrófagos Importam no Câncer
Macrófagos são células brancas do sangue que atuam tanto como coletores de lixo quanto como soldados de linha de frente. Em muitos tumores sólidos, eles são abundantes — mas frequentemente em um modo inadequado. Em vez de atacar, assumem um estado “curador” que, na verdade, ajuda o tumor a crescer, disseminar‑se e escapar de outras células imunes. Os autores raciocinaram que, se pudessem de forma confiável empurrar os macrófagos para um estado inflamatório e fortemente agressivo e mantê‑los assim dentro do tumor, essas células poderiam tanto matar células cancerosas diretamente quanto mobilizar outros combatentes imunes, como células T e células natural killer (NK).
Tomando emprestada uma enzima da pressão arterial para dar poder ao sistema imune
A equipe concentrou‑se na enzima conversora de angiotensina (ECA), mais conhecida por seu papel no controle da pressão arterial e como alvo de medicamentos cardíacos comuns. Trabalhos anteriores em camundongos sugeriram que níveis mais altos de ECA em células mieloides, incluindo macrófagos, tornam essas células melhores no combate a infecções e tumores. Neste estudo, os pesquisadores trouxeram essa ideia para um sistema humano. Eles usaram células-tronco pluripotentes induzidas — células adultas reprogramadas de volta a um estado semelhante a tronco — e inseriram um interruptor genético que permite ajustar os níveis de ECA para cima ou para baixo com o antibiótico comum doxiciclina. A partir dessas células-tronco engenheiradas, produziram grandes quantidades de macrófagos sob demanda, uma plataforma escalável que chamam de ACE‑iMac.
Construindo macrófagos turbinados no laboratório
Quando o interruptor da ECA foi ativado, as células ACE‑iMac resultantes pareceram e se comportaram de maneira muito diferente dos macrófagos cultivados em laboratório comuns. Liberaram quantidades muito maiores de sinais inflamatórios, geraram grandes rajadas de espécies reativas de oxigênio e óxido nítrico — armas químicas que danificam células tumorais — e exibiram padrões de atividade gênica associados a um estado altamente ativado, “semelhante a M1”. Ao mesmo tempo, reduziram a produção de moléculas vinculadas a um modo mais supressivo que favorece o tumor. Em placas de cultura, as células ACE‑iMac retardaram o crescimento de melanoma, câncer de mama triple‑negative e câncer de cabeça e pescoço resistente a drogas muito mais eficazmente do que macrófagos controle.
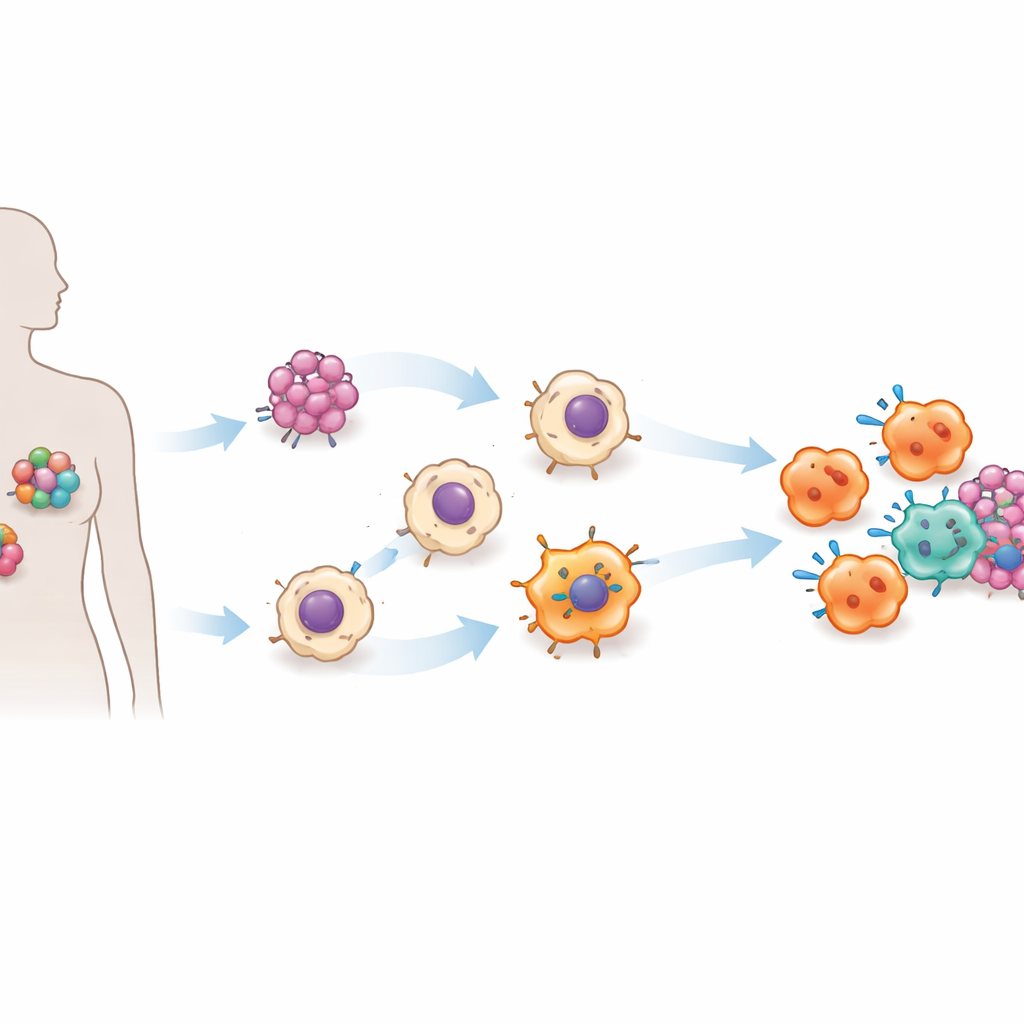
Parando tumores e despertando outras células imunes
O teste crucial veio em modelos de camundongo portadores de tumores humanos. Quando células ACE‑iMac foram injetadas diretamente em tumores sólidos, esses tumores encolheram dramaticamente — cerca de três quartos ou mais em comparação com tumores que receberam macrófagos comuns. Isso foi observado em modelos de melanoma, câncer de mama e câncer de cabeça e pescoço. Dentro dos tumores, as células ACE‑iMac mostraram fortes assinaturas inflamatórias e foram acompanhadas por células NK mais ativas e, em camundongos humanizados com um sistema imunológico humano funcional, por células T citotóxicas humanas mais potentes. Interessantemente, o número total dessas outras células imunes não mudou muito; em vez disso, elas tornaram‑se mais ativadas, o que sugere que as células ACE‑iMac atuam como treinadoras no local que energizam a resposta imune mais ampla em vez de simplesmente adicionar mais combatentes.
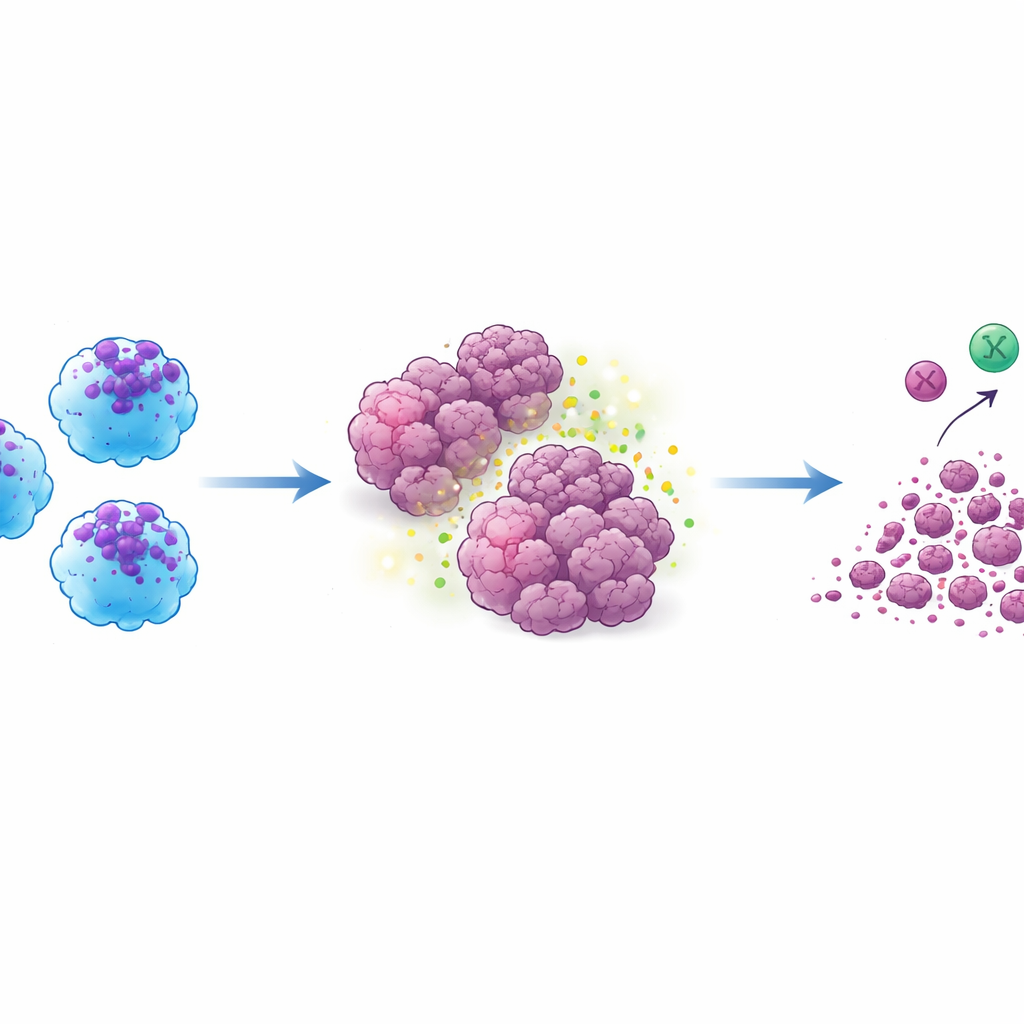
Decodificando os mecanismos internos
Para entender o que impulsiona esse comportamento, os pesquisadores examinaram a atividade gênica global nas células ACE‑iMac. Ativar a ECA potencializou redes ligadas à ativação clássica de macrófagos, produção de citocinas, processamento de antígenos e montagem de “estômagos” celulares chamados fagossomos que digerem alvos. Também ajustou vias que ajudam macrófagos a apresentar fragmentos de proteínas tumorais às células T, o que pode explicar a resposta mais forte de células T em camundongos humanizados. Sob estimulação semelhante à encontrada em tumores, as células ACE‑iMac apresentaram ganhos adicionais em genes envolvidos em metabolismo e diferenciação, mudanças que provavelmente as ajudam a permanecer ativas no ambiente hostil do tumor em vez de se exaurirem ou mudarem de lado.
O que isso pode significar para o futuro do tratamento do câncer
Para um não especialista, a conclusão é que os autores criaram uma fonte controlável e renovável de macrófagos humanos que se comportam como caçadores de tumor altamente focados e impulsionadores do sistema imune. Ao aumentar os níveis de ECA apenas quando necessário usando um fármaco externo, eles podem, em princípio, ajustar a intensidade e o tempo dessa resposta, o que pode melhorar a segurança. Embora muitos passos permaneçam antes do uso em pacientes — incluindo testar a administração via intravenosa, segurança a longo prazo e combinações com terapias existentes — este trabalho aponta para uma nova classe de terapia celular. Em vez de segmentar um marcador tumoral por vez, as células ACE‑iMac visam redefinir amplamente o panorama imune dentro de tumores sólidos, potencialmente tornando o câncer mais visível e mais vulnerável às defesas do próprio corpo.
Citação: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Palavras-chave: imunoterapia contra o câncer, macrófagos, células-tronco pluripotentes induzidas, enzima conversora de angiotensina, tumores sólidos