Clear Sky Science · it
Macrofagi umani derivati da iPSC bioingegnerizzati con aumentata espressione dell'enzima di conversione dell'angiotensina (ACE) sopprimono la crescita dei tumori solidi
Rivoltare i nostri difensori contro il cancro
L’immunoterapia oncologica ha cambiato le prospettive per alcuni pazienti, ma molti tumori continuano a trovare modi per nascondersi o logorare il sistema immunitario. Questo studio esplora un nuovo modo per potenziare uno dei difensori naturali del corpo — i macrofagi — riprogrammandoli in laboratorio affinché diventino molto più aggressivi contro i tumori solidi. Il lavoro suggerisce un futuro in cui i medici potrebbero infondere nei pazienti cellule immunitarie su misura che attaccano un’ampia gamma di tumori senza dover riconoscere un singolo marcatore tumorale specifico.
Perché i macrofagi sono importanti nel cancro
I macrofagi sono globuli bianchi che fungono sia da netturbini sia da soldati in prima linea. All’interno di molti tumori solidi sono abbondanti — ma spesso in modalità sbagliata. Invece di attaccare, assumono uno stato “riparatore” che in realtà favorisce la crescita, la diffusione e l’evasione del tumore rispetto ad altre cellule immunitarie. Gli autori hanno ipotizzato che se fosse possibile spingere i macrofagi in modo affidabile verso uno stato infiammatorio e fortemente aggressivo, e mantenerli tali all’interno del tumore, queste cellule potrebbero sia uccidere direttamente le cellule tumorali sia richiamare altri combattenti immunitari come le cellule T e le cellule natural killer (NK).
Prendere in prestito un enzima della pressione sanguigna per potenza immunitaria
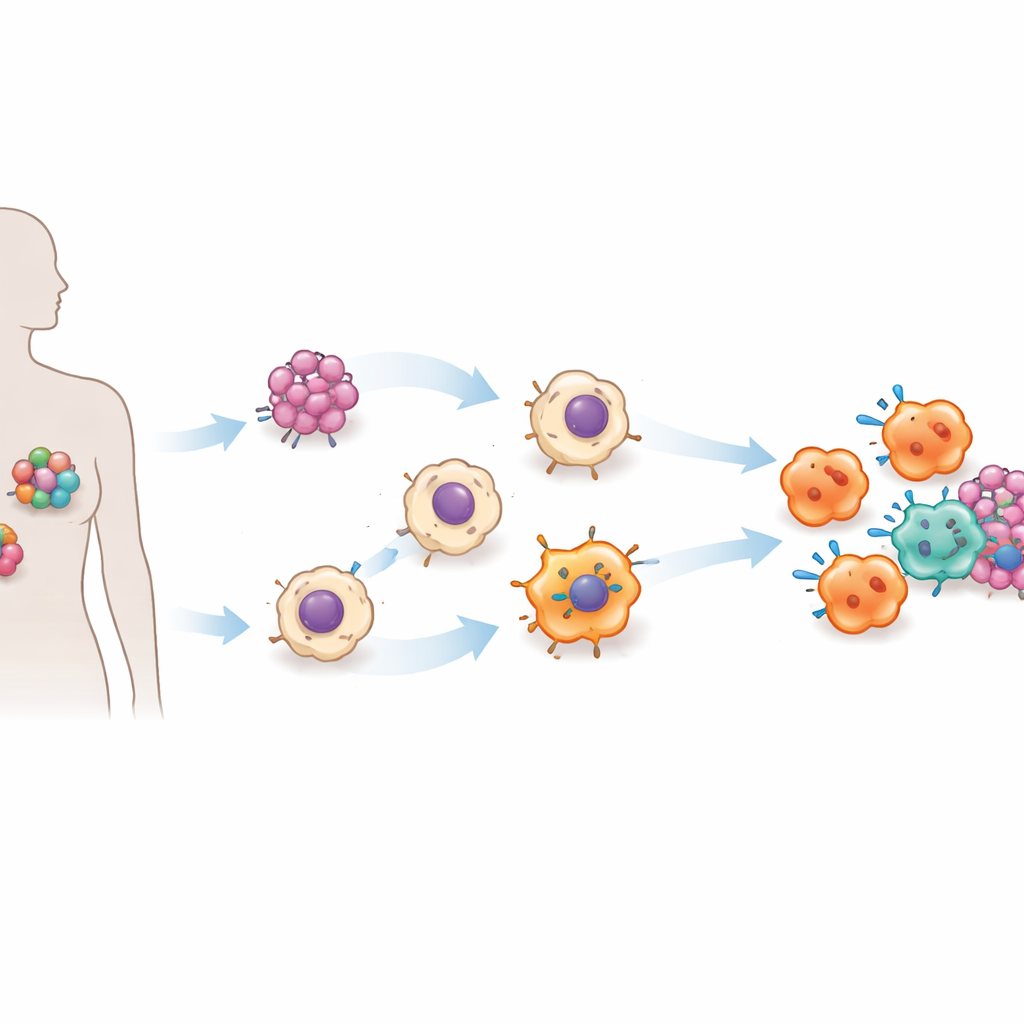
Il team si è concentrato sull’enzima di conversione dell’angiotensina (ACE), noto soprattutto per il suo ruolo nel controllo della pressione arteriosa e come bersaglio di comuni farmaci cardiaci. Lavori precedenti sui topi suggerivano che livelli più alti di ACE nelle cellule mieloidi, inclusi i macrofagi, rendono queste cellule migliori nel combattere infezioni e tumori. In questo studio i ricercatori hanno portato l’idea a un sistema umano. Hanno usato cellule staminali pluripotenti indotte — cellule adulte riprogrammate in uno stato simile a quello staminale — e hanno inserito un interruttore genetico che consente di regolare i livelli di ACE su o giù tramite il comune antibiotico doxiciclina. Da queste cellule staminali ingegnerizzate hanno prodotto grandi quantità di macrofagi su richiesta, una piattaforma scalabile che chiamano ACE-iMac.
Costruire macrofagi sovralimentati in laboratorio
Quando l’interruttore ACE è stato attivato, le cellule ACE-iMac risultanti apparivano e si comportavano in modo molto diverso rispetto ai macrofagi coltivati in laboratorio convenzionali. Rilasciavano quantità molto maggiori di segnali infiammatori, generavano grandi esplosioni di specie reattive dell’ossigeno e ossido nitrico — armi chimiche che danneggiano le cellule tumorali — e mostravano profili di attività genica associati a uno stato altamente attivato, di tipo “M1‑like”. Allo stesso tempo riducevano la produzione di molecole legate a una modalità più soppressiva che favorisce il tumore. In piastre di coltura, le cellule ACE-iMac rallentavano la crescita di melanoma, carcinoma mammario triplo negativo e cellule di cancro testa‑collo resistenti ai farmaci molto più efficacemente rispetto ai macrofagi di controllo.
Fermare i tumori e risvegliare altre cellule immunitarie
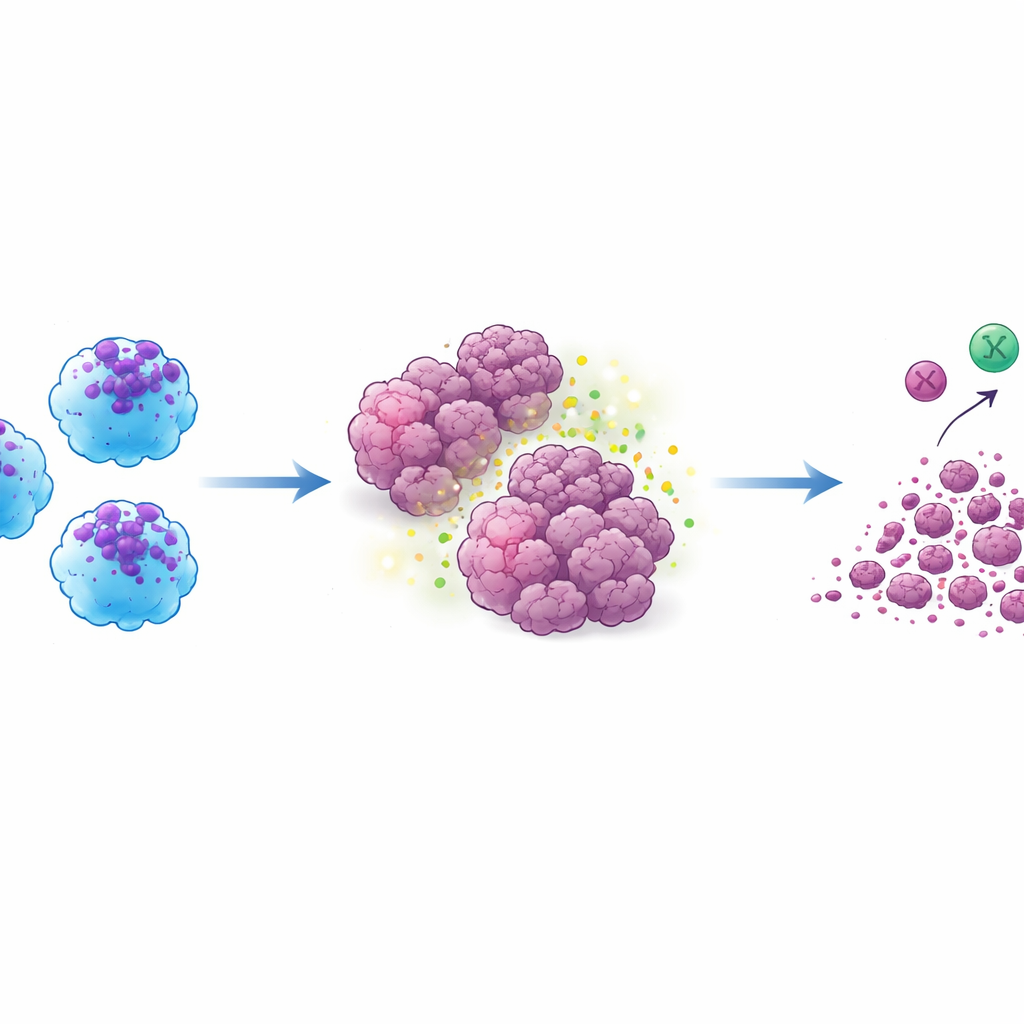
La prova cruciale è arrivata nei modelli murini portatori di tumori umani. Quando le cellule ACE-iMac sono state iniettate direttamente nei tumori solidi, quei tumori si sono ridotti in modo drammatico — di circa tre quarti o più rispetto ai tumori che ricevevano macrofagi ordinari. Questo risultato è stato valido nei modelli di melanoma, tumore al seno e testa e collo. All’interno dei tumori, le cellule ACE-iMac mostravano forti firme infiammatorie e erano accompagnate da cellule NK più attive e, in topi umanizzati con un sistema immunitario umano funzionale, da cellule T citotossiche umane più potenti. È interessante che il numero complessivo di queste altre cellule immunitarie non cambiasse molto; invece, esse risultavano più attivate, suggerendo che le cellule ACE-iMac agiscono come allenatori in loco che energizzano la risposta immunitaria più ampia anziché limitarsi ad aggiungere più combattenti.
Decifrare i meccanismi interni
Per capire cosa guida questo comportamento, i ricercatori hanno esaminato l’attività genica globale nelle cellule ACE-iMac. L’attivazione di ACE potenziava reti collegate all’attivazione classica dei macrofagi, alla produzione di citochine, all’elaborazione degli antigeni e all’assemblaggio dei “tomacelli” cellulari chiamati fagosomi che digeriscono i bersagli. Ha inoltre modulato percorsi che aiutano i macrofagi a presentare frammenti di proteine tumorali alle cellule T, il che può spiegare la più forte risposta delle cellule T nei topi umanizzati. Sotto stimoli simili a quelli tumorali, le cellule ACE-iMac mostravano ulteriori aumenti nei geni coinvolti nel metabolismo e nella differenziazione, cambiamenti che probabilmente le aiutano a rimanere attive nell’ambiente ostile del tumore invece di esaurirsi o cambiare schieramento.
Cosa potrebbe significare per la cura del cancro futura
Per un non specialista, il punto chiave è che gli autori hanno creato una fonte controllabile e rinnovabile di macrofagi umani che si comportano come cacciatori di tumori altamente focalizzati e potenziatori immunitari. Aumentando i livelli di ACE solo quando necessario mediante un farmaco esterno, è possibile, in linea di principio, modulare l’intensità e il timing di questa risposta, il che potrebbe migliorare la sicurezza. Pur restando molti passi prima dell’uso clinico — compresi test sulla somministrazione endovenosa, la sicurezza a lungo termine e le combinazioni con terapie esistenti — questo lavoro indica una nuova classe di terapia cellulare. Piuttosto che mirare a un marcatore tumorale alla volta, le cellule ACE-iMac mirano a ripristinare in modo ampio il paesaggio immunitario all’interno dei tumori solidi, rendendo potenzialmente il cancro sia più visibile sia più vulnerabile alle difese proprie dell’organismo.
Citazione: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Parole chiave: immunoterapia del cancro, macrofagi, cellule staminali pluripotenti indotte, enzima di conversione dell'angiotensina, tumori solidi