Clear Sky Science · he
מאקרופאגים אנושיים מופקים מ‑iPSC בהנדסה ביולוגית עם ביטוי מוגבר של אנזים הממיר אנגיוטנסין (ACE) מעכבים גדילת גידולים סולידיים
לכוון את המגינים שלנו נגד הסרטן
אימונותרפיה לסרטן שינתה את התחזית עבור חלק מהחולים, אך גידולים רבים עדיין מוצאים דרכים להסתתר מהמערכת החיסונית או לשחוק אותה. המחקר בוחן שיטה חדשה להעצמת אחד ממגיני הגוף—המאקרופאגים—על ידי תכנות מחודש במעבדה כך שיהיו תוקפניים יותר כלפי גידולים סולידיים. הממצאים מרמזים על עתיד שבו רופאים עשויים להזרים למטופלים תאי חיסון מותאמים אישית התוקפים מגוון רחב של סרטן בלי הצורך לזהות סימן יחיד ספציפי של הגידול.
מדוע מאקרופאגים חשובים בסרטן
מאקרופאגים הם תאי דם לבנים המשמשים גם כיוצאי חפצים וגם כחיילים בחזית. בתוך גידולים סולידיים רבים הם שפעיים—אך לעתים קרובות במצב הלא נכון. במקום לתקוף, הם עוברים למצב של "מרפא" שמסייע למעשה לגידולים לגדול, להתפשט ולהתחמק מתאים חיסוניים אחרים. המחברים הגיעו למסקנה שאם יוכלו לדחוף באופן אמין את המאקרופאגים למצב דלקתי תקיף ולשמרם כך בתוך הגידול, תאים אלה עשויים גם להרוג תאי סרטן ישירות וגם לגייס לוחמים חיסוניים נוספים כמו תאי T ותאי הרג טבעיים (NK).
לשאול אנזים של ויסות לחץ־דם לטובת כוח חיסוני
הצוות התמקד באנזים הממיר אנגיוטנסין (ACE), הידוע בעיקר בשל תפקידו בוויסות לחץ הדם וכמטרה לתרופות לב נפוצות. עבודות קודמות בעכברים רמזו שרמות ACE גבוהות בתאים מיויידיים, כולל מאקרופאגים, משפרות את היכולת של תאים אלה להילחם בזיהומים ובגידולים. במחקר זה הביאו החוקרים רעיון זה למערכת אנושית. הם השתמשו בתאי גזע פלוריפוטנטים מושרים—תאים בוגרים שתוכנתו חזרה למצב דמוי גזע—והכניסו מתג גנטי שמאפשר לכוונן את רמות ה‑ACE מעלה או מטה בעזרת האנטיביוטיקה הנפוצה דוקסיציקלין. מתוך תאי הגזע המהונדסים הללו הפיקו כמויות גדולות של מאקרופאגים לפי דרישה, פלטפורמה מדרגית שהן קוראים לה ACE‑iMac.
בנייה של מאקרופאגים מואצים במעבדה
כשמנוע ה‑ACE הופעל, תאי ה‑ACE‑iMac שנוצרו נראו והתנהגו שונה מאוד ממאקרופאגים תרביית מעבדה רגילים. הם שחררו כמויות גבוהות בהרבה של איתותים דלקתיים, ייצרו פרצים גדולים של מולקולות חמצון ותחמוצת חנקן—נשקים כימיים שפוגעים בתאי גידול—והציגו דפוסי ביטוי גנים המקושרים למצב מופעל מאוד, בדומה ל"M1". במקביל הם הפחיתו ייצור מולקולות המשוייכות למצב מדכא שמסייע לגידול. במיתקני תרבית, תאי ACE‑iMac האטו את הגדילה של מלנומה, סרטן שד טריפל־נגטיבי וסרטן ראש וצוואר עמיד לתרופות בצורה משמעותית יותר מאשר מאקרופאגים בקרתיים.
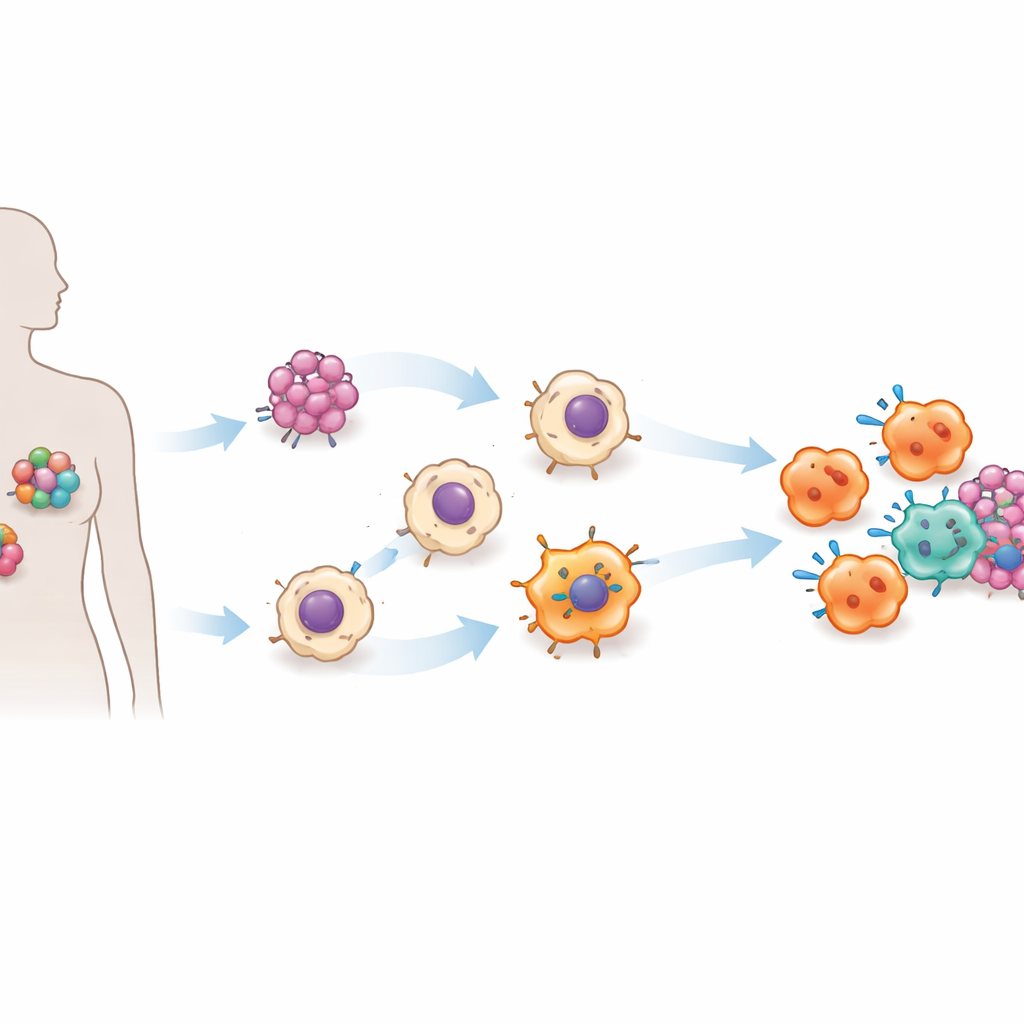
עיכוב גידולים והפעלת תאים חיסוניים נוספים
המבחן הקריטי הגיע במודלים עכבריים הנושאים גידולים אנושיים. כאשר הוחדרו תאי ACE‑iMac ישירות לתוך גידולים סולידיים, הגידולים הצטמצמו באופן דרמטי—בערך בשלושה רבעים או יותר בהשוואה לגידולים שקיבלו מאקרופאגים רגילים. ההשפעה נצפתה במודלים של מלנומה, סרטן שד וראש־צוואר. בתוך הגידולים, תאי ACE‑iMac הראו חתימות דלקתיות חזקות והיו מלוּות בתאי NK פעילים יותר, ובעכברים מיוחדים עם מערכת חיסון אנושית פונקציונלית הובילו גם לתאי T אנושיים קוטלי־חזק יותר. מעניין כי המספר הכולל של התאים החיסוניים האחרים לא השתנה משמעותית; במקום זאת הם הפכו לפעילים יותר, מה שמרמז שתאי ACE‑iMac פועלים כמאמנים בשטח שמאנרגטיים את התגובה החיסונית הרחבה במקום פשוט להוסיף לוחמים נוספים.
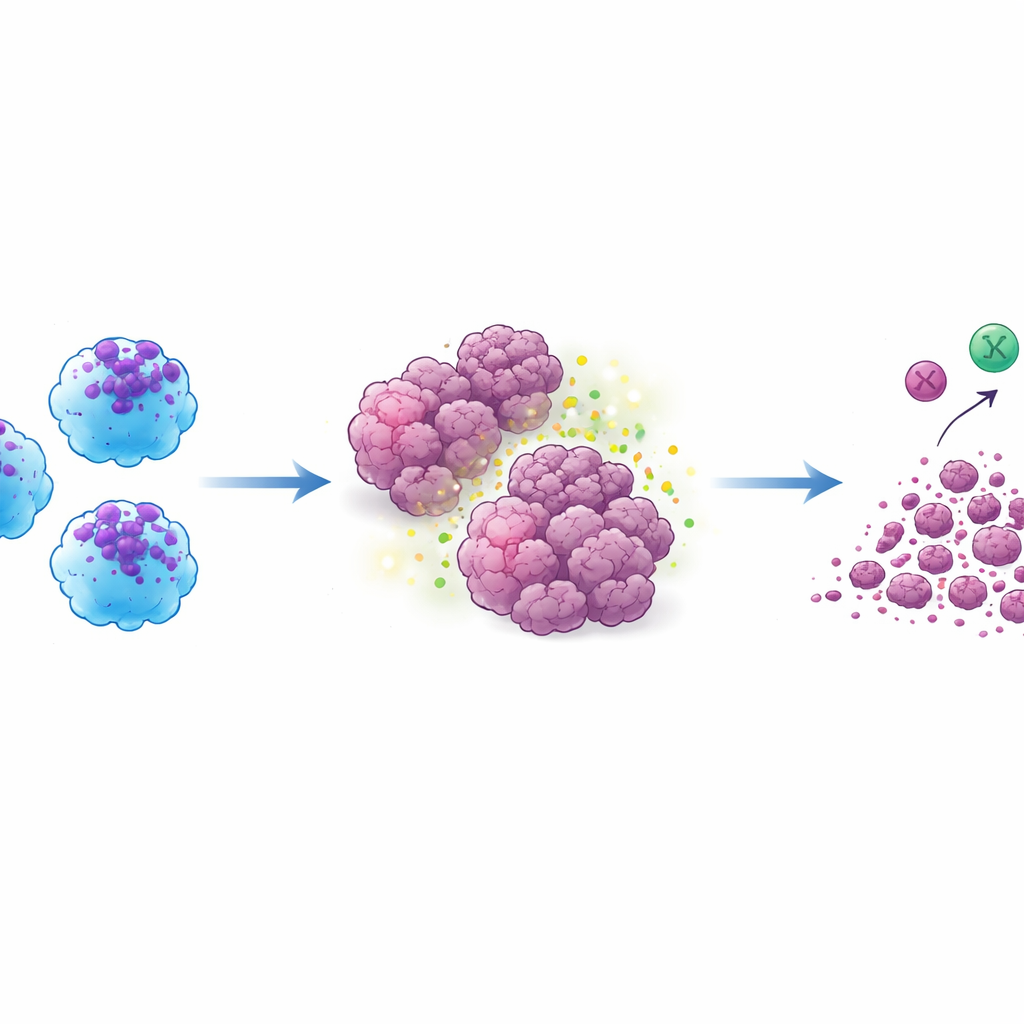
פיענוח המנגנונים הפנימיים
כדי להבין מה מניע התנהגות זו בחנו החוקרים את פעילות הגנים העולמית בתאי ACE‑iMac. הדלקת ה‑ACE הגביר עיצובים הקשורים להפעלה הקלאסית של מאקרופאגים, ייצור ציטוקינים, עיבוד אנטיגן והרכבת "קיבות" תאיות שנקראות פגוזומים שמעכלות מטרות. הוא גם כיוון מסלולים שעוזרים למאקרופאגים להציג קטעי חלבון גידול לתאי T, מה שעשוי להסביר את תגובת תאי ה‑T החזקה בעכברים האנושיים. תחת גירוי בדומה לסביבת גידול, תאי ACE‑iMac הראו עוד עליות בגנים המעורבים במטבוליזם ובהבחנה תאית—שינויים הסבירים שעוזרים להם להישאר פעילים בסביבה הקשה של הגידול במקום להישחק או לעבור לצד השני.
מה זה עשוי משמעותית לטיפול בסרטן בעתיד
ללא מומחיות מיוחדת, המסקנה היא שהמחברים בנו מקור נשלט וניתן לחדש של מאקרופאגים אנושיים שמתנהגים כמו ציידי גידולים ממוקדים ומגבירי חיסון. על ידי העלאת רמות ACE רק כשהנדרש בעזרת תרופה חיצונית, ניתן בעקרון לכוונן את עוצמת וזמן התגובה, מה שעשוי לשפר את הבטיחות. בעוד שנדרשים עוד שלבים רבים לפני שימוש בחולים—כולל בדיקות מסירה תוך ורידית, בטיחות לטווח ארוך ושילובים עם טיפולים קיימים—העבודה מצביעה על כיתה חדשה של טיפול תאי. במקום לכוון לסמן גידול אחד בכל פעם, תאי ACE‑iMac שואפים לאפס באופן רחב את הנוף החיסוני בתוך גידולים סולידיים, מה שעשוי להפוך את הסרטן לנראה ופגיע יותר בפני מגיני הגוף עצמם.
ציטוט: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
מילות מפתח: אימונותרפיה של סרטן, מאקרופאגים, תאי גזע פלוריפוטנטים מושרים, אנזים הממיר אנגיוטנסין, גידולים סולידיים