Clear Sky Science · sv
Bioengineenarerade makrofager härledda från iPSC med ökad uttryck av angiotensin‑konverterande enzym (ACE) hämmar tillväxten av solida tumörer
Vända våra egna försvarare mot cancer
Cancerimmunterapi har förändrat prognosen för vissa patienter, men många tumörer hittar fortfarande sätt att gömma sig för eller uttrötta immunsystemet. Denna studie utforskar ett nytt sätt att överladda en av kroppens naturliga försvarare — makrofager — genom att omprogrammera dem i laboratoriet så att de blir mycket mer aggressiva mot solida tumörer. Arbetet antyder en framtid där läkare kan tillföra patienterna skräddarsydda immunceller som angriper en bred uppsättning cancerformer utan att behöva känna igen en enskild specifik tumörmarkör.
Varför makrofager är viktiga vid cancer
Makrofager är vita blodkroppar som fungerar både som sopuppsamlare och frontsoldater. Inuti många solida tumörer finns de i riklig mängd — men ofta i fel läge. Istället för att attackera glider de in i ett "läknings"‑tillstånd som faktiskt hjälper tumörer att växa, sprida sig och undvika andra immunceller. Forskarna resonerade att om de på ett pålitligt sätt kunde få makrofager att anta ett hårt slående, inflammatoriskt tillstånd och hålla dem där inne i tumören, skulle dessa celler både kunna döda cancerceller direkt och mobilisera andra immunkämpar såsom T‑celler och naturliga mördarceller (NK‑celler).
Låna ett blodtrycksenzym för immunstyrka
Teamet fokuserade på angiotensin‑konverterande enzym (ACE), mest känt för sin roll i blodtryckskontroll och som mål för vanliga hjärtmediciner. Tidigare arbete i möss antydde att högre ACE‑nivåer i myeloida celler, inklusive makrofager, gör dessa celler bättre på att bekämpa infektioner och tumörer. I denna studie förde forskarna in den idén i ett mänskligt system. De använde inducerade pluripotenta stamceller — adulta celler omprogrammerade tillbaka till ett stamliknande tillstånd — och infogade en genetisk strömbrytare som låter dem justera ACE‑nivåerna upp eller ner med den vanliga antibiotikan doxycyklin. Från dessa ingenjörsframställda stamceller producerade de stora mängder makrofager på begäran, en skalbar plattform de kallar ACE‑iMac.
Bygga superladdade makrofager i laboratoriet
När ACE‑strömbrytaren sattes på såg de resulterande ACE‑iMac‑cellerna mycket annorlunda ut och uppträdde olikt vanliga laboratorieodlade makrofager. De frisatte mycket större mängder inflammatoriska signaler, genererade stora utbrott av reaktiva syreradikaler och kväveoxid — kemiska vapen som skadar tumörceller — och visade genaktivitetsmönster som förknippas med ett starkt aktiverat, "M1‑liknande" tillstånd. Samtidigt minskade de produktionen av molekyler kopplade till ett mer undertryckande, tumörhjälpande läge. I odlingsplattor bromsade ACE‑iMac‑celler tillväxten av melanom, trippelnegativ bröstcancer och läkemedelsresistenta huvud‑ och halscancerceller mycket effektivare än kontrollmakrofager.
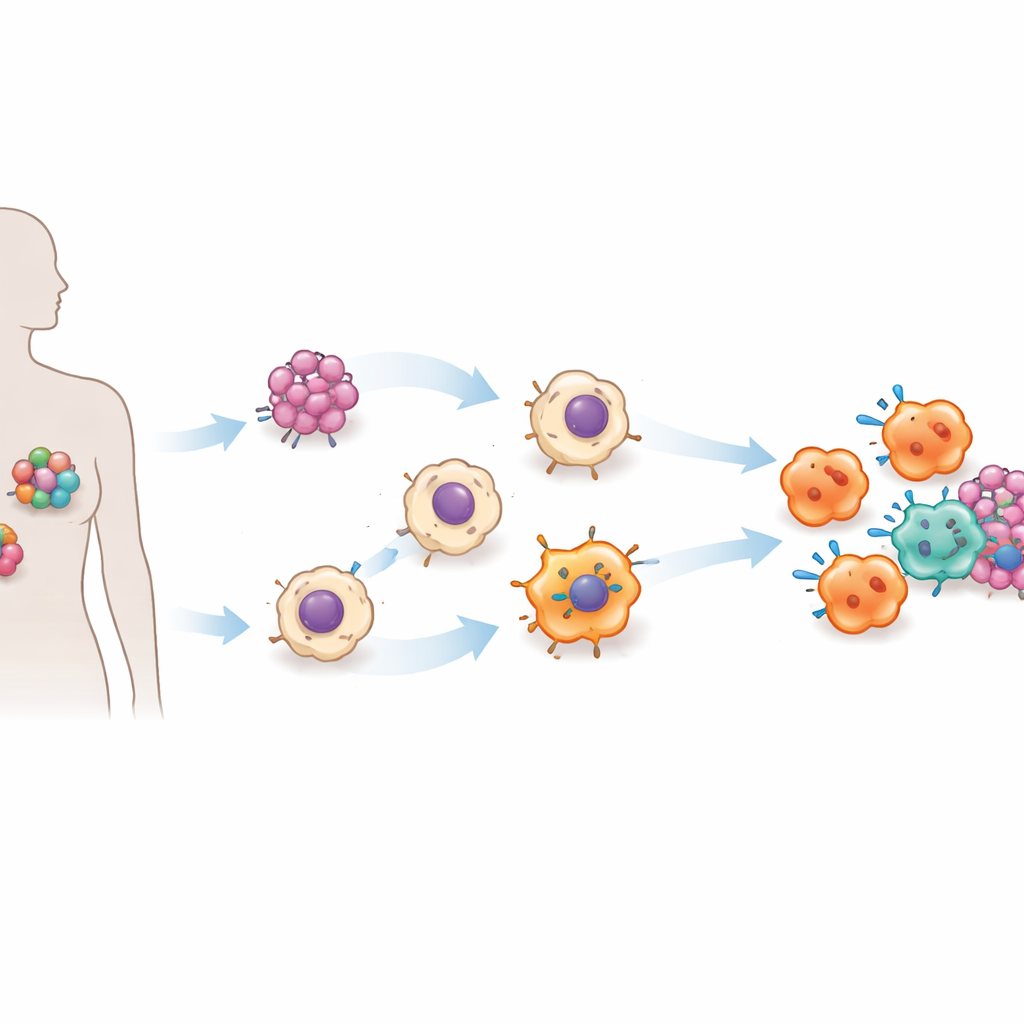
Stoppa tumörer och väcka andra immunceller
Det avgörande testet gjordes i musmodeller med mänskliga tumörer. När ACE‑iMac‑celler injicerades direkt i solida tumörer krympte dessa tumörer dramatiskt — med ungefär tre fjärdedelar eller mer jämfört med tumörer som fick vanliga makrofager. Detta gällde över modeller för melanom, bröstcancer och huvud‑ och halscancer. Inne i tumörerna uppvisade ACE‑iMac‑celler starka inflammatoriska signaturer och ackompanjerades av mer aktiva NK‑celler och, i särskilt humaniserade möss med ett funktionellt mänskligt immunsystem, mer potenta mänskliga cytotoxiska T‑celler. Intressant nog ändrades inte det totala antalet av dessa andra immunceller mycket; istället blev de mer aktiverade, vilket tyder på att ACE‑iMac‑celler fungerar som platsbundna coacher som energiserar den bredare immunsvaret snarare än att bara tillföra fler kämpar.
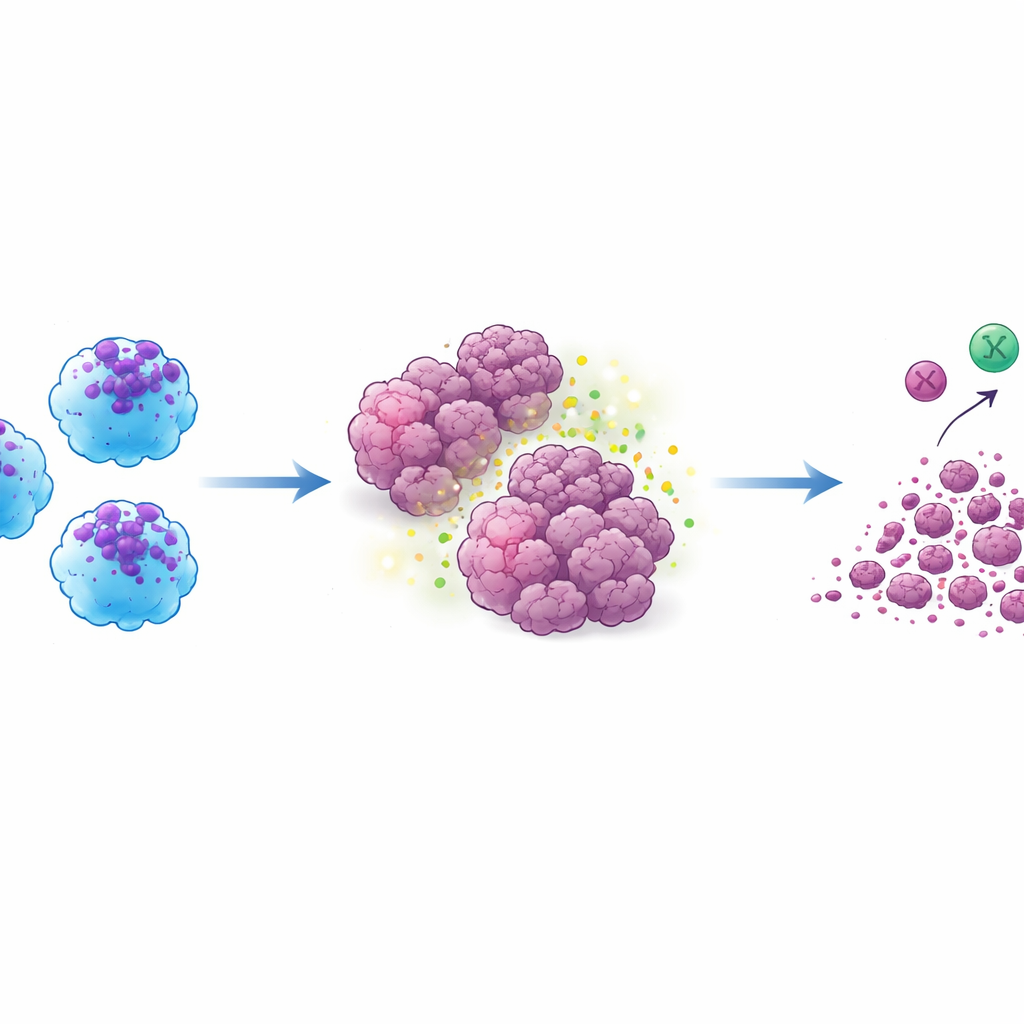
Avkoda de inre mekanismerna
För att förstå vad som driver detta beteende undersökte forskarna global genaktivitet i ACE‑iMac‑celler. Att slå på ACE ökade nätverk kopplade till klassisk makrofagaktivering, cytokinproduktion, antigenbearbetning och bildandet av cellulära "magar" kallade fagosomer som smälter ner måltavlor. Det ställde också in signalvägar som hjälper makrofager att presentera fragment av tumörproteiner för T‑celler, vilket kan förklara det starkare T‑cellsansvaret i de humaniserade mössen. Under tumörliknande stimulans visade ACE‑iMac‑celler ytterligare ökningar i gener involverade i metabolism och differentiering, förändringar som sannolikt hjälper dem att förbli aktiva i den hårda tumörmiljön istället för att bli utmattade eller byta sida.
Vad detta kan innebära för framtidens cancerbehandling
För en icke‑specialist är slutsatsen att författarna har byggt en kontrollerbar, förnybar källa av mänskliga makrofager som beter sig som högt fokuserade tumörjägare och immunstärkare. Genom att höja ACE‑nivåerna endast när det behövs med ett externt läkemedel kan de i princip finjustera styrkan och tidpunkten för detta svar, vilket kan förbättra säkerheten. Många steg återstår innan användning hos patienter — inklusive tester av intravenös leverans, långtidsäkerhet och kombinationer med befintliga terapier — men detta arbete pekar mot en ny klass av cellterapi. Istället för att rikta in sig på en tumörmarkör i taget siktar ACE‑iMac‑celler på att brett återställa immunsituationen inne i solida tumörer, vilket potentiellt gör cancer både mer synlig och mer sårbar för kroppens egna försvar.
Citering: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Nyckelord: cancerimmunterapi, makrofager, inducerade pluripotenta stamceller, angiotensin‑konverterande enzym, solida tumörer