Clear Sky Science · fr
Macrophages humains dérivés d’iPSC bio‑ingénierés avec expression accrue de l’enzyme de conversion de l’angiotensine (ECA) suppriment la croissance des tumeurs solides
Retourner nos propres défenseurs contre le cancer
L’immunothérapie du cancer a modifié le pronostic pour certains patients, mais de nombreuses tumeurs trouvent encore des moyens de se cacher du système immunitaire ou de l’épuiser. Cette étude explore une nouvelle manière de suralimenter l’un des défenseurs naturels du corps — les macrophages — en les reprogrammant en laboratoire pour qu’ils deviennent bien plus agressifs contre les tumeurs solides. Les résultats laissent entrevoir un avenir où les médecins pourraient infuser aux patients des cellules immunitaires sur mesure qui attaquent un large éventail de cancers sans avoir besoin de reconnaître un marqueur tumoral spécifique.
Pourquoi les macrophages comptent en cancérologie
Les macrophages sont des globules blancs qui jouent à la fois le rôle d’éboueurs et de soldats de première ligne. Dans de nombreuses tumeurs solides, ils sont abondants — mais souvent dans le mauvais mode. Plutôt que d’attaquer, ils basculent dans un état « réparateur » qui aide en réalité les tumeurs à croître, se propager et échapper aux autres cellules immunitaires. Les auteurs ont raisonnablement pensé que s’ils pouvaient pousser de façon fiable les macrophages vers un état inflammatoire et fortement actif — et les y maintenir dans la tumeur — ces cellules pourraient à la fois tuer directement les cellules cancéreuses et mobiliser d’autres combattants immunitaires comme les lymphocytes T et les cellules tueuses naturelles (NK).
Emprunter une enzyme de la pression artérielle pour renforcer l’immunité
L’équipe s’est concentrée sur l’enzyme de conversion de l’angiotensine (ECA), mieux connue pour son rôle dans le contrôle de la pression artérielle et comme cible de médicaments cardiaques courants. Des travaux antérieurs chez la souris laissaient entendre que des niveaux plus élevés d’ECA dans les cellules myéloïdes, y compris les macrophages, renforcent leur capacité à lutter contre les infections et les tumeurs. Dans cette étude, les chercheurs ont transposé cette idée au système humain. Ils ont utilisé des cellules souches pluripotentes induites — des cellules adultes reprogrammées à un état proche de la souche — et ont inséré un interrupteur génétique qui leur permet d’augmenter ou de diminuer le niveau d’ECA avec l’antibiotique courant doxycycline. À partir de ces cellules souches modifiées, ils ont produit en grande quantité des macrophages à la demande, une plateforme évolutive qu’ils appellent ACE‑iMac.
Construire des macrophages surpuissants en laboratoire
Lorsque l’interrupteur ECA était activé, les cellules ACE‑iMac obtenues semblaient et se comportaient très différemment des macrophages cultivés en laboratoire classiques. Elles libéraient des quantités beaucoup plus élevées de signaux inflammatoires, généraient de fortes poussées d’espèces réactives de l’oxygène et d’oxyde nitrique — armes chimiques qui endommagent les cellules tumorales — et présentaient des profils d’expression génique associés à un état fortement activé de type « M1 ». Dans le même temps, elles réduisaient la production de molécules liées à un mode plus suppressif et favorable à la tumeur. In vitro, les cellules ACE‑iMac ralentissaient la croissance de mélanomes, de cancers du sein triple négatifs et de cellules de cancers tête‑et‑cou résistantes aux médicaments bien plus efficacement que des macrophages témoins.
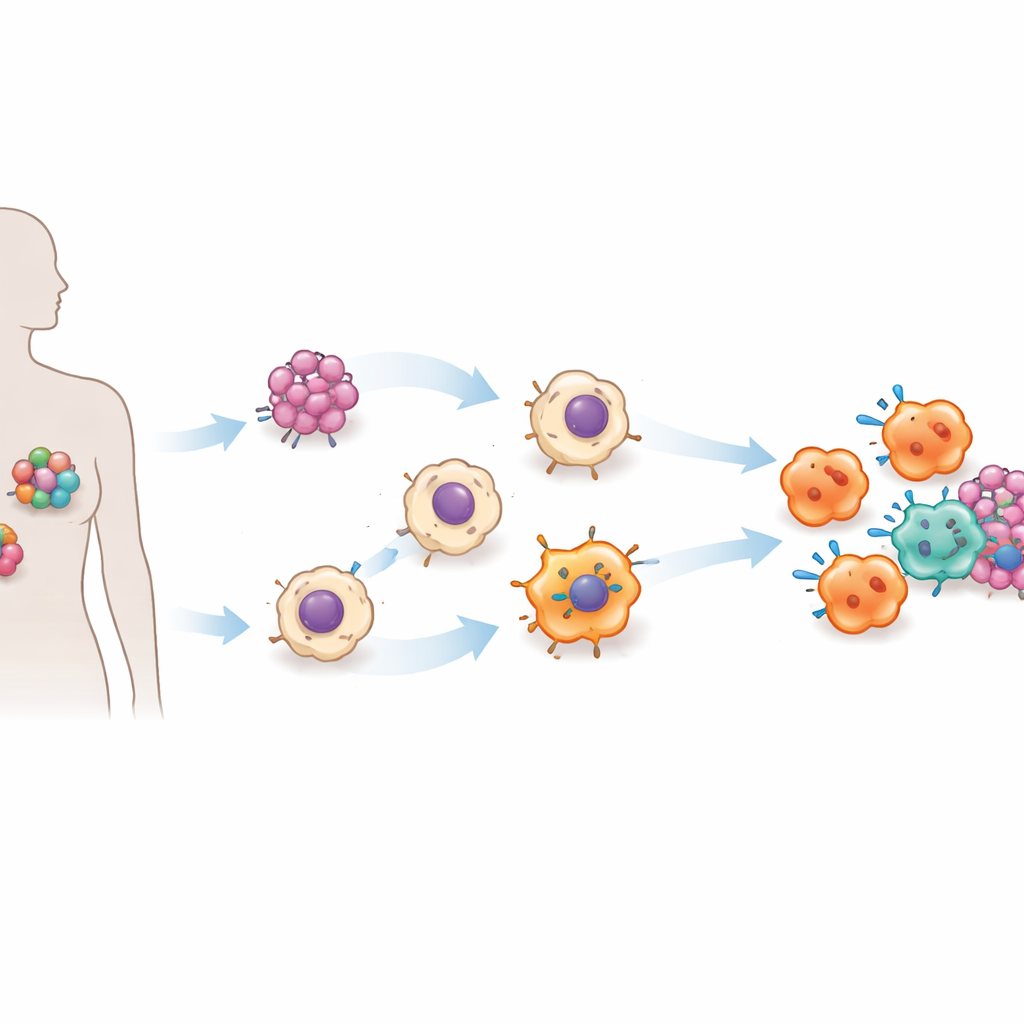
Arrêter les tumeurs et réveiller les autres cellules immunitaires
Le test crucial a été réalisé dans des modèles murins portant des tumeurs humaines. Lorsque des cellules ACE‑iMac ont été injectées directement dans des tumeurs solides, ces tumeurs ont rétréci de façon spectaculaire — d’environ trois quarts ou plus par rapport aux tumeurs recevant des macrophages ordinaires. Cela s’est avéré vrai pour des modèles de mélanome, de cancer du sein et de cancers tête‑et‑cou. À l’intérieur des tumeurs, les cellules ACE‑iMac présentaient de fortes signatures inflammatoires et s’accompagnaient d’un plus grand nombre de cellules NK activées et, chez des souris humanisées disposant d’un système immunitaire humain fonctionnel, de lymphocytes T cytotoxiques humains plus puissants. Fait intéressant, le nombre global de ces autres cellules immunitaires ne changeait pas beaucoup ; elles devenaient plutôt plus activées, ce qui suggère que les ACE‑iMac agissent comme des entraîneurs sur place qui dynamisent la réponse immunitaire globale plutôt que d’apporter simplement davantage de combattants.
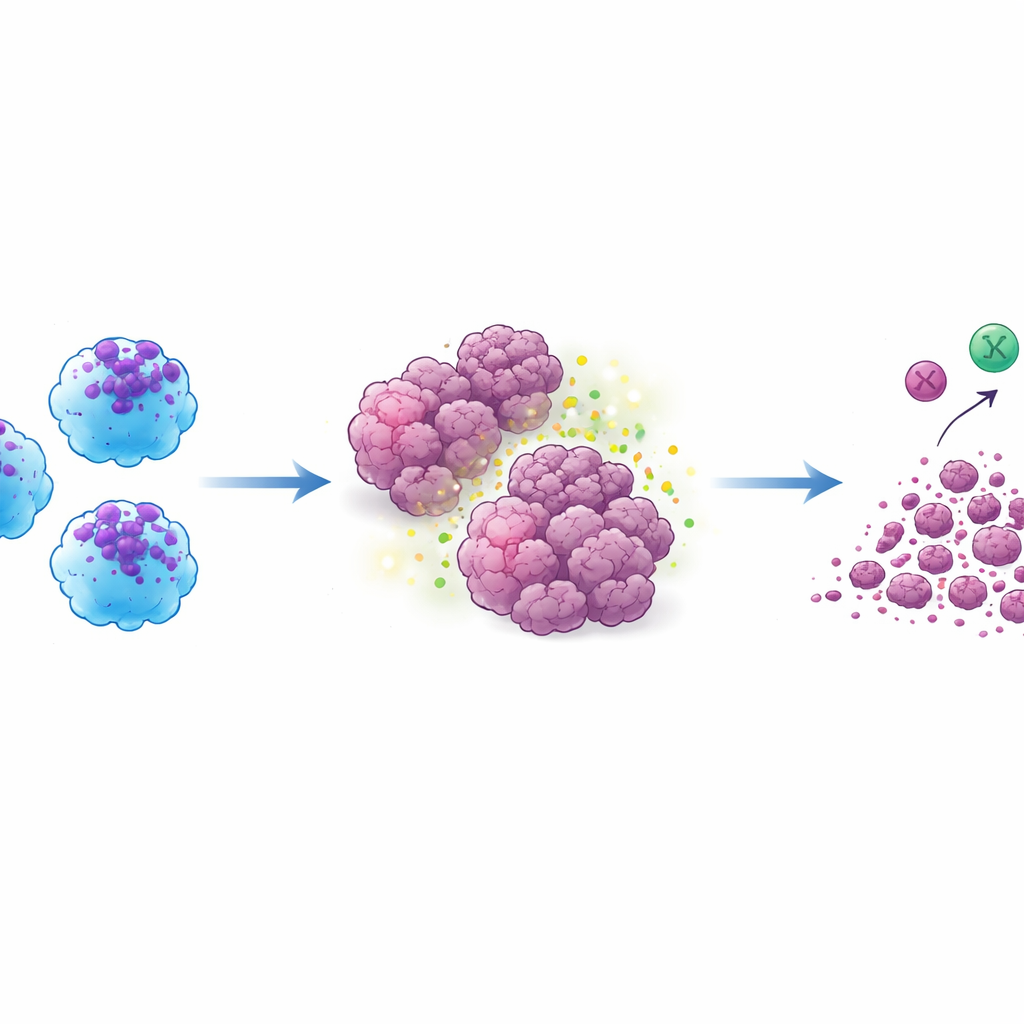
Décoder les mécanismes internes
Pour comprendre ce qui pilote ce comportement, les chercheurs ont examiné l’activité génique globale des cellules ACE‑iMac. L’activation de l’ECA a renforcé des réseaux liés à l’activation macrophagique classique, à la production de cytokines, au traitement des antigènes et à l’assemblage de « estomacs » cellulaires appelés phagosomes qui digèrent les cibles. Elle a aussi modulé des voies aidant les macrophages à présenter des fragments de protéines tumorales aux lymphocytes T, ce qui peut expliquer la réponse T plus forte observée chez les souris humanisées. Sous une stimulation de type tumoral, les ACE‑iMac montraient des gains supplémentaires dans des gènes impliqués dans le métabolisme et la différenciation, des changements qui les aident probablement à rester actives dans l’environnement tumoral hostile plutôt que de s’épuiser ou de changer de camp.
Ce que cela pourrait signifier pour les soins du cancer
Pour un non‑spécialiste, la conclusion est que les auteurs ont conçu une source contrôlable et renouvelable de macrophages humains qui se comportent comme des chasseurs de tumeurs hautement focalisés et des amplificateurs immunitaires. En augmentant les niveaux d’ECA uniquement lorsque nécessaire grâce à un médicament externe, ils peuvent, en principe, régler l’intensité et le timing de cette réponse, ce qui pourrait améliorer la sécurité. De nombreuses étapes restent à franchir avant une utilisation clinique — tests d’administration intraveineuse, sécurité à long terme et combinaisons avec des thérapies existantes — mais ce travail ouvre la voie à une nouvelle classe de thérapies cellulaires. Plutôt que de cibler un marqueur tumoral à la fois, les cellules ACE‑iMac visent à réinitialiser largement le paysage immunitaire à l’intérieur des tumeurs solides, rendant potentiellement le cancer plus visible et plus vulnérable aux défenses naturelles de l’organisme.
Citation: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Mots-clés: immunothérapie du cancer, macrophages, cellules souches pluripotentes induites, enzyme de conversion de l'angiotensine, tumeurs solides