Clear Sky Science · de
Bioengineered iPSC-abgeleitete menschliche Makrophagen mit erhöhter Angiotensin-konvertierender Enzym‑(ACE)Expression unterdrücken das Wachstum solider Tumoren
Unsere eigenen Verteidiger gegen Krebs wenden
Die Krebsimmuntherapie hat die Prognose für einige Patientinnen und Patienten verbessert, doch viele Tumoren finden weiterhin Wege, sich vor dem Immunsystem zu verstecken oder es zu erschöpfen. Diese Studie untersucht einen neuen Ansatz, um einen der natürlichen Verteidiger des Körpers — Makrophagen — zu verstärken, indem man sie im Labor so umprogrammiert, dass sie gegenüber soliden Tumoren weit aggressiver werden. Die Arbeit deutet auf eine Zukunft hin, in der Ärztinnen und Ärzte maßgeschneiderte Immunzellen verabreichen könnten, die ein breites Spektrum von Krebserkrankungen angreifen, ohne einen einzelnen spezifischen Tumormarker erkennen zu müssen.
Warum Makrophagen in der Krebsbekämpfung wichtig sind
Makrophagen sind weiße Blutkörperchen, die sowohl als Müllabfuhr als auch als Frontsoldaten dienen. In vielen soliden Tumoren sind sie zahlreich — aber oft im falschen Modus. Statt anzugreifen, verweilen sie in einem „heilenden“ Zustand, der Tumoren tatsächlich beim Wachstum, bei der Ausbreitung und beim Entkommen vor anderen Immunzellen hilft. Die Autoren vermuteten, dass, wenn man Makrophagen zuverlässig in einen durchschlagskräftigen, entzündlichen Zustand versetzen und diesen Zustand im Tumor aufrechterhalten könnte, diese Zellen sowohl Krebszellen direkt töten als auch andere Immunakteure wie T‑Zellen und natürliche Killerzellen (NK‑Zellen) mobilisieren könnten.
Ein Blutdruckenzym als Immunverstärker nutzen
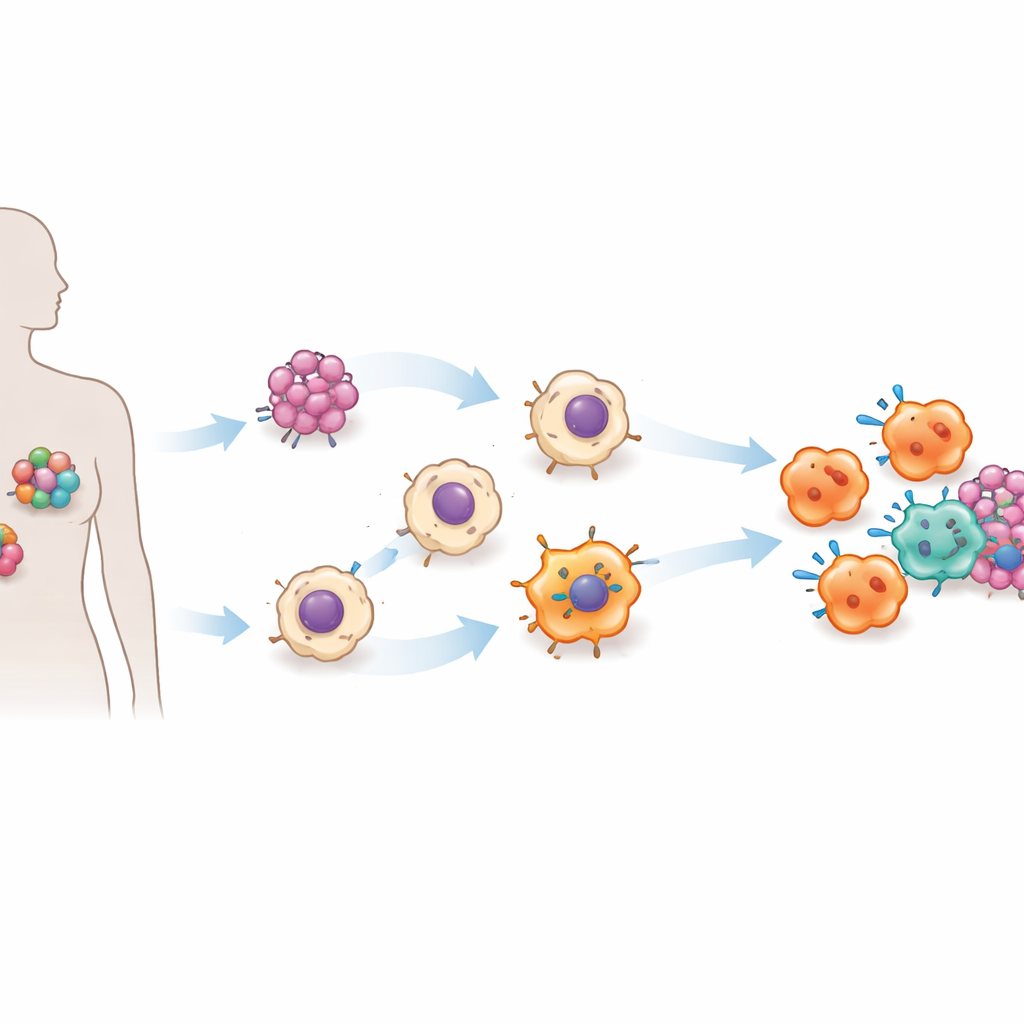
Das Team konzentrierte sich auf das Angiotensin‑konvertierende Enzym (ACE), das vor allem für seine Rolle bei der Blutdruckregulation und als Ziel üblicher Herzmedikamente bekannt ist. Frühere Arbeiten in Mäusen deuteten darauf hin, dass höhere ACE‑Spiegel in myeloiden Zellen, einschließlich Makrophagen, diese Zellen besser bei der Bekämpfung von Infektionen und Tumoren machen. In dieser Studie überführten die Forschenden diese Idee in ein menschliches System. Sie verwendeten induzierte pluripotente Stammzellen — ausgereifte Zellen, die zurück in einen stammesähnlichen Zustand reprogrammiert wurden — und fügten einen genetischen Schalter ein, mit dem sich ACE‑Spiegel mittels des verbreiteten Antibiotikums Doxycyclin hoch- oder herunterregeln lassen. Aus diesen gentechnisch veränderten Stammzellen erzeugten sie auf Abruf große Mengen an Makrophagen, eine skalierbare Plattform, die sie ACE‑iMac nennen.
Supergeladene Makrophagen im Labor erzeugen
Wenn der ACE‑Schalter eingeschaltet wurde, unterschieden sich die resultierenden ACE‑iMac‑Zellen in Aussehen und Verhalten deutlich von gewöhnlichen im Labor gezüchteten Makrophagen. Sie setzten deutlich höhere Mengen entzündlicher Signale frei, erzeugten große Ausbrüche reaktiver Sauerstoff‑ und Stickstoffspezies — chemische Waffen, die Tumorzellen schädigen — und zeigten Genaktivitätsmuster, die mit einem stark aktivierten, „M1‑ähnlichen“ Zustand assoziiert sind. Gleichzeitig verringerten sie die Produktion von Molekülen, die mit einem eher unterdrückenden, tumorfördernden Modus verbunden sind. In Kulturphasen verlangsamten ACE‑iMac‑Zellen das Wachstum von Melanom-, dreifach negativem Brustkrebs‑ und medikamentenresistenten Kopf‑ und Halskrebszellen deutlich wirksamer als Kontrollmakrophagen.
Tumoren stoppen und andere Immunzellen wecken
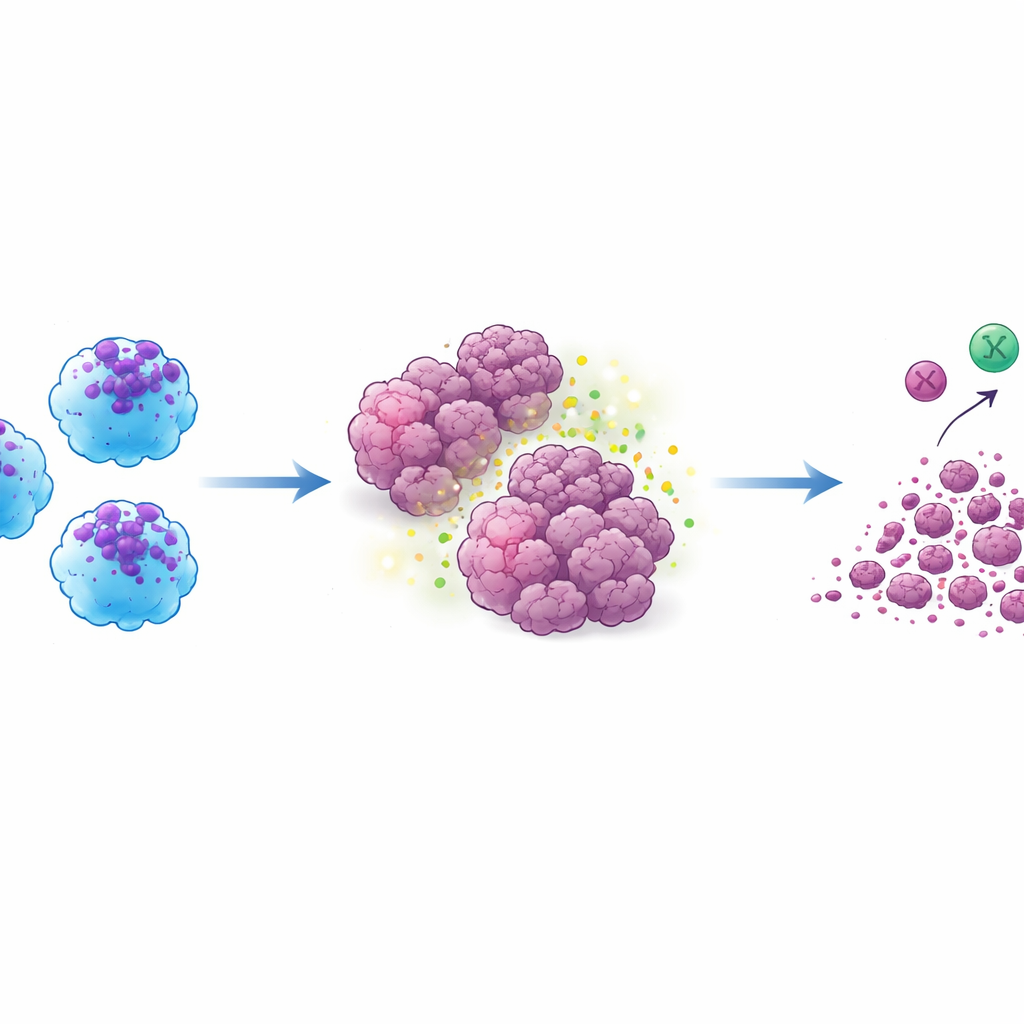
Die entscheidende Prüfung fand in Mausmodellen mit humanen Tumoren statt. Wurden ACE‑iMac‑Zellen direkt in solide Tumoren injiziert, schrumpften diese Tumoren dramatisch — um etwa drei Viertel oder mehr im Vergleich zu Tumoren, die gewöhnliche Makrophagen erhielten. Dies galt über Melanom‑, Brust‑ und Kopf‑Hals‑Krebsmodelle hinweg. Innerhalb der Tumoren zeigten ACE‑iMac‑Zellen starke entzündliche Signaturen und traten zusammen mit aktiveren NK‑Zellen und — in speziell humanisierten Mäusen mit funktionierendem menschlichem Immunsystem — mit stärkeren humanen zytotoxischen T‑Zellen auf. Interessanterweise veränderte sich die Gesamtzahl dieser anderen Immunzellen nicht stark; vielmehr wurden sie aktiver. Das legt nahe, dass ACE‑iMac‑Zellen vor Ort als Trainer fungieren, die die breitere Immunantwort ankurbeln, anstatt lediglich zusätzliche Kämpfer hinzuzufügen.
Die inneren Mechanismen entschlüsseln
Um zu verstehen, was dieses Verhalten antreibt, untersuchten die Forschenden die globale Genaktivität in ACE‑iMac‑Zellen. Das Einschalten von ACE verstärkte Netzwerke, die mit klassischer Makrophagenaktivierung, Zytokinproduktion, Antigenverarbeitung und dem Aufbau von zellulären „Mägen“ namens Phagosomen verbunden sind, die Zielstrukturen verdauen. Es stimmte außerdem Pfade ab, die Makrophagen dabei helfen, Bruchstücke von Tumorproteinen T‑Zellen zu präsentieren, was die stärkere T‑Zell‑Antwort in humanisierten Mäusen erklären könnte. Unter tumorähnlicher Stimulation zeigten ACE‑iMac‑Zellen weitere Zuwächse in Genen, die an Stoffwechsel und Differenzierung beteiligt sind — Änderungen, die ihnen wahrscheinlich helfen, in der harten Tumorumgebung aktiv zu bleiben, anstatt erschöpft zu werden oder die Seite zu wechseln.
Was das für die künftige Krebsbehandlung bedeuten könnte
Für Nicht‑Spezialisten lässt sich zusammenfassen: Die Autoren haben eine kontrollierbare, erneuerbare Quelle menschlicher Makrophagen geschaffen, die wie hoch fokussierte Tumorjäger und Immunverstärker agieren. Indem sie die ACE‑Spiegel nur bei Bedarf mit einem externen Medikament erhöhen, können sie prinzipiell Stärke und Timing dieser Reaktion steuern, was die Sicherheit verbessern könnte. Zwar sind vor einer Anwendung am Menschen noch viele Schritte nötig — darunter die Prüfung einer intravenösen Verabreichung, Langzeitsicherheit und Kombinationen mit bestehenden Therapien —, doch deutet diese Arbeit auf eine neue Klasse von Zelltherapien hin. Anstatt jeweils einen Tumormarker anzuzielen, zielen ACE‑iMac‑Zellen darauf ab, die Immunlandschaft innerhalb solider Tumoren breit umzustimmen und damit Krebs sowohl sichtbarer als auch anfälliger für die körpereigenen Abwehrkräfte zu machen.
Zitation: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Schlüsselwörter: Krebsimmuntherapie, Makrophagen, induzierte pluripotente Stammzellen, Angiotensin‑konvertierendes Enzym, solide Tumoren