Clear Sky Science · ar
البلعميات البشرية المشتقة من الخلايا الجذعية متعددة القدرات المحورة وراثيًا مع زيادة في تعبير إنزيم تحويل الأنجيوتنسين (ACE) تثبط نمو الأورام الصلبة
تحويل مدافعينا الذاتيين ضد السرطان
غيّرت العلاجات المناعية للسرطان توقعات المصابين في بعض الحالات، لكن العديد من الأورام لا تزال تجد طرقًا للاختفاء من جهاز المناعة أو إرهاقه. تستكشف هذه الدراسة نهجًا جديدًا لتقوية أحد المدافعين الطبيعيين في الجسم—البلعميات—عن طريق إعادة برمجتها مخبريًا لجعلها أكثر عدوانية تجاه الأورام الصلبة. وتقترح النتائج مستقبلًا قد يقوم فيه الأطباء بضخ خلايا مناعية مُفصَّلة حسب الحاجة تهاجم مجموعة واسعة من السرطانات دون الحاجة إلى التعرف على علامة ورمية محددة واحدة.
لماذا تهم البلعميات في السرطان
البلعميات هي خلايا دم بيضاء تعمل كجامعي نفايات وجنود في الخطوط الأمامية في الوقت نفسه. داخل العديد من الأورام الصلبة، تكون وفيرة—لكن غالبًا في الوضع الخاطئ. فبدلًا من الهجوم، تنزلق إلى حالة "مُعافِية" تساعد الأورام على النمو والانتشار والتهرب من خلايا المناعة الأخرى. افترض الباحثون أنه إذا أمكن دفع البلعميات بثبات إلى حالة التهابية شديدة والحفاظ عليها داخل الورم، فقد تتمكن هذه الخلايا من قتل الخلايا السرطانية مباشرة وتحفيز مقاتلين مناعيين آخرين مثل الخلايا التائية والخلايا القاتلة الطبيعية.
استعارة إنزيم خافض للضغط لتعزيز المناعة
ركَّز الفريق على إنزيم تحويل الأنجيوتنسين (ACE)، المعروف بدوره في ضبط ضغط الدم وكهدف لأدوية القلب الشائعة. أشارت أعمال سابقة في الفئران إلى أن ارتفاع مستويات ACE في الخلايا النخاعية، بما في ذلك البلعميات، يجعل هذه الخلايا أفضل في مواجهة العدوى والأورام. في هذه الدراسة، نقل الباحثون هذه الفكرة إلى نظام بشري. استخدموا خلايا جذعية متعددة القدرات المحفزة—خلايا بالغة أعيد برمجتها إلى حالة تشبه الخلايا الجذعية—وأدخلوا مفتاحًا جينيًا يتيح لهم تعديل مستويات ACE صعودًا أو هبوطًا باستخدام المضاد الحيوي الشائع دوكسيسيكلين. ومن هذه الخلايا الجذعية المحورة، أنتجوا أعدادًا كبيرة من البلعميات عند الطلب، وهو منصة قابلة للتوسع يسمونها ACE-iMac.
بناء بلعميات فائقة الشحن في المختبر
عندما شُغِّل مفتاح ACE، بدت خلايا ACE-iMac المتحصل عليها وتصرّفت بشكل مختلف للغاية عن البلعميات المزروعة مخبريًا العادية. أفرزت كميات أكبر بكثير من الإشارات الالتهابية، وتولدت فيها دفعات كبيرة من الأكسجين التفاعلي وأكسيد النيتريك—أسلحة كيميائية تضرّ الخلايا الورمية—وأظهرت أنماط نشاط جيني مرتبطة بحالة تنشيطية عالية تشبه "M1". وفي الوقت نفسه، خفَّضت إنتاج جزيئات مرتبطة بحالة أكثر قمعًا تساعد الورم. في أطباق الثقافة، أبطأت خلايا ACE-iMac نمو خلايا الميلانوما وسرطان الثدي ثلاثي السلائف وسرطان الرأس والعنق المقاوم للأدوية بفعالية أكبر بكثير من البلعميات الضابطة.
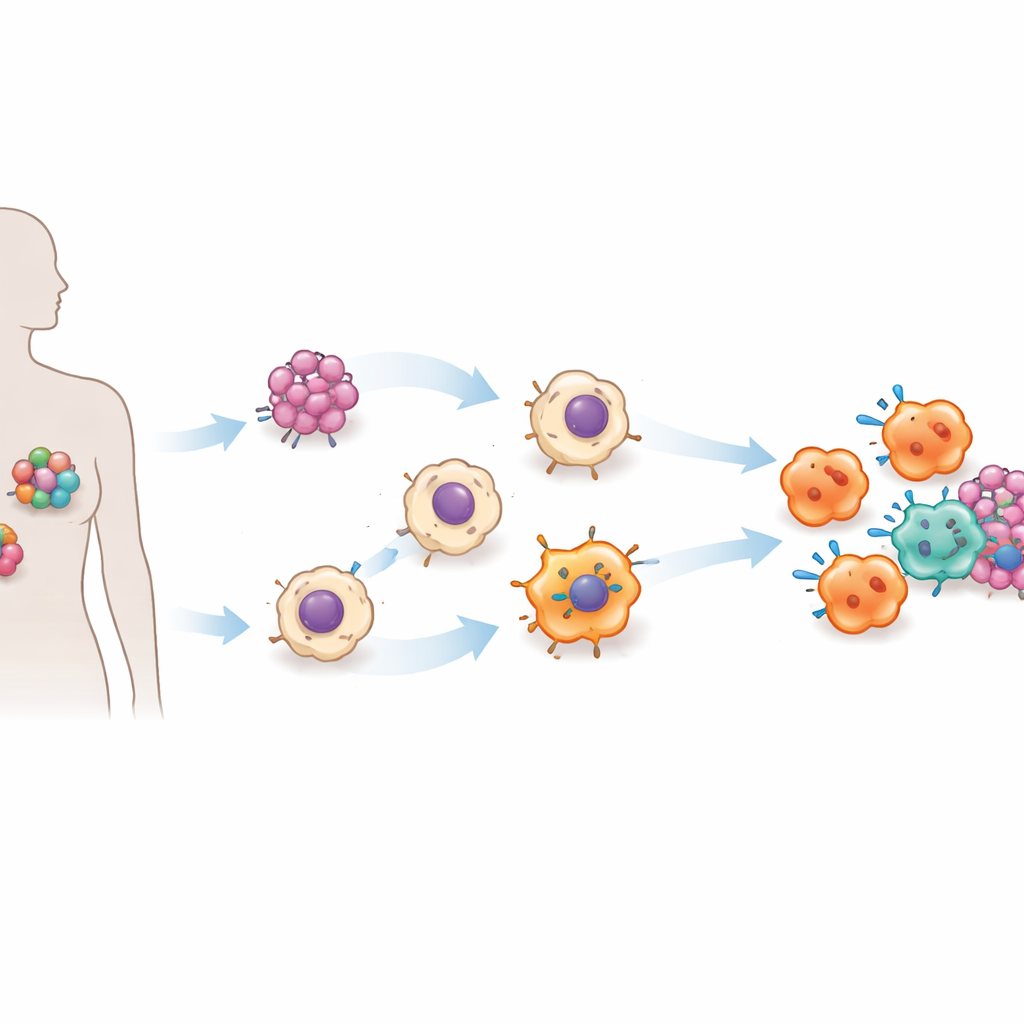
إيقاف الأورام وإيقاظ خلايا مناعية أخرى
كانت الاختبار الحاسم في نماذج الفئران الحاملة لأورام بشرية. عندما حقنوا خلايا ACE-iMac مباشرة داخل الأورام الصلبة، تقلصت تلك الأورام بشكل دراماتيكي—بمقدار يقارب ثلاثة أرباع أو أكثر مقارنة بالأورام التي تلقت بلعميات عادية. كان هذا صحيحًا عبر نماذج الميلانوما والثدي والرأس والعنق. داخل الأورام، أظهرت خلايا ACE-iMac توقيعات التهابية قوية ورافقها نشاط أكبر للخلايا القاتلة الطبيعية، وفي فئران مُؤنثة خصيصًا تمتلك جهاز مناعي بشري وظيفي، ظهرت خلايا تائية بشرية قاتلة أقوى. ومن المثير للاهتمام أن العدد الإجمالي لهذه الخلايا المناعية الأخرى لم يتغير كثيرًا؛ بل أصبحت أكثر تنشيطًا، مما يشير إلى أن خلايا ACE-iMac تعمل كمدربين في الموقع ينعشون الاستجابة المناعية الأوسع بدلًا من مجرد إضافة مقاتلين جدد.
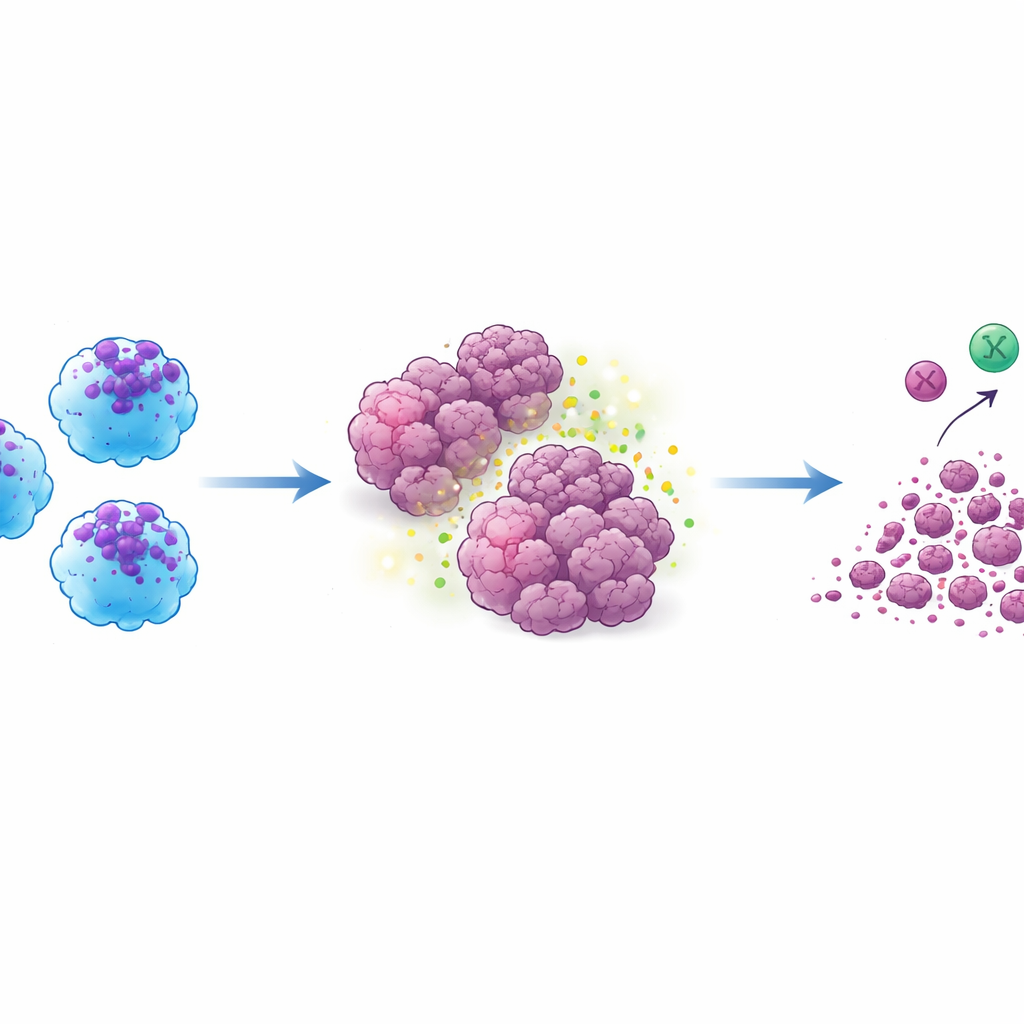
فك تشفير الآليات الداخلية
لفهم ما يقود هذا السلوك، فحص الباحثون النشاط الجيني الشامل في خلايا ACE-iMac. أدى تشغيل ACE إلى تعزيز الشبكات المرتبطة بالتنشيط التقليدي للبلعميات، وإنتاج السيتوكينات، ومعالجة المستضدات، وتشكيل "المِعَدان الخَلَوِي" المسمى الحويصلات البلعومية التي تهضم الأهداف. كما ضَبَّط مسارات تساعد البلعميات على تقديم شظايا من بروتينات الورم للخلايا التائية، مما قد يفسر استجابة الخلايا التائية الأقوى في الفئران المؤنثة بالبشر. تحت تحفيز يشابه بيئة الورم، أظهرت خلايا ACE-iMac مكاسب إضافية في جينات متعلقة بالتمثيل الغذائي والتمايز، تغييرات قد تساعدها على البقاء نشطة في بيئة الورم القاسية بدلًا من الاستنزاف أو الانقسام إلى الجانب المؤيد للورم.
ماذا قد يعني هذا لرعاية السرطان في المستقبل
لغير المتخصص، الخلاصة أن المؤلفين بنوا مصدرًا متحكمًا ومتجددًا من البلعميات البشرية التي تتصرف كمطاردين مركزين للأورام ومحفزين للمناعة. عن طريق رفع مستويات ACE فقط عند الحاجة باستخدام دواء خارجي، يمكنهم من حيث المبدأ ضبط قوة وتوقيت هذه الاستجابة، مما قد يحسّن السلامة. وبينما تبقى خطوات عديدة قبل الاستخدام السريري—بما في ذلك اختبار التسليم عن طريق الوريد، والسلامة على المدى الطويل، والتكامل مع العلاجات الحالية—تشير هذه العمل إلى فئة جديدة من العلاج الخلوي. بدلًا من استهداف علامة ورمية واحدة في كل مرة، تهدف خلايا ACE-iMac إلى إعادة ضبط المشهد المناعي داخل الأورام الصلبة بشكل واسع، مما قد يجعل السرطان أكثر وضوحًا وأكثر عرضة لمدافعات الجسم نفسها.
الاستشهاد: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
الكلمات المفتاحية: المناعة المناعية للسرطان, البلعميات, الخلايا الجذعية متعددة القدرات المحفزة, إنزيم تحويل الأنجيوتنسين, الأورام الصلبة