Clear Sky Science · nl
Bio-geëngineerde, uit iPSC afgeleide humane macrofagen met verhoogde expressie van angiotensine-converterend enzym (ACE) remmen de groei van solide tumoren
Onze eigen verdedigers tegen kanker inzetten
Kankerimmunotherapie heeft het vooruitzicht voor sommige patiënten veranderd, maar veel tumoren vinden nog steeds manieren om zich te verbergen voor of het immuunsysteem uit te putten. Deze studie onderzoekt een nieuwe manier om een van de natuurlijke verdedigers van het lichaam — macrofagen — te versterken door ze in het laboratorium te herprogrammeren zodat ze veel agressiever ten opzichte van solide tumoren optreden. Het werk suggereert een toekomst waarin artsen patiënten kunnen infuseren met op maat gemaakte immuuncellen die een breed scala aan kankers aanvallen zonder afhankelijk te zijn van herkenning van één specifiek tumormarker.
Waarom macrofagen belangrijk zijn bij kanker
Macrofagen zijn witte bloedcellen die zowel fungeren als opruimers als frontlinie-soldaten. In veel solide tumoren zijn ze talrijk — maar vaak in de verkeerde toestand. In plaats van aan te vallen, schakelen ze over naar een "herstellende" staat die tumoren juist helpt groeien, uitzaaien en andere immuuncellen te ontwijken. De onderzoekers redeneerden dat als ze macrofagen betrouwbaar in een krachtig, ontstekingsgericht stadium konden duwen en ze daarbinnen in de tumor konden houden, deze cellen zowel kankercellen direct zouden kunnen doden als andere immuunstrijders zoals T-cellen en natural killer (NK)-cellen zouden kunnen mobiliseren.
Een bloeddrukenzym lenen voor immuunkracht
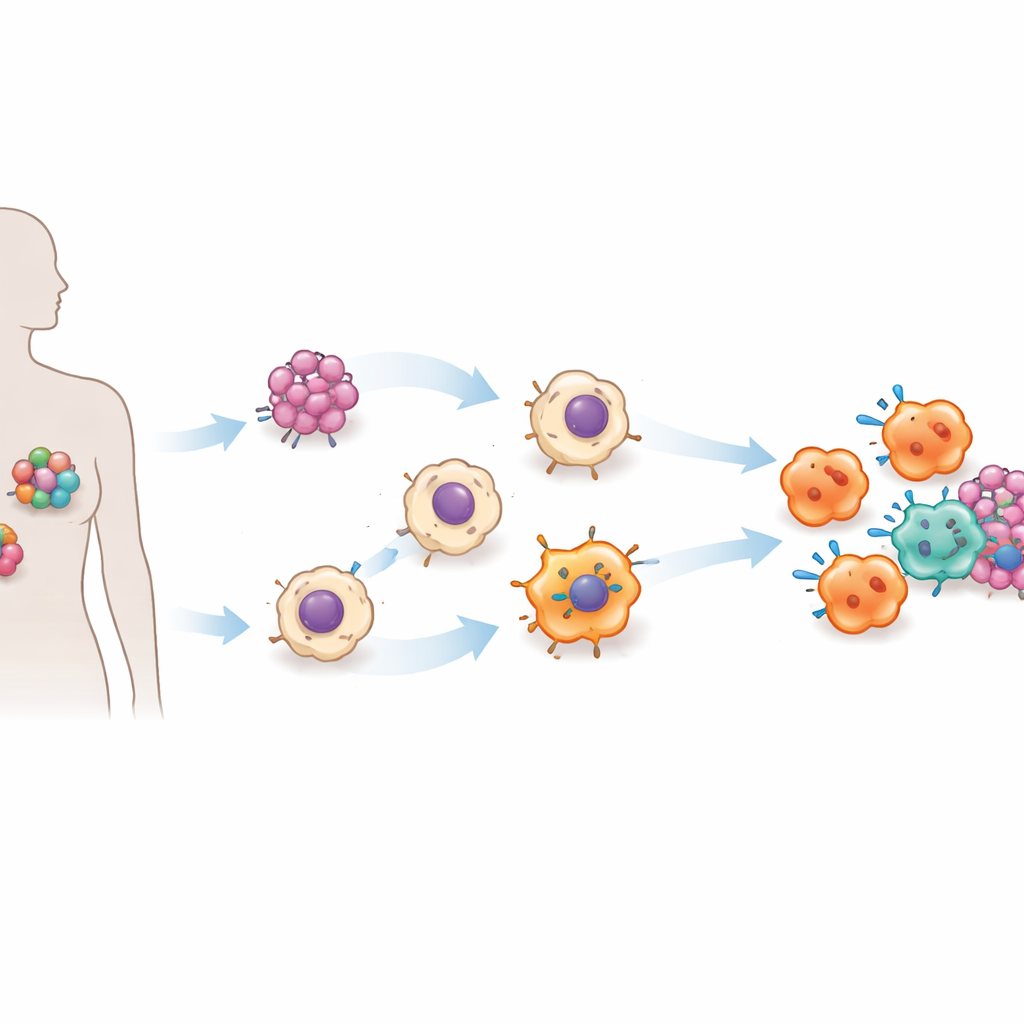
Het team richtte zich op het angiotensine-converterende enzym (ACE), vooral bekend om zijn rol in de regulatie van de bloeddruk en als doelwit van veelgebruikte hartmedicijnen. Vroegere muisstudies wezen erop dat hogere ACE-niveaus in myeloïde cellen, waaronder macrofagen, deze cellen beter maken in het bestrijden van infecties en tumoren. In deze studie brachten de onderzoekers dat idee naar een menselijk systeem. Ze gebruikten geïnduceerde pluripotente stamcellen — volwassen cellen die teruggeprogrammeerd zijn naar een stamcelachtige staat — en introduceerden een genetische schakelaar waarmee ze ACE-niveaus omhoog of omlaag kunnen draaien met het veelgebruikte antibioticum doxycycline. Uit deze gemodificeerde stamcellen produceerden ze op aanvraag grote aantallen macrofagen, een schaalbaar platform dat ze ACE-iMac noemen.
Supercharged macrofagen in het laboratorium bouwen
Wanneer de ACE-schakelaar werd ingeschakeld, zagen en gedroegen de resulterende ACE-iMac-cellen zich heel anders dan gewone in het lab gekweekte macrofagen. Ze gaven veel grotere hoeveelheden ontstekingssignalen af, genereerden grote uitbarstingen van reactieve zuurstof en stikstofoxide — chemische wapens die tumorcellen beschadigen — en toonden genactiviteitspatronen die geassocieerd zijn met een sterk geactiveerde, "M1-achtige" toestand. Tegelijkertijd verminderden ze de productie van moleculen die gekoppeld zijn aan een meer onderdrukkende, tumorbevorderende modus. In kweekschalen vertraagden ACE-iMac-cellen de groei van melanoom, triple-negatieve borstkanker en geneesmiddelresistente hoofd- en halskankercellen veel effectiever dan controlemacrofagen.
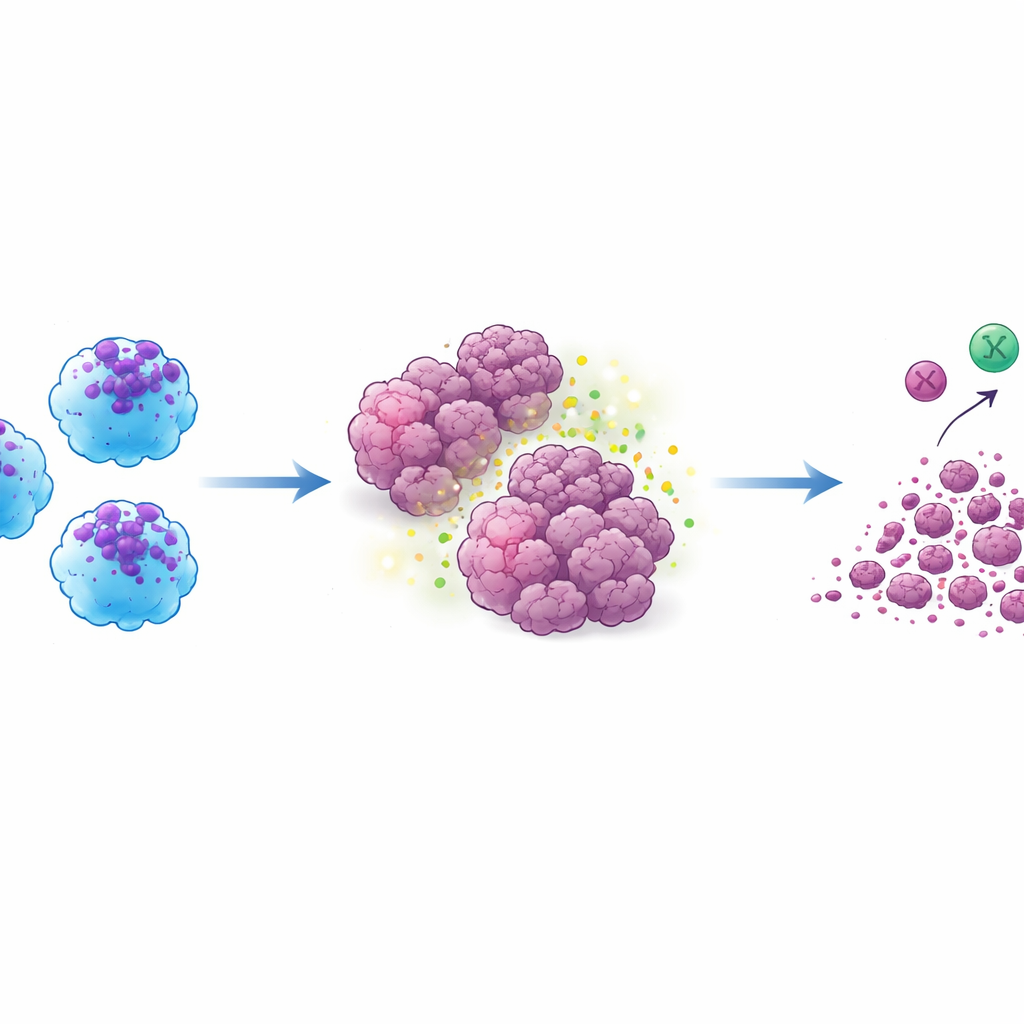
Tumoren stoppen en andere immuuncellen activeren
De cruciale test vond plaats in muismodellen met menselijke tumoren. Wanneer ACE-iMac-cellen direct in solide tumoren werden geïnjecteerd, krimpten die tumoren dramatisch — met ongeveer driekwart of meer vergeleken met tumoren die gewone macrofagen kregen. Dit gold voor modellen van melanoom, borstkanker en hoofd- en halskanker. Binnenin de tumoren toonden ACE-iMac-cellen sterke ontstekingshandtekeningen en gingen ze gepaard met actiever NK-cellen en, in speciaal gehumaniseerde muizen met een functioneel menselijk immuunsysteem, krachtigere menselijke cytotoxische T-cellen. Interessant genoeg veranderde het totale aantal van deze andere immuuncellen niet veel; in plaats daarvan raakten ze meer geactiveerd, wat suggereert dat ACE-iMac-cellen fungeren als coaches ter plaatse die de bredere immuunrespons energieker maken in plaats van simpelweg meer strijders toe te voegen.
De interne werking ontcijferen
Om te begrijpen wat dit gedrag aandrijft, onderzochten de onderzoekers de globale genactiviteit in ACE-iMac-cellen. Het inschakelen van ACE versterkte netwerken die verband houden met klassieke macrophage-activatie, cytokineproductie, antigeenverwerking en de opbouw van cellulaire "maagjes" genaamd fagosomen die targets verteren. Het stemde ook paden af die macrofagen helpen fragmenten van tumorproteïnen aan T-cellen te presenteren, wat de sterkere T-celrespons in gehumaniseerde muizen kan verklaren. Onder tumorlijnde stimulatie vertoonden ACE-iMac-cellen extra verbeteringen in genen die betrokken zijn bij stofwisseling en differentiatie, veranderingen die hen waarschijnlijk helpen actief te blijven in de vijandige tumoromgeving in plaats van uitgeput te raken of van kant te wisselen.
Wat dit zou kunnen betekenen voor toekomstige kankerzorg
Voor een niet-specialist komt het neer op dit: de auteurs hebben een controleerbare, hernieuwbare bron van menselijke macrofagen ontwikkeld die zich gedragen als scherp gerichte tumorjagers en immuunversterkers. Door ACE-niveaus alleen te verhogen wanneer dat nodig is met een extern middel, kunnen ze in principe de sterkte en timing van deze respons afstemmen, wat de veiligheid kan verbeteren. Hoewel er veel stappen nodig zijn voordat dit bij patiënten kan worden toegepast — waaronder testen van intraveneuze toediening, langetermijnveiligheid en combinaties met bestaande therapieën — wijst dit werk op een nieuwe klasse van celtherapie. In plaats van telkens één tumormarker te targeten, streven ACE-iMac-cellen ernaar het immuunsysteem in solide tumoren breed te resetten, waardoor kanker mogelijk zichtbaarder en kwetsbaarder wordt voor de eigen verdedigingsmechanismen van het lichaam.
Bronvermelding: Shibata, T., Bhat, S., Cao, D. et al. Bioengineered iPSC-derived human macrophages with increased angiotensin-converting enzyme (ACE) expression suppress solid tumor growth. Sig Transduct Target Ther 11, 132 (2026). https://doi.org/10.1038/s41392-026-02650-3
Trefwoorden: kankerimmunotherapie, macrofagen, geïnduceerde pluripotente stamcellen, angiotensine-converterend enzym, solide tumoren