Clear Sky Science · zh
K‑Ras Gly12 突变对结肠上皮稳态与肿瘤发生的影响
癌症基因的微小变化为何重要
结肠癌是最常见的癌症之一,许多病例由名为 KRAS 的基因损伤驱动。长期以来临床发现,携带 KRAS 突变的肿瘤患者通常对治疗反应较差,但并非所有 KRAS 改变都相同。本研究提出了一个看似简单却对精准医学有重大意义的问题:三种常见的 KRAS 突变在结肠中是否表现不同,且这些差异能否被用于开发更有效的个体化治疗?
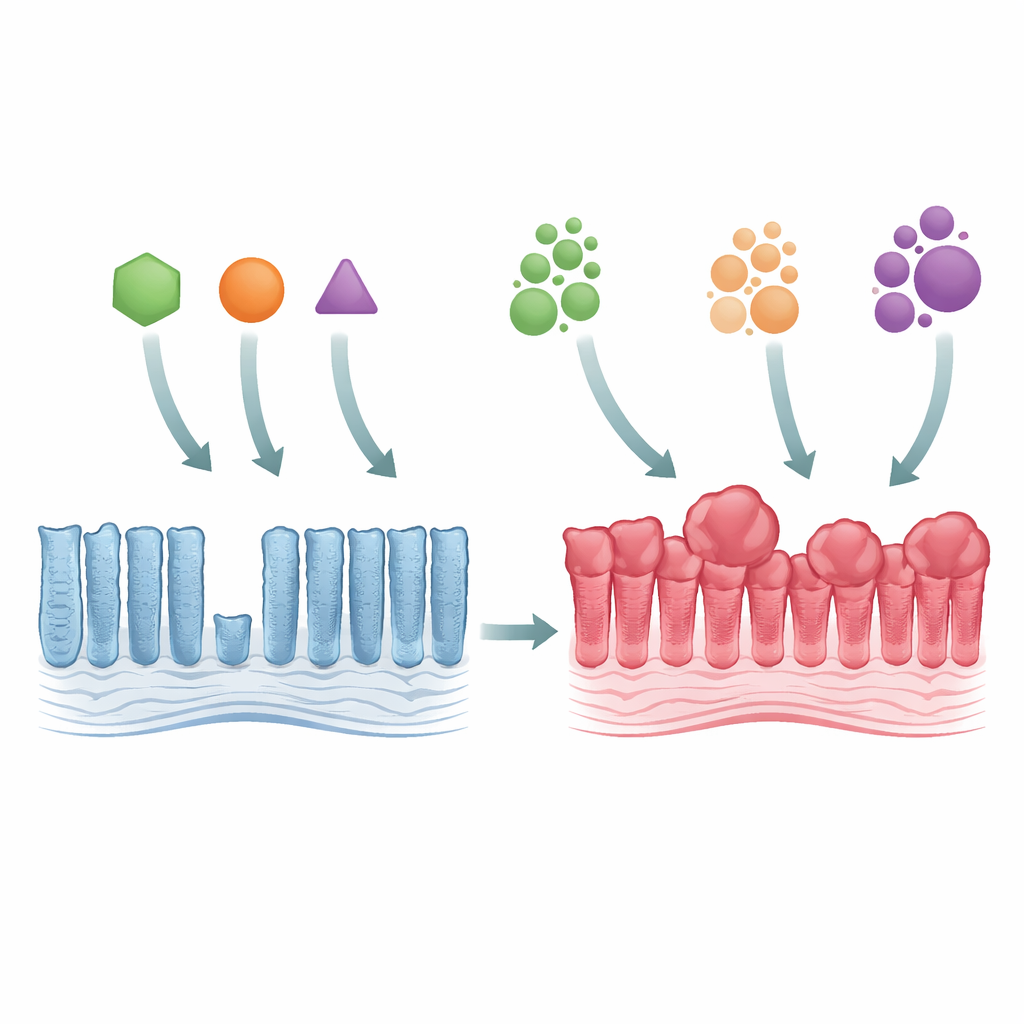
从正常肠上皮到早期肿瘤生长
研究者使用基因工程小鼠模拟三种主要的 KRAS 突变,这些突变都作用于蛋白中的同一位残基(称为 Gly12),但以不同方式改变该位点(G12C、G12D 和 G12V)。当这些突变任一在结肠上皮被激活时,组织变得更厚并且更拥挤,腺体拉长且成熟细胞过多。尽管出现这种过度生长,细胞分裂的实际区域并未明显扩大,提示问题并非细胞产生更快,而是细胞更新变慢。所有三种突变均强烈激活了称为 MAPK 的生长控制通路,并导致某些特殊肠细胞群被抑制,表明即便是微小的基因变化也能广泛扰乱肠道的内在平衡。
表面相似的肿瘤,截然不同的结局
为研究癌症形成,团队将每种 KRAS 突变与肿瘤抑制基因 APC 的丢失结合,这是人类结肠癌中的常见早期事件。所得的肿瘤在显微镜下均呈相似外观,并显示出 KRAS 驱动的核心生长通路的可比激活水平。然而小鼠的结局并不相同。携带 G12D 突变的动物发展出最多的肿瘤且存活期最短,G12V 居中,而 G12C 肿瘤最少且存活更久。在体外培养的这些小鼠来源迷你肿瘤(类器官)对新型 KRAS 抑制药的反应也各不相同:G12D 肿瘤最难被消灭,G12V 最敏感,G12C 则位于中间并且其反应依赖于药物的作用方式。
小鼠与人类共享的生长程式
为了解这些突变在细胞内的作用,研究者对小鼠肿瘤和人类结肠癌数据集进行了全局基因表达和蛋白水平测量。他们发现跨物种存在共同的 KRAS 突变“签名”:推动细胞分裂并支持 MAPK 生长通路的基因被激活,而许多能量代谢基因被下调,与癌细胞重塑能量利用方式一致。若干参与反馈回路的基因和蛋白——无论是放大还是试图抑制 KRAS 信号——都持续升高。研究组还观察到与炎症和免疫信号相关通路的增强活性,提示这些突变可能在疾病早期就帮助塑造有利于肿瘤的微环境。
一种突变的特殊弱点
尽管存在这一共享的核心程式,G12C 突变表现出独特之处。携带 G12C 的肿瘤显示出对发育相关通路(如 Wnt/β‑catenin 和 Notch)的额外激活,这些通路影响细胞命运的决定。单独使用抑制这些通路的药物对所有突变体的影响大致相似。但当研究者将一种 G12C 特异性的 KRAS 抑制剂与 Wnt 或 Notch 抑制剂联合使用时,带有 G12C 突变的类器官显著缩小,远超过 G12D 或 G12V。这表明 G12C 驱动的肿瘤尤其依赖这些附加通路,同时同时靶向 KRAS 与其辅助通路能将其推向崩溃。
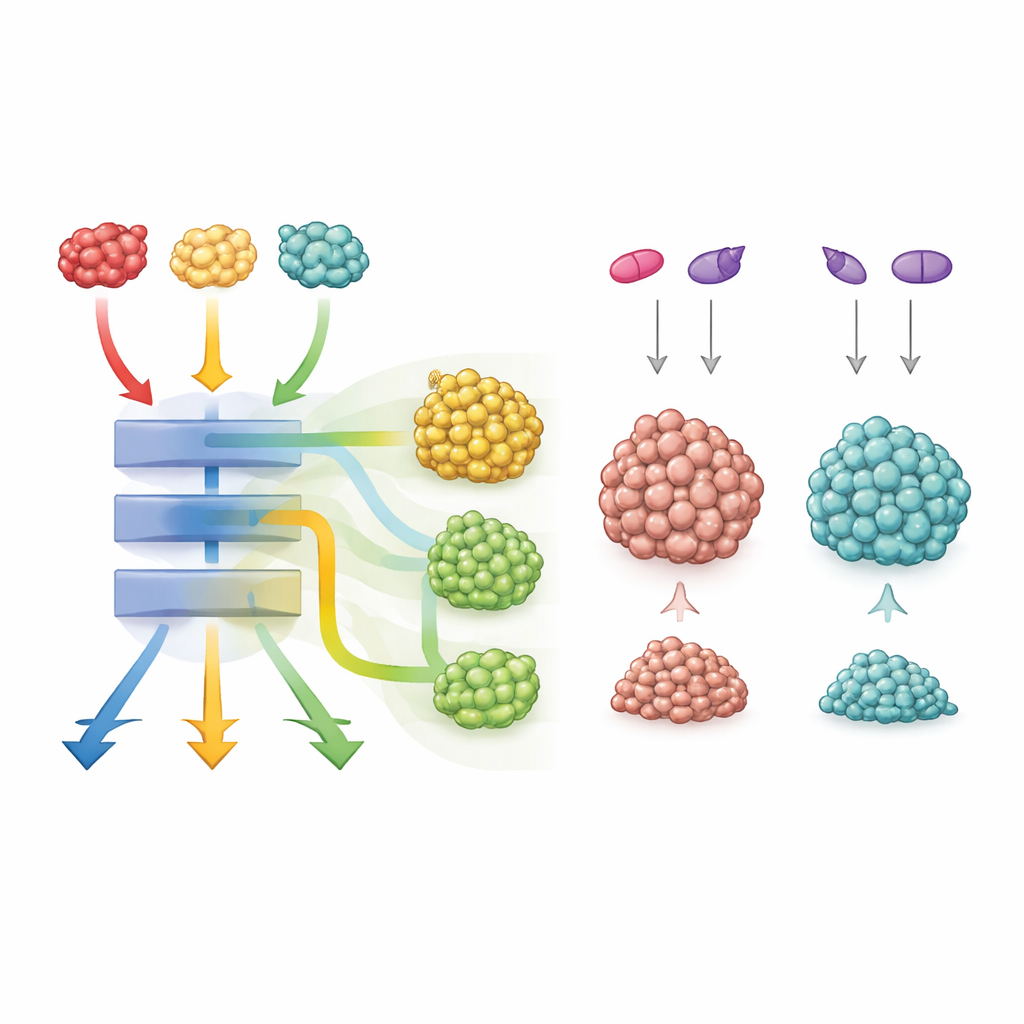
对未来癌症治疗的意义
总体而言,该研究表明位于同一位点的三种 KRAS 突变可以产生外观相似但在生长、存活和药物反应上截然不同的结肠肿瘤。它们共享推动细胞分裂和代谢重编程的强大核心引擎,但每种突变以自身方式微调额外的信号网络。对于患者而言,这意味着仅知道肿瘤是“KRAS 突变”并不够。明确是哪一种 KRAS 变体以及它招募了哪些伴随通路,可能指导更聪明的靶向药物组合——尤其对 G12C 突变,将 KRAS 抑制剂与 Wnt 或 Notch 抑制剂配合,或许为更有效的治疗打开新途径。
引用: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
关键词: KRAS 突变, 结肠癌, 等位基因特异性治疗, 肿瘤信号传导, 联合靶向