Clear Sky Science · sv
Effekten av K-Ras Gly12-mutander på homeostas och tumörutveckling i kolonets epitel
Varför små förändringar i en cancergen spelar roll
Koloncancer är en av de vanligaste cancerformerna, och många fall drivs av skador i en gen som kallas KRAS. Läkare har länge vetat att patienter med tumörer som bär KRAS-mutationer ofta svarar dåligt på behandling, men alla KRAS-förändringar är inte likadana. Denna studie ställer en till synes enkel fråga med stora konsekvenser för precisionmedicin: beter sig tre mycket vanliga varianter av muterat KRAS olika i kolon, och kan dessa skillnader utnyttjas för mer effektiva, skräddarsydda behandlingar?
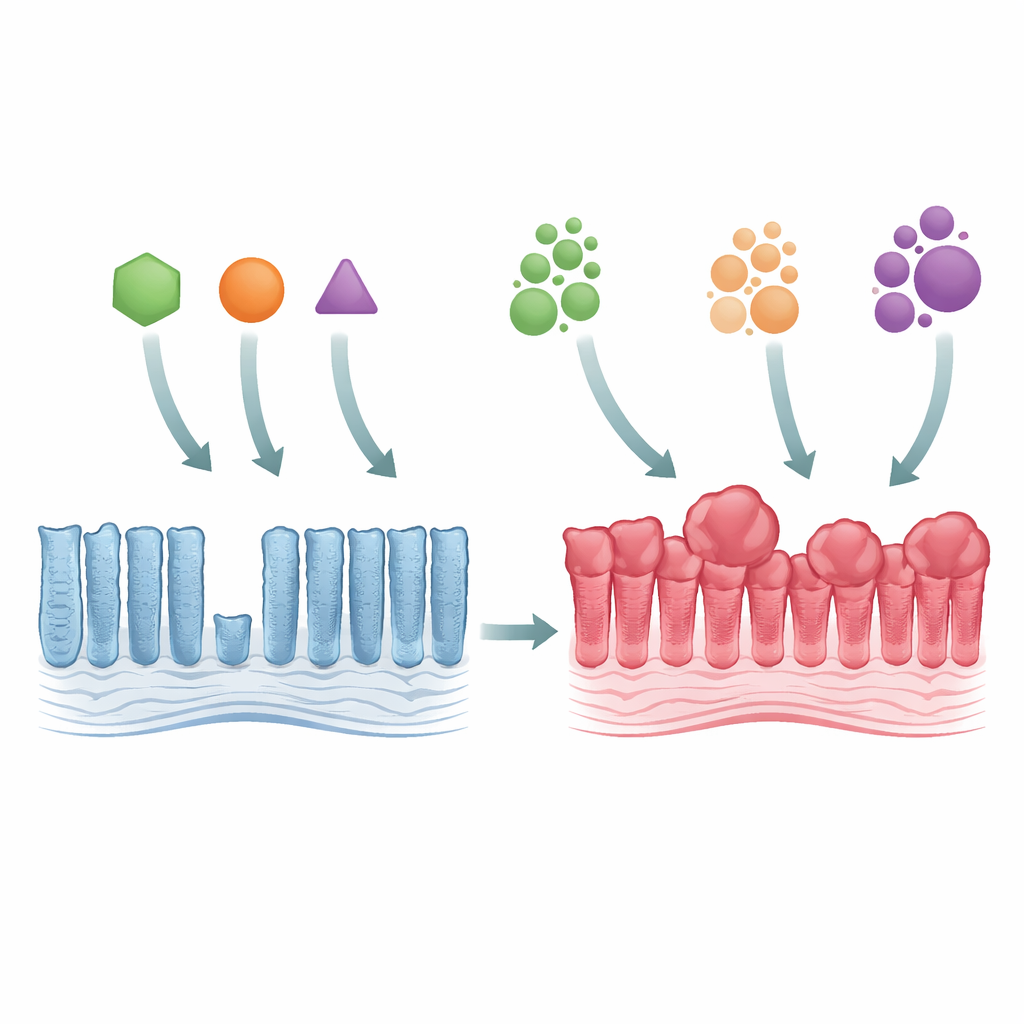
Från normalt tarmepitel till tidig tumörtillväxt
Forskarna använde genetiskt modifierade möss för att efterlikna tre stora KRAS-mutationer, alla som påverkar samma byggsten i proteinet (kallad Gly12) men förändrar den på olika sätt (G12C, G12D och G12V). När någon av dessa mutanter aktiverades i kolonets epitel blev vävnaden tjockare och mer trång, med förlängda körtlar och ett överskott av mogna celler. Trots denna överväxt expanderade den faktiska zonen där cellerna delade sig inte mycket, vilket tyder på att problemet inte var snabbare celldelning utan långsammare cellomsättning. Alla tre mutanter aktiverade starkt en tillväxtkontrollerande bana känd som MAPK, och de utplånade vissa specialiserade tarmceller, vilket visar att även subtila genetiska förändringar kan rubba tarmens inre balans i stor omfattning.
Tumörer som ser lika ut men ger mycket olika utfall
För att studera tumörbildning kombinerade teamet varje KRAS-mutant med förlust av tumörsupressorgenet APC, ett vanligt tidigt steg i mänsklig koloncancer. De resulterande tumörerna såg alla likartade ut i mikroskop och visade jämförbar aktivering av den kärnmässiga tillväxtbanan som drivs av KRAS. Ändå klarade sig inte mössen lika bra. Djur med G12D-mutationen utvecklade flest tumörer och hade kortast överlevnad, de med G12V var i ett mellanläge, och de med G12C hade färre tumörer och levde längre. Mini‑tumörer odlade i laboratoriet från dessa möss (organoider) visade också olika svar på nya KRAS‑hämmare: G12D‑tumörer var svårast att döda, G12V mest känsliga, och G12C hamnade mitt emellan och svarade olika beroende på läkemedlets verkningssätt.
Delade tillväxtprogram i möss och människor
För att förstå vad dessa mutationer gjorde inne i cellerna mätte forskarna global genaktivitet och proteinnivåer både i mus‑tumörer och i mänskliga koloncancer-dataset. De fann en vanlig KRAS‑mutant "signatur" över arter: gener som driver celldelning och stöder MAPK‑tillväxtbanan var påslagna, medan många gener för energimetabolism var nedreglerade, i linje med att cancerceller omprogrammerar hur de använder bränsle. Flera gener och proteiner som verkar i återkopplingsslingor—antingen förstärkande eller som försöker dämpa KRAS‑signaleringen—var konsekvent förhöjda. Teamet såg också starkare aktivitet i banor kopplade till inflammation och immunsignaler, vilket antyder att dessa mutationer tidigt kan bidra till att forma en tumörvänlig mikromiljö.
En särskild sårbarhet hos en mutant
Trots detta delade kärnprogram stack en mutant, G12C, ut. Tumörer med G12C visade extra aktivering av utvecklingsbanor såsom Wnt/β‑catenin och Notch, som påverkar hur celler bestämmer sina öden. På egen hand hade läkemedel som blockerade dessa banor liknande effekter över alla mutanter. Men när forskarna kombinerade en G12C‑specifik KRAS‑hämmare med blockerare av Wnt eller Notch krympte organoider med G12C‑mutationen dramatiskt, mycket mer än de med G12D eller G12V. Detta tyder på att G12C‑drivna tumörer lutar särskilt tungt mot dessa kompletterande banor och kan övertalas att kollapsa när både KRAS och dess hjälpbanar riktas samtidigt.
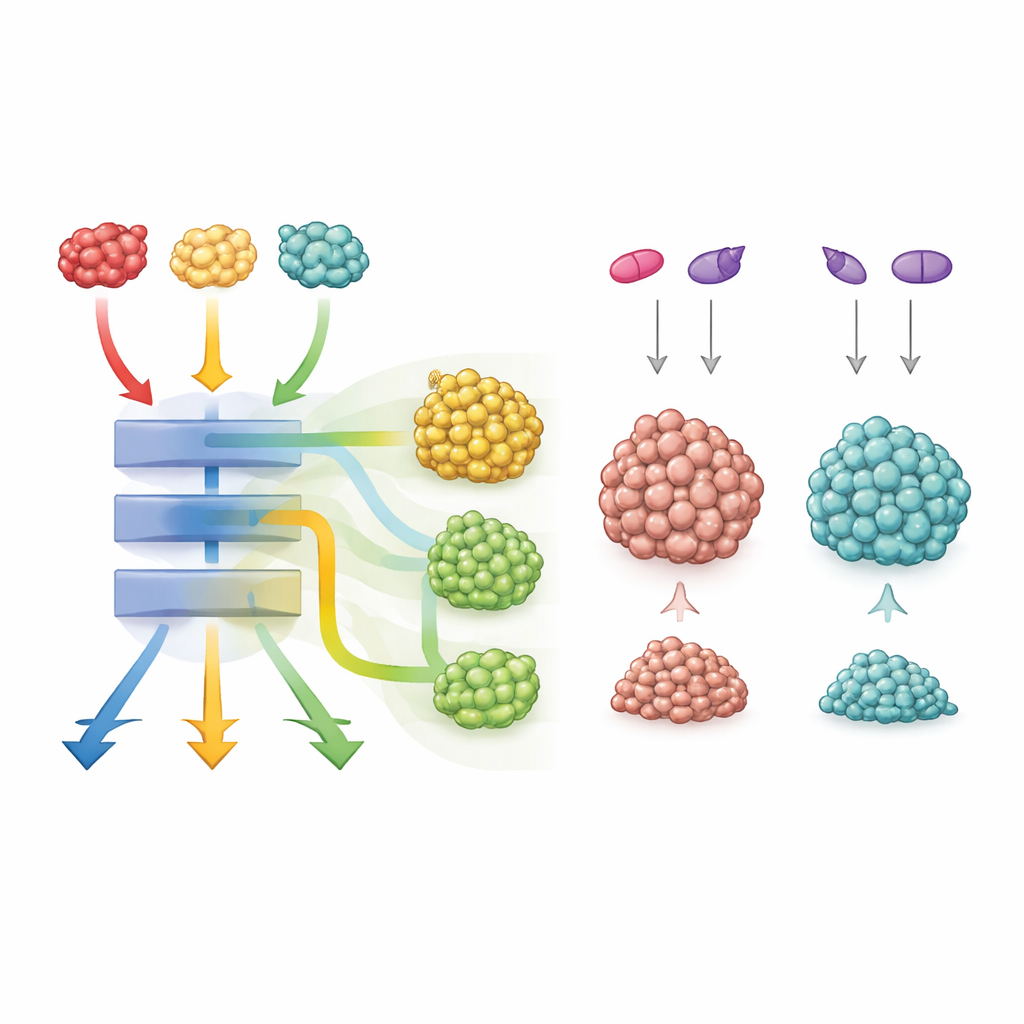
Vad detta betyder för framtida cancerbehandling
Sammantaget visar studien att tre KRAS‑mutationer på exakt samma position kan ge kolontumörer som ser likadana ut men beter sig mycket olika vad gäller tillväxt, överlevnad och läkemedelssvar. Alla delar en kraftfull kärnmotor som driver celldelning och metabol omkoppling, men varje mutant finjusterar ytterligare signalnätverk på sitt sätt. För patienter innebär detta att det inte räcker att veta att en tumör är "KRAS‑muterad". Att förstå exakt vilken KRAS‑förändring som finns och vilka partnerbanor den engagerar kan vägleda smartare kombinationer av riktade läkemedel—särskilt för G12C‑mutanten, där att para ihop KRAS‑hämmare med Wnt‑ eller Notch‑blockerare kan erbjuda en ny väg till bättre behandlingar.
Citering: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Nyckelord: KRAS-mutationer, koloncancer, allel-specifik terapi, tumörsignalering, kombinationsinriktning