Clear Sky Science · tr
Kolonik epitelde K-Ras Gly12 mutantlerinin homeostaz ve tümör oluşumu üzerindeki etkisi
Kanser genindeki küçük değişiklikler neden önemli
Kolon kanseri en yaygın kanserlerden biridir ve birçok vaka KRAS adlı bir gendeki hasar tarafından yönlendirilir. Doktorlar uzun süredir tümörleri KRAS mutasyonu taşıyan hastaların sıklıkla tedaviye kötü yanıt verdiğini biliyordu, ancak tüm KRAS değişiklikleri aynı değildir. Bu çalışma, hassas tıp için büyük çıkarımları olan aldatıcı derecede basit bir soruyu soruyor: çok yaygın üç farklı mutant KRAS kolonda farklı davranıyor mu ve bu farklılıklar daha etkili, kişiye özel tedavilere dönüştürülebilir mi?
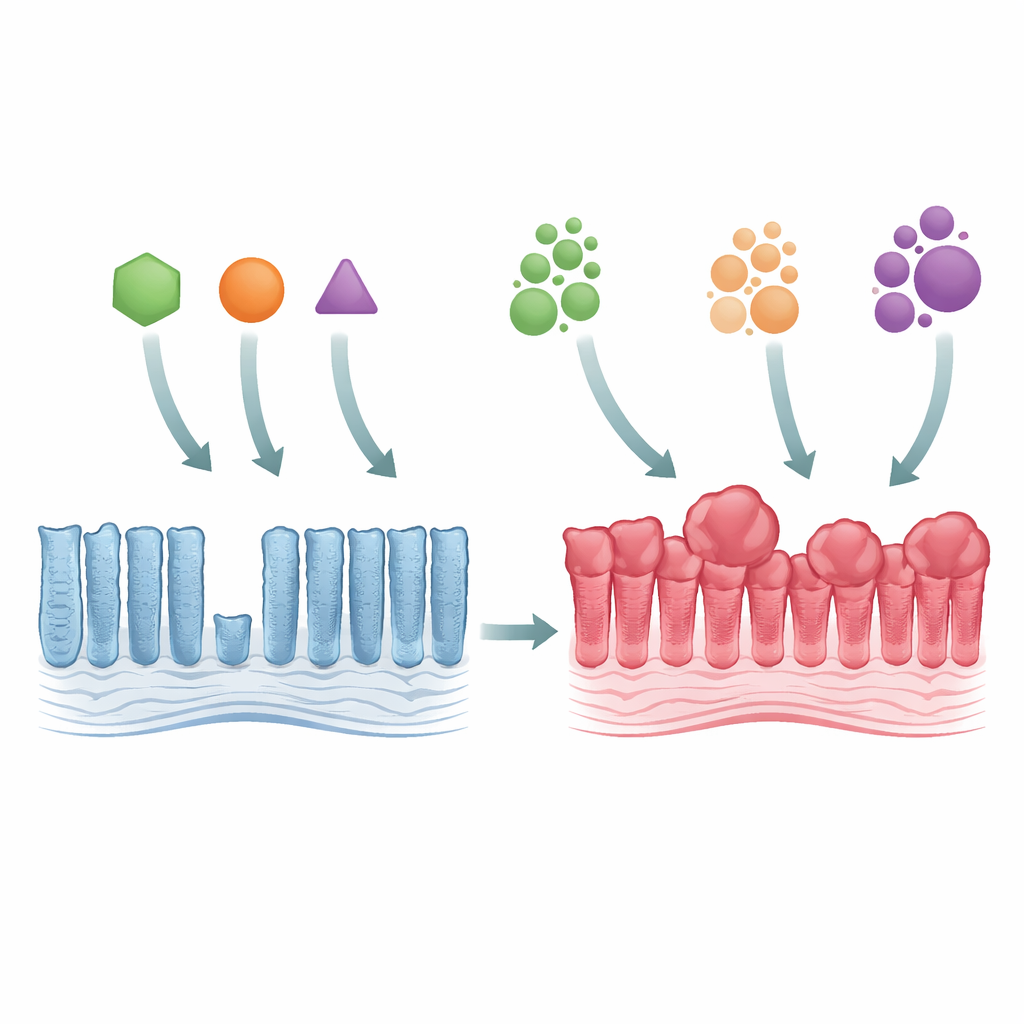
Normal bağırsak örtüsünden erken tümör büyümesine
Araştırmacılar, proteindeki aynı yapı taşını (Gly12) etkileyen ama farklı şekillerde değiştiren üç ana KRAS mutasyonunu (G12C, G12D ve G12V) taklit etmek için genetik olarak değiştirilmiş fareler kullandılar. Bu mutasyonların herhangi biri kolon örtüsünde etkinleştirildiğinde, doku kalınlaştı ve daha sıkışık hale geldi; bezeler uzadı ve olgun hücrelerde artış görüldü. Bu aşırı büyümeye rağmen hücrelerin bölündüğü bölge çok genişlemedi; bu da sorunun daha hızlı hücre doğumundan değil, hücre yenilenmesinin yavaşlamasından kaynaklandığını düşündürüyor. Üç mutant da MAPK olarak bilinen büyüme-kontrol yolunu güçlü şekilde etkinleştirdi ve belirli özelleşmiş bağırsak hücrelerini yok etti; bu da küçük genetik değişikliklerin bağırsak iç dengesini geniş ölçekte bozabileceğini gösteriyor.
Benzeyen tümörler, çok farklı sonuçlar
Tümör oluşumunu incelemek için ekip her KRAS mutantını, insan kolon kanserinde sık görülen erken bir olay olan tümör baskılayıcı gen APC kaybıyla birleştirdi. Ortaya çıkan tümörlerin mikroskop altında görünümü benzerdi ve KRAS tarafından yönlendirilen ana büyüme yolunun benzer düzeyde etkinleşmesini gösterdiler. Ancak farelerin kaderi aynı olmadı. G12D mutasyonuna sahip hayvanlar en çok tümörü geliştirdi ve en kısa sağkalımı gösterdi; G12V ara düzeydeydi; G12C ise daha az tümöre sahip oldu ve daha uzun yaşadı. Bu farelerden laboratuvarda büyütülen mini-tümörler (organoidler) de yeni KRAS-engelleyici ilaçlara farklı tepkiler gösterdi: G12D tümörleri öldürmesi en zor olanlar, G12V en hassas olanlar, G12C ise arada kaldı ve ilacın etki mekanizmasına bağlı olarak farklı yanıt verdi.
Fareler ve insanlarda paylaşılan büyüme programları
Bu mutasyonların hücre içinde ne yaptığını anlamak için araştırmacılar fare tümörlerinde ve insan kolon kanseri veri setlerinde genel gen aktivitesi ve protein düzeylerini ölçtüler. Türler arasında ortak bir KRAS mutant “imzası” buldular: hücre bölünmesini destekleyen ve MAPK büyüme yolunu güçlendiren genler açığa çıkmışken, birçok enerji metabolizması geni aşağı çekilmişti; bu, kanser hücrelerinin yakıt kullanımını yeniden düzenlediğiyle uyumlu. KRAS sinyalini ya güçlendiren ya da sınırlamaya çalışan geri besleme döngülerinde yer alan birkaç gen ve protein tutarlı şekilde yükselmişti. Ekip ayrıca iltihap ve bağışıklık sinyalleriyle ilişkili yolların daha güçlü aktivitesini gördü; bu, bu mutasyonların hastalığın erken döneminde tümör-dostu bir mikroçevre şekillendirmeye yardımcı olabileceğini işaret ediyor.
Bir mutantta özel bir zayıflık
Bu paylaşılan çekirdek programa rağmen, G12C bir mutant olarak öne çıktı. G12C taşıyan tümörler Wnt/β-katenin ve Notch gibi hücre kaderini etkileyen gelişimsel yolların ekstra aktivasyonunu gösterdi. Tek başına bu yolları bloke eden ilaçlar tüm mutantlarda benzer etkiler gösterdi. Ancak araştırmacılar G12C-spesifik bir KRAS inhibitörünü Wnt veya Notch bloke edicilerle birleştirdiklerinde, G12C organoidleri dramatik şekilde küçüldü; bu etki G12D veya G12V taşıyanlarda çok daha azdı. Bu, G12C kaynaklı tümörlerin özellikle bu ek yollara güçlü şekilde dayanma eğiliminde olduğunu ve hem KRAS hem de yardımcı yollar aynı anda hedeflendiğinde kritik eşiklerin aşılabileceğini düşündürüyor.
Bu bulguların gelecekteki kanser bakımına anlamı
Genel olarak, çalışma aynı pozisyondaki üç KRAS mutasyonunun kolon tümörleri görüntü olarak benzer olabilse de büyüme, sağkalım ve ilaç yanıtı açısından oldukça farklı davranışlar üretebileceğini gösteriyor. Hepsi hücre bölünmesini ve metabolik yeniden programlamayı sürdüren güçlü bir çekirdek motoru paylaşıyor, ancak her mutant ilave sinyal ağlarını kendi biçiminde ince ayarlıyor. Hastalar için bunun anlamı, bir tümörün yalnızca “KRAS-mutant” olduğunu bilmenin yeterli olmadığıdır. Hangi KRAS değişikliğinin bulunduğunu ve hangi partner yolları devreye soktuğunu anlamak, hedefe yönelik ilaçların daha akıllıca kombinasyonlarını yönlendirebilir—özellikle G12C mutantı için, KRAS inhibitörlerini Wnt veya Notch bloke edicilerle eşleştirmenin daha iyi tedavilere giden yeni bir yol sunabileceği olasıdır.
Atıf: Yang, M.H., Sheth, S., Shui, B. et al. The impact of K-Ras Gly12 mutants on homeostasis and tumorigenesis in the colonic epithelium. Oncogene 45, 1828–1839 (2026). https://doi.org/10.1038/s41388-026-03771-3
Anahtar kelimeler: KRAS mutasyonları, kolon kanseri, allel-spesifik tedavi, tümör sinyalizasyonu, kombinasyon hedefleme